Clear Sky Science · pt
Colecistoquinina derivada de células beta impulsiona o desenvolvimento de adenocarcinoma pancreático associado à obesidade
Quando o Excesso de Peso Conversa com o Pâncreas
Sabe-se que a obesidade aumenta o risco de câncer de pâncreas, um dos mais letais, mas a “conversa” biológica que liga o excesso de gordura corporal aos tumores tem sido obscura. Este estudo revela um mensageiro inesperado: um hormônio digestivo chamado colecistoquinina, ou CCK, produzido dentro das células que fabricam insulina no pâncreas. Ao traçar como essas células mudam sob estresse metabólico, os autores mostram como um hormônio pensado para ajudar o corpo a lidar pode, em vez disso, alimentar o câncer, e sugerem novas formas de interceptar a doença antes que ela se estabeleça.
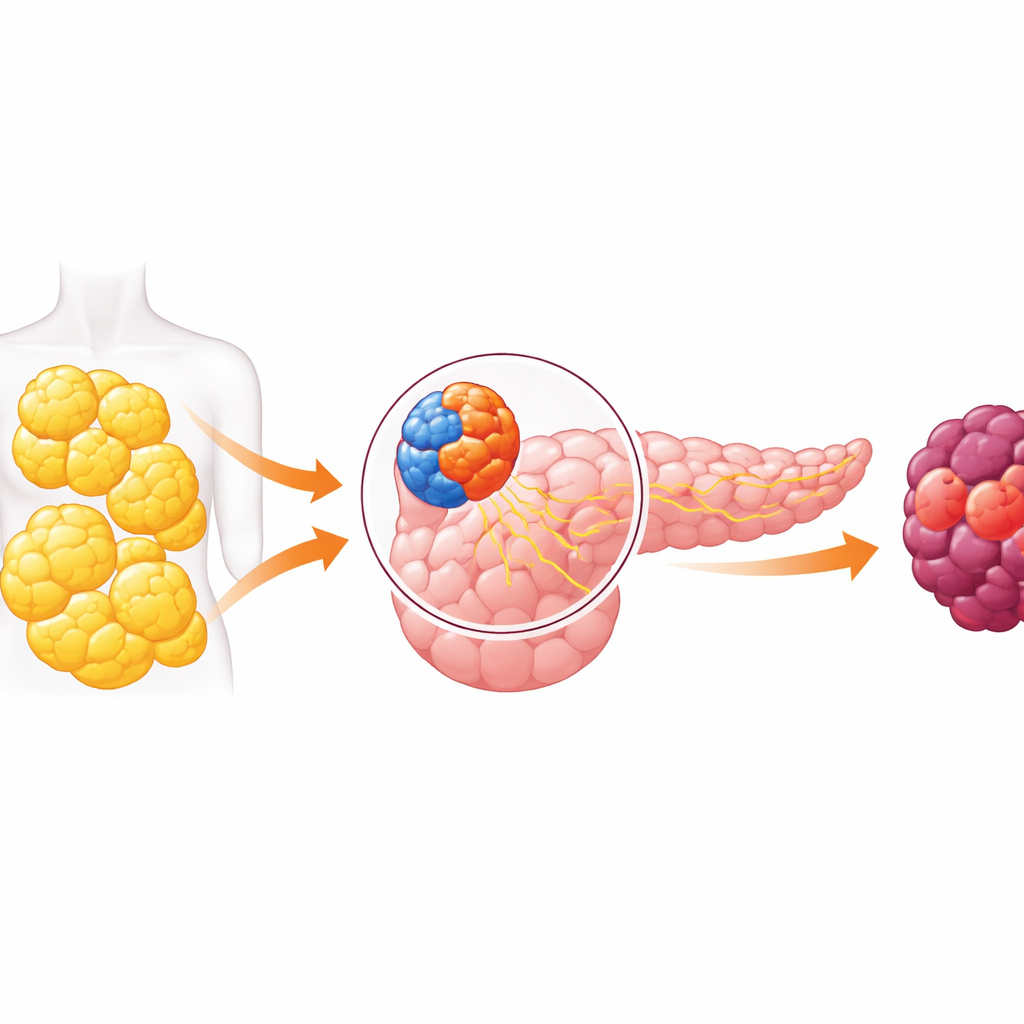
Um Órgão de Dois Lados e um Diálogo Perigoso
O pâncreas tem duas funções principais. Um lado, a parte endócrina, contém pequenas ilhotas de células que liberam hormônios como a insulina para controlar o açúcar no sangue. O outro, a porção exócrina, produz sucos digestivos e inclui as células que mais frequentemente dão origem ao câncer pancreático. Durante anos, os pesquisadores presumiram que esses compartimentos funcionavam em grande parte isolados. Trabalhos recentes derrubaram essa ideia, mostrando que sinais de células produtoras de hormônios podem influenciar as células digestivas vizinhas. Este artigo mergulha nesse diálogo e constata que, na obesidade, ele pode empurrar o lado digestivo do pâncreas na direção do câncer.
Estresse nas Células Hormônio Gera um Novo Sinal
Na obesidade, as células beta produtoras de insulina sofrem pressão constante para suprir a demanda crescente por insulina. Usando sequenciamento de RNA de célula única e ferramentas computacionais avançadas, os pesquisadores acompanharam células beta individuais enquanto camundongos passavam de magros a com sobrepeso e, depois, severamente obesos. Eles descobriram que um subconjunto de células beta imaturas expandiu-se e gradualmente perdeu sua identidade especializada de insulina. Conforme essas células ficavam estressadas, aumentaram marcadores de sobrecarga no dobramento de proteínas e de dano celular, enquanto a produção de insulina diminuía. Ao mesmo tempo, essas células passaram a produzir altos níveis de CCK, um hormônio geralmente associado ao intestino que pode estimular as células digestivas a crescer e se transformar.
De Hormônio Útil a Combustível para o Câncer
Para testar se essa CCK recém-produzida era apenas um subproduto do estresse ou um motor ativo da doença, a equipe engenheirou camundongos cujas células beta produziam CCK extra, mesmo sem obesidade. Esses animais desenvolveram pré-câncer pancreático e tumores invasivos em grau semelhante ao observado em camundongos obesos, apesar de apresentarem peso e glicemia normais. Em contraste, quando a CCK foi removida especificamente do pâncreas de camundongos obesos, a carga tumoral caiu acentuadamente, embora os animais continuassem pesados e com níveis elevados de insulina. Em vários modelos de camundongo, os níveis de CCK no pâncreas acompanharam de perto a quantidade de tumor, enquanto os níveis de insulina tendiam a mover-se na direção oposta. Isso indicou que a CCK — e não a insulina — era o hormônio dominante conectando obesidade ao câncer pancreático nesses sistemas.
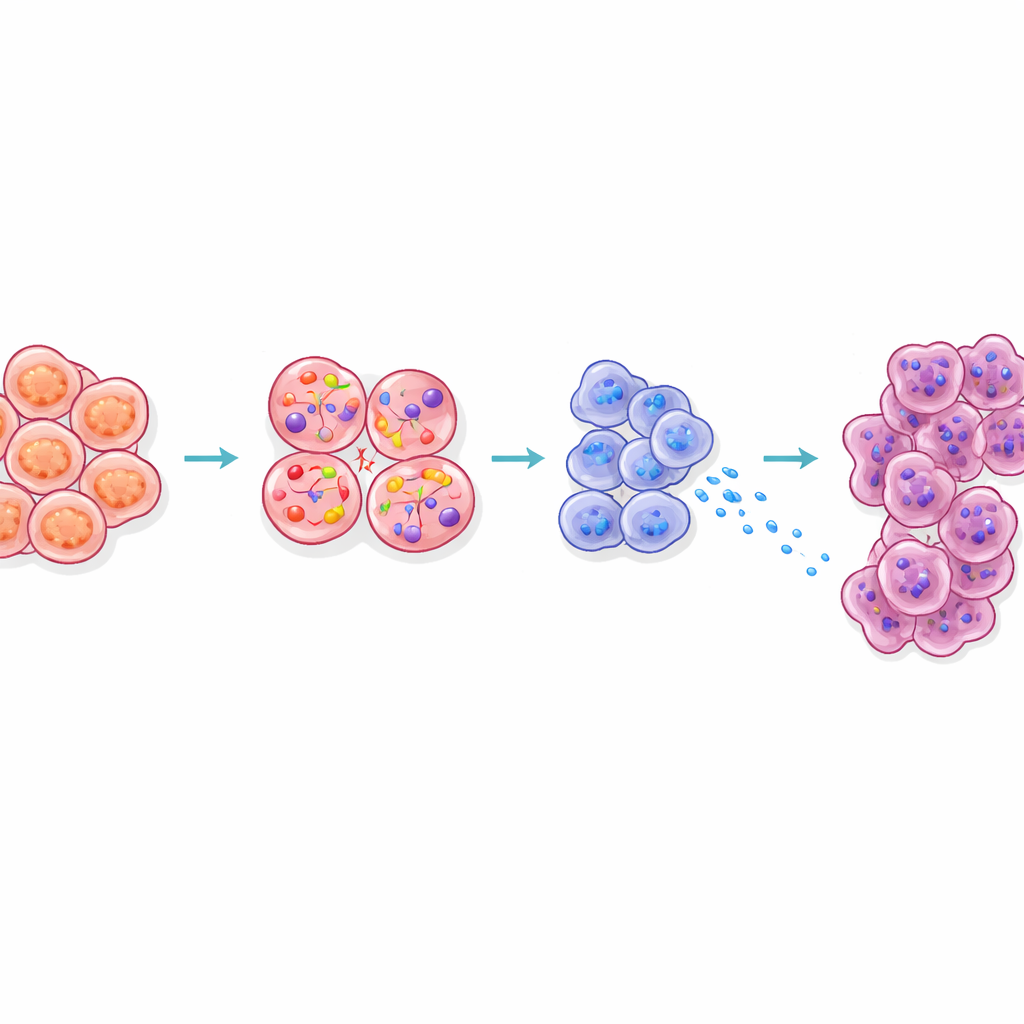
Como o Sinal Alcança e Prepara Células Vizinhas
O estudo também examinou como a CCK das células beta remodela o tecido circundante. Células acinares, que normalmente secretam enzimas digestivas, ficam bem próximas às ilhotas no pâncreas. Em camundongos obesos, as células acinares próximas às ilhotas exibiram assinatura de estresse, produziram mais enzimas digestivas e proteínas chamadas Reg, e migraram para estados conhecidos por serem mais facilmente transformados em câncer. Bloquear a sinalização da CCK em camundongos obesos reduziu esses sinais Reg. Imagens tridimensionais revelaram ainda que lesões precancerosas iniciais tendiam a surgir incomumente próximas às ilhotas em animais obesos. Em conjunto, esses resultados sugerem que a difusão de CCK a partir de células beta estressadas cria uma “zona quente” ao redor das ilhotas onde as células digestivas ficam predispostas a se transformar em tumores.
Padrões Compartilhados com Diabetes Humana e um Interruptor Chave
Ao comparar dados de camundongos com tecido pancreático humano de pessoas com e sem diabetes tipo 2, os autores encontraram paralelos marcantes: células beta de doadores diabéticos mapearam-se nos mesmos estados estressados e menos maturados observados em camundongos obesos. Em seguida, eles usaram uma análise regulatória para perguntar o que liga a CCK nas células beta e identificaram uma via responsiva ao estresse centrada na proteína cJun. Quando bloquearam a via JNK–cJun a montante em camundongos obesos ou em células semelhantes a beta em cultura, os níveis de CCK caíram, e observou-se cJun ligando-se próximo a uma região regulatória do gene CCK. Isso sugere que o estresse crônico ativa JNK–cJun, que por sua vez converte as células beta para um modo produtor de CCK.
O Que Isso Significa para Pessoas em Risco
Para um leitor leigo, a mensagem central é que, sob a pressão da obesidade e do diabetes, as células produtoras de insulina no pâncreas não apenas falham — elas se adaptam de maneira que, inadvertidamente, incentivam células vizinhas a formar câncer. Fazem isso ao ativar a CCK, um hormônio que atua como sinal de crescimento e de estresse para células digestivas vizinhas, ajudando a criar um terreno fértil para tumores. Como a CCK proveniente do pâncreas não é essencial para manter o controle da glicemia, mirar essa fonte específica do hormônio ou seu interruptor ativado pelo estresse poderia, em princípio, reduzir o risco de câncer pancreático em pessoas com obesidade ou diabetes tipo 2 sem comprometer o equilíbrio hormonal geral. O trabalho recontextualiza o câncer de pâncreas como uma doença de comunicação mal direcionada entre os dois lados do órgão e destaca novas vias para prevenção precoce.
Citação: Garcia, C.C., Venkat, A., McQuaid, D.C. et al. Beta cell-derived cholecystokinin drives obesity-associated pancreatic adenocarcinoma development. Nat Commun 17, 3292 (2026). https://doi.org/10.1038/s41467-026-69821-2
Palavras-chave: câncer de pâncreas, obesidade, células beta, colecistoquinina, diabetes tipo 2