Clear Sky Science · pt
Formação do domínio PIN composto SMG5-SMG6 é essencial para NMD
Como as Células se Protegem de Mensagens Defeituosas
Nossas células leem constantemente mensagens genéticas (mRNAs) para produzir proteínas. Mas essas mensagens às vezes contêm sinais de término prematuros que produziririam proteínas truncadas e potencialmente nocivas. O processo que destrói essas mensagens defeituosas é chamado decaimento de mRNA mediado por nonsense (NMD). Este artigo revela como duas proteínas-chave, SMG5 e SMG6, cooperam fisicamente para cortar mensagens defeituosas, explicando um mistério de longa data sobre como funciona o controle de qualidade celular.
Encontrando a Parceria Oculta
Durante anos, os cientistas sabiam que o SMG6 pode cortar RNA diretamente, enquanto o SMG5 era considerado “cataliticamente inativo” e atuava principalmente como ajudante ou andaime. Ainda assim, experimentos em células mostravam algo intrigante: o SMG6 não funcionava corretamente sem o SMG5, e o NMD colapsava se qualquer um dos dois estivesse ausente. Os autores usaram previsão de estrutura de ponta (AlphaFold), ensaios bioquímicos com proteínas purificadas e testes genéticos em linhagens celulares humanas para resolver essa contradição. Seus modelos previram que as regiões finais do SMG5 e do SMG6, chamadas domínios PIN, se encaixam lado a lado para formar uma estrutura conjunta. Essa unidade composta — apelidada de “cPIN” — foi proposta como a verdadeira máquina de corte no NMD. 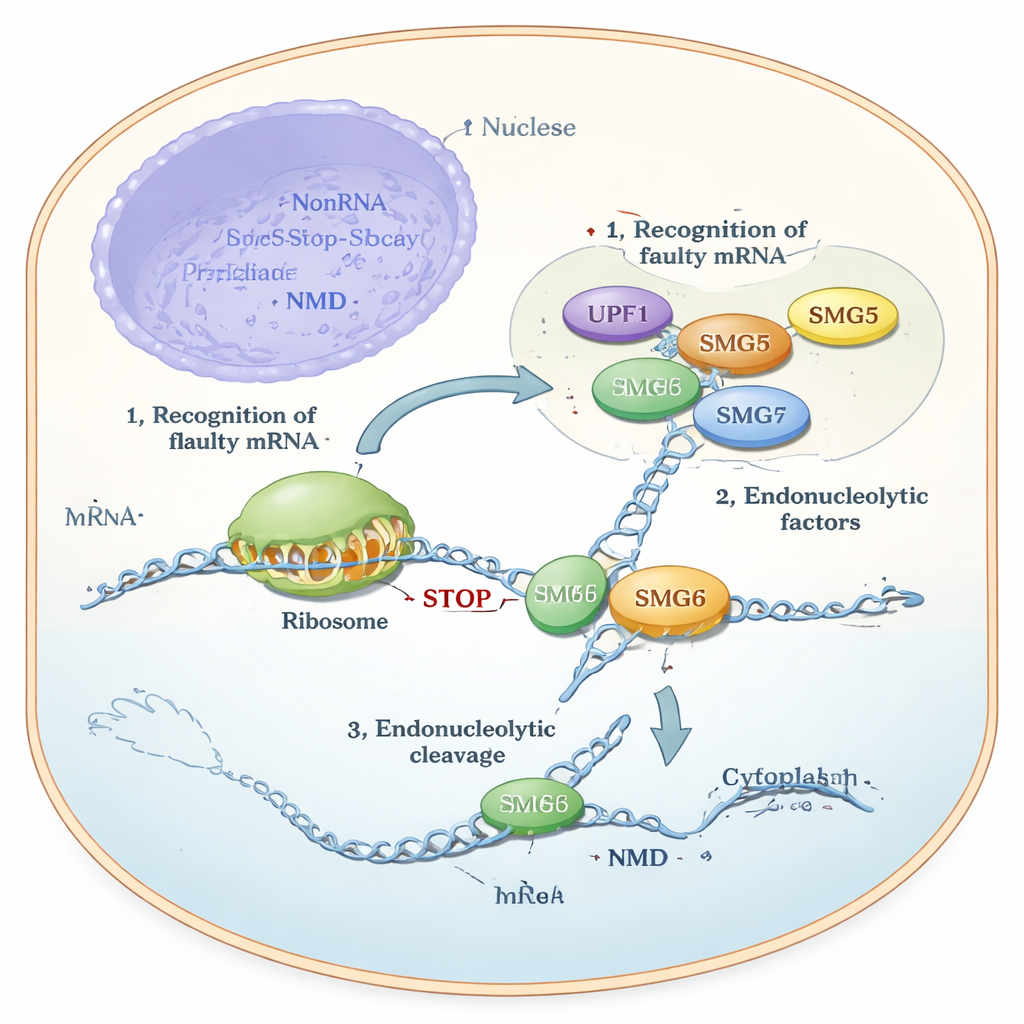
Reconstruindo as Tesouras Moleculares em Tubo de Ensaio
Para testar a previsão, a equipe produziu fragmentos humanos de SMG5 e SMG6 em bactérias e os purificou. Sozinho, o SMG6 mostrou apenas uma fraca capacidade de cortar um substrato de RNA projetado, e o SMG5 isolado mostrou praticamente nenhuma atividade. Mas quando os dois fragmentos foram misturados, a atividade de clivagem aumentou acentuadamente, mesmo em condições nas quais enzimas contaminantes dificilmente teriam papel. O mesmo efeito apareceu em moléculas‑teste de RNA lineares e circulares, indicando que o aumento da clivagem vinha realmente do par SMG5–SMG6. Reações de crosslink químico e espectrometria de massa também mostraram que as duas proteínas entram em contato próximo, apoiando a ideia de uma parceria direta, ainda que transitória.
Completando a Lâmina de Corte
Os modelos estruturais sugeriram exatamente como o SMG5 potencializa o SMG6. O SMG6 contribui com quatro aminoácidos ácidos que coordenam íons metálicos no centro do sítio de corte, como é típico nessa família de enzimas. Surpreendentemente, os modelos colocaram um resíduo ácido adicional do SMG5 bem ao lado deles, estendendo efetivamente o bolso catalítico. Outros resíduos carregados positivamente no SMG5 foram previstos para agarrar o esqueleto do RNA e ajudar a posicioná‑lo para a clivagem. Quando os pesquisadores mutaram esses resíduos críticos do SMG5 ou do SMG6, o complexo composto perdeu grande parte de sua capacidade de corte in vitro. As mesmas mutações também falharam em resgatar o NMD em células humanas modificadas onde a proteína normal havia sido depletada, vinculando firmemente o modelo estrutural à função celular real. 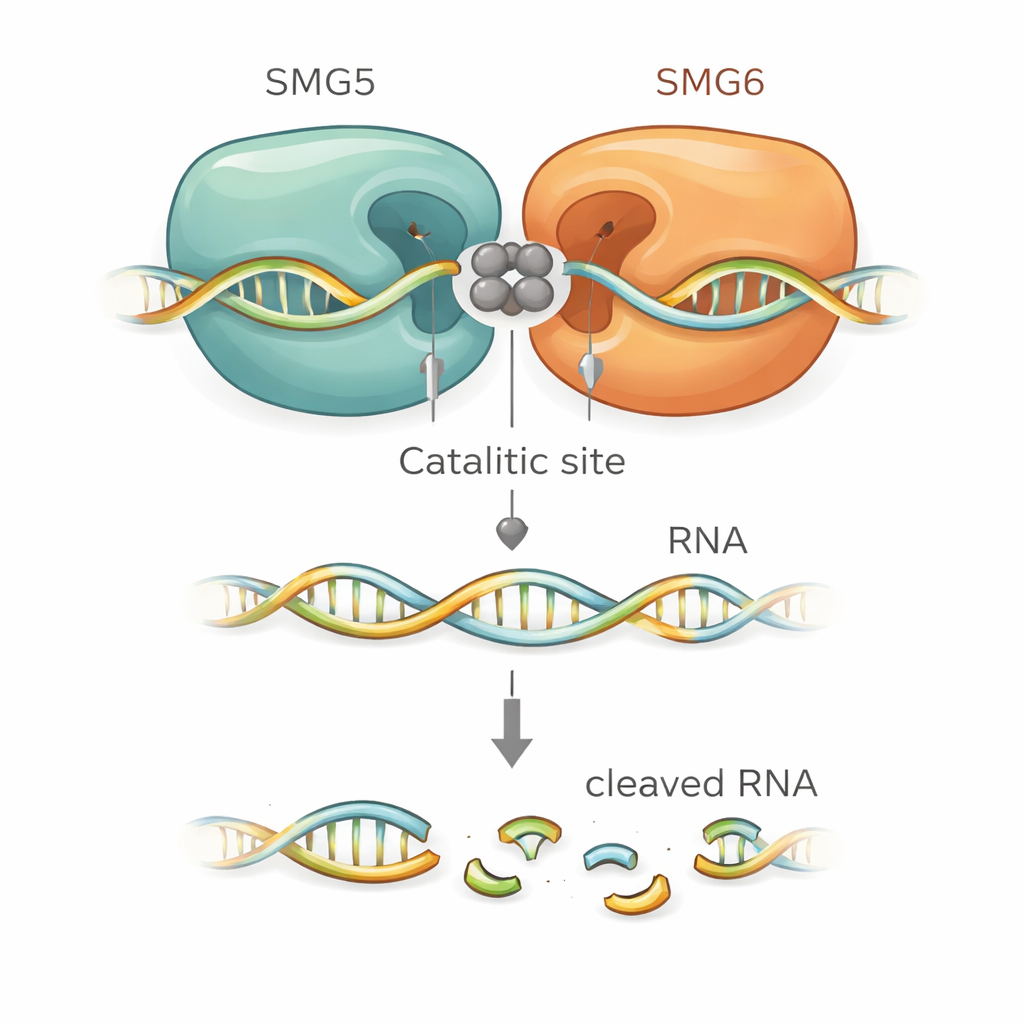
Provando que Ambos os Parceiros São Essenciais nas Células
Como a remoção completa de SMG5 ou SMG6 mata as células, a equipe usou um sistema de “degron” que permite marcar cada proteína para que ela possa ser rapidamente destruída por uma pequena molécula. Combinando essa degradação rápida com interferência de RNA, obtiveram remoção quase total de SMG5, SMG6 ou de um regulador central chamado UPF1. O sequenciamento de RNA em escala genômica revelou então o que acontece ao NMD quando cada fator é perdido. A depleção de SMG5 ou UPF1 produziu mudanças quase idênticas nos RNAs celulares, com transcritos defeituosos e sensíveis ao NMD se acumulando fortemente. A remoção do SMG6 causou um efeito muito similar, embora ligeiramente mais brando. Esses dados mostram que SMG5 e SMG6 não são ramos paralelos opcionais da via; ao contrário, atuam juntos com UPF1 como componentes centrais de uma rota principal de decaimento.
Por que Isso Importa para a Saúde Celular
Em termos simples, o estudo demonstra que SMG5 e SMG6 se encaixam para formar um par molecular único e poderoso de tesouras que corta mensagens genéticas defeituosas. O SMG6 fornece a maior parte da lâmina, mas o SMG5 supre um fio ausente e ajuda a manter o RNA no lugar, transformando um cortador fraco em um eficiente. Esse “cPIN” composto explica por que as células exigem absolutamente ambas as proteínas para manter suas mensagens de RNA limpas. Ao esclarecer como o passo-chave de corte do NMD é ativado somente quando mensagens defeituosas são reconhecidas, o trabalho oferece uma imagem mais clara de como as células evitam o acúmulo de proteínas truncadas e tóxicas e ajustam finamente a expressão gênica.
Citação: Kurscheidt, K., Theunissen, S., Pasquali, N. et al. Composite SMG5-SMG6 PIN domain formation is essential for NMD. Nat Commun 17, 1934 (2026). https://doi.org/10.1038/s41467-026-69819-w
Palavras-chave: decaimento de mRNA mediado por nonsense, controle de qualidade de RNA, SMG5 SMG6, vigilância de mRNA, regulação da expressão gênica