Clear Sky Science · pt
Análogos de acetil-lisina não hidrolisáveis para estudar a acetilação de proteínas in vitro e em células
Por que pequenas etiquetas químicas nas proteínas importam
Dentro de cada célula, proteínas são constantemente ajustadas com pequenas etiquetas químicas que funcionam como interruptores liga/desliga ou dimmers para sua atividade. Uma das mais importantes dessas etiquetas é a acetilação, que pode alterar o comportamento de uma proteína sem mudar seu código genético subjacente. Entender exatamente o que a acetilação faz em um sítio específico de uma proteína específica tem sido surpreendentemente difícil, porque as células podem remover essas etiquetas tão rapidamente quanto as adicionam. Este estudo apresenta um engenhoso "substituto" químico para a acetilação que não pode ser removido, oferecendo aos cientistas uma forma de congelar esses interruptores no lugar e observar o que acontece.
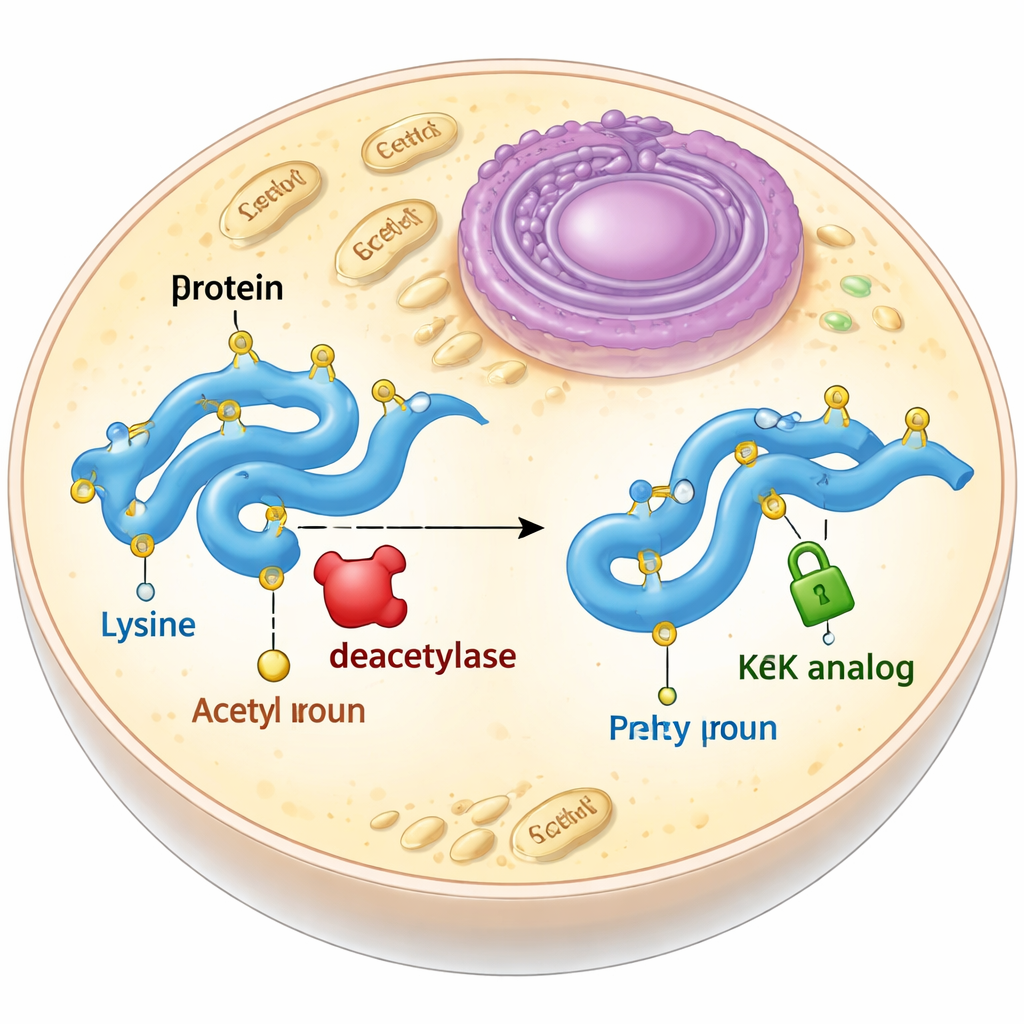
Um substituto estável para uma etiqueta efêmera
A acetilação geralmente ocorre em um bloco de construção das proteínas chamado lisina. Quando uma lisina é acetilada, ela perde sua carga positiva e sua cadeia lateral fica um pouco mais longa. Biólogos frequentemente tentam imitar isso mutando a lisina para outro aminoácido, glutamina, que é neutra, mas mais curta, ou adicionando acetil-lisina verdadeira usando expansão do código genético. Ambas as abordagens têm desvantagens: a glutamina não reproduz totalmente as mudanças de forma causadas pela acetilação, e a acetil-lisina verdadeira é rapidamente removida por enzimas chamadas desacetilases dentro das células. Os autores se propuseram a desenhar e testar semelhantes à acetil-lisina que mantivessem o tamanho e a forma corretos, mas que não pudessem ser removidos.
Testando novos imitadores químicos em uma proteína modelo
A equipe concentrou-se primeiro na ubiquitina, uma proteína pequena e bem estudada que por sua vez é decorada com muitas etiquetas diferentes. Usando engenharia genética avançada, eles colocaram variantes de lisina em uma posição da ubiquitina: acetil-lisina natural, dois análogos não removíveis chamados TFAcK e cetolisina (KeK), e substitutos comuns como glutamina, alanina e arginina. Em seguida, examinaram como essas mudanças afetavam a forma e a função da ubiquitina. Medidas de RMN de alta resolução mostraram que acetil-lisina, TFAcK e KeK produziram quase idênticas alterações estruturais, especialmente em torno de um hélice central, enquanto glutamina e outras mutações simples não o fizeram. Testes funcionais usando uma enzima chamada HDM2 revelaram que a ubiquitina contendo acetil-lisina, TFAcK ou KeK se comportava de forma semelhante entre si e diferente da versão com glutamina, destacando que o comprimento e o volume da cadeia lateral — não apenas sua carga — são cruciais.
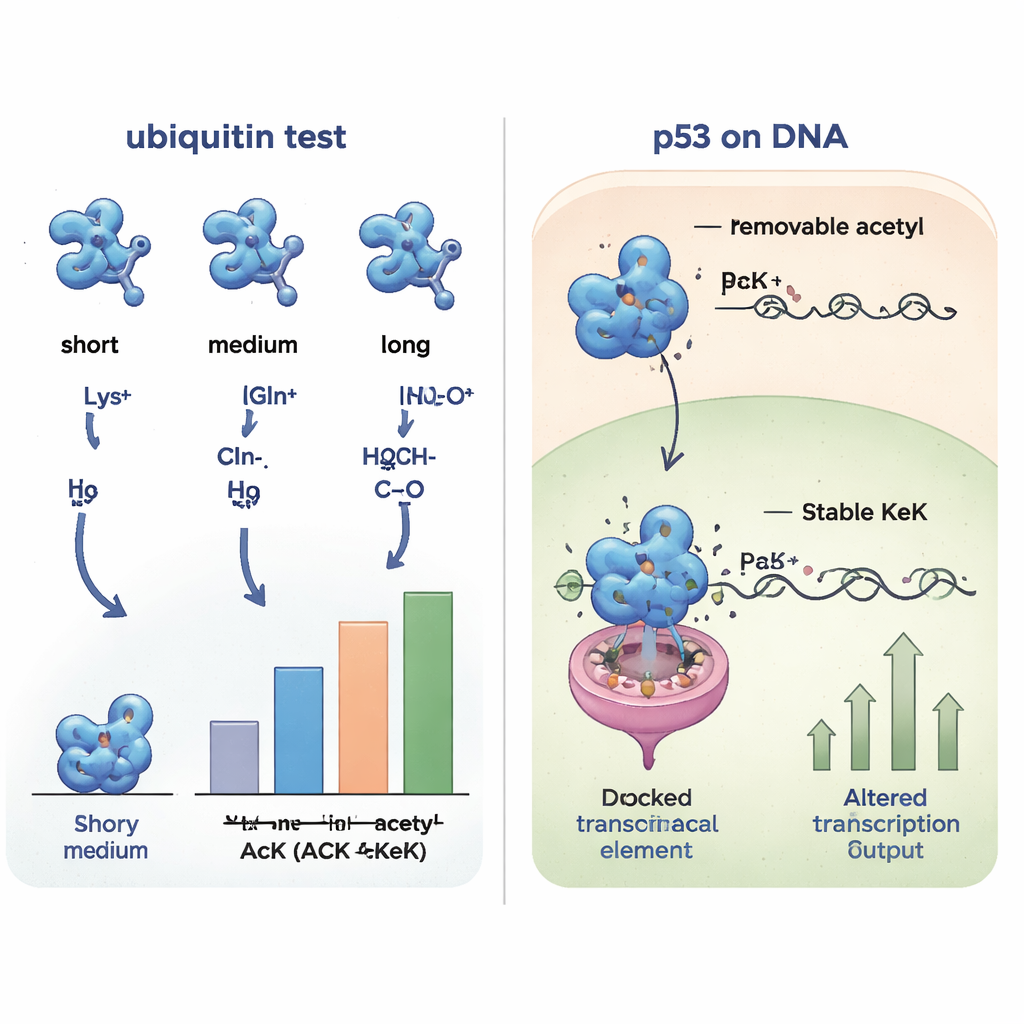
Sondando parcerias proteicas por toda a célula
Como pequenas mudanças estruturais podem alterar com quais parceiros uma proteína interage, os pesquisadores compararam em seguida como as várias versões de ubiquitina se ligavam a outras proteínas extraídas de células humanas. Pescando parceiros de união e identificando-os por espectrometria de massa, eles descobriram que a ubiquitina contendo acetil-lisina, TFAcK ou KeK apresentava padrões de interação muito semelhantes, enquanto formas contendo glutamina ou alanina se agrupavam e pareciam diferentes. Variantes carregadas positivamente (lisina ou arginina) formaram outro grupo. Essa comparação sistemática mostrou que os análogos não removíveis TFAcK e, especialmente, KeK imitam tanto a estrutura quanto o comportamento de ligação da acetilação verdadeira muito melhor do que a tradicional substituição por glutamina.
Congelando a acetilação no supressor tumoral p53
Para verificar se essas ferramentas funcionam dentro de células vivas, os autores recorreram ao p53, um supressor tumoral chave frequentemente chamado de "guardião do genoma." Lisinas específicas na região de ligação ao DNA do p53 podem ser acetiladas, alterando quais genes ele ativa, como aqueles que interrompem o ciclo celular ou desencadeiam a morte celular. A equipe engenheirou células humanas para que o p53 incorporasse acetil-lisina, TFAcK ou KeK em duas posições de lisina importantes (120 e 164) somente quando o aminoácido não padrão correspondente fosse fornecido. Todos os três puderam ser incorporados ao p53, mas medições detalhadas mostraram que, nas células, os grupos acetil e TFAcK foram amplamente removidos por desacetilases, enquanto KeK permaneceu intacto. Quando testaram a capacidade do p53 de ativar um gene repórter e o gene natural p21, variantes carregando KeK nesses sítios foram muito menos ativas, correspondendo ao esperado quando a acetilação nessas posições está bloqueada, enquanto acetil-lisina e TFAcK se comportaram mais como o p53 normal porque haviam sido desacetilados.
O que isso significa para estudar decisões celulares
No geral, o estudo mostra que KeK é um substituto fiel e não removível para a acetil-lisina: ele reproduz de perto as mudanças estruturais, as preferências de interação e as consequências funcionais da acetilação, mas não pode ser apagado por enzimas celulares. Para não especialistas, isso significa que os pesquisadores agora têm uma forma de "congelar" um interruptor químico normalmente reversível em um único sítio de uma proteína e então observar como isso afeta processos como regulação gênica e decisões de destino celular. Isso deve facilitar muito separar os papéis específicos da acetilação daqueles de outras modificações sobrepostas, e pode, em última instância, esclarecer como a acetilação de proteínas mal regulada contribui para doenças como o câncer.
Citação: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
Palavras-chave: acetilação de proteínas, modificação pós-traducional, ubiquitina, p53, expansão do código genético