Clear Sky Science · pt
Remodelação transcriptômica dinâmica em células progenitoras neurais humanas transplantadas revela mecanismos de preservação da visão em um modelo de rato com retinite pigmentosa
Por que proteger a visão em declínio é importante
Retinite pigmentosa é um grupo de doenças hereditárias que roubam gradualmente a visão das pessoas, frequentemente começando com cegueira noturna e avançando até a cegueira legal. Como centenas de mutações gênicas diferentes podem causar essa condição, tratar cada uma individualmente com terapia gênica é difícil. Este estudo explora uma abordagem mais universal: transplantar células progenitoras neurais humanas — células nervosas imaturas cultivadas em laboratório — no olho para proteger as células sensíveis à luz que ainda restam. Entender exatamente como essas células transplantadas se comportam e ajudam a preservar a visão pode moldar tratamentos futuros não só para retinite pigmentosa, mas também para outros distúrbios que causam cegueira.
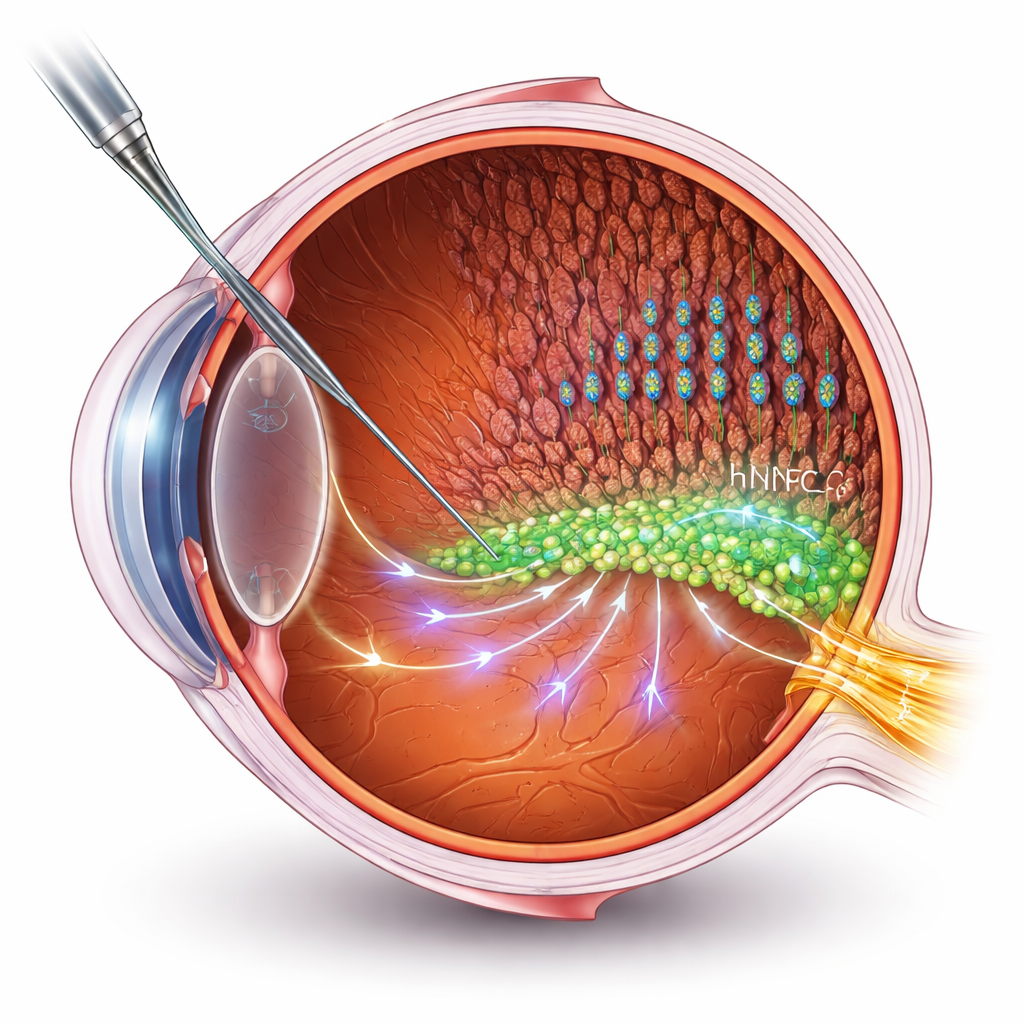
Ajudar células em vez de substituí-las
Muitas terapias com células-tronco visam substituir células mortas ou danificadas. Mas, em doenças retinais avançadas, reconstruir novas conexões com o cérebro é um grande desafio técnico. Aqui, os pesquisadores seguem outro caminho: usar células progenitoras neurais humanas (hNPCs) como “ajudantes” que sustentam as próprias células retinais do paciente. Eles transplantaram hNPCs no espaço subretiniano de um modelo de rato bem conhecido para retinite pigmentosa e então mediram a visão usando registros elétricos e testes comportamentais. Os ratos tratados mantiveram melhor função visual e camadas de fotorreceptores — bastonetes e cones que captam a luz — mais intactas do que os animais não tratados, embora a degeneração tenha continuado a progredir lentamente.
Como as células transplantadas mudam dentro do olho doente
Para ver o que acontece em nível molecular, a equipe usou sequenciamento de RNA de célula única, uma técnica que perfila quais genes estão ativados em milhares de células individuais. Acompanharam as hNPCs transplantadas em dois pontos temporais, aproximadamente estágios iniciais e mais tardios após o transplante. Em vez de se transformarem em novos fotorreceptores, a maioria das células transplantadas amadureceu em células de suporte semelhantes a astrócitos, com uma fração menor exibindo marcadores de oligodendrócitos ou neurônios imaturos. Com o tempo, essas células se estabilizaram, adotando características que sugerem que estão ajustadas para sobreviver em um ambiente estressante e degenerativo e para interagir estreitamente com as células retinais vizinhas.
Sinais de proteção, metabolismo e limpeza
As hNPCs produziram uma mistura rica de proteínas protetoras conhecidas como fatores tróficos. Entre elas estavam MANF e MYDGF, ligadas à sobrevivência celular, redução do estresse oxidativo e atenuação da inflamação, além de outros fatores como midkine e pleiotrofina que suportam o crescimento e o movimento de células neurais. Essas moléculas pareciam agir tanto no próprio enxerto quanto na retina circundante. Nos ratos tratados, bastonetes e cones mostraram padrões de atividade gênica mais próximos dos controles saudáveis, com suporte melhorado à sinalização visual e à manutenção celular. As células transplantadas também impulsionaram vias envolvidas na remoção de detritos celulares e no ajuste do metabolismo, sugerindo que ajudam os fotorreceptores a lidar com as demandas energéticas e os subprodutos tóxicos que se acumulam durante a doença.
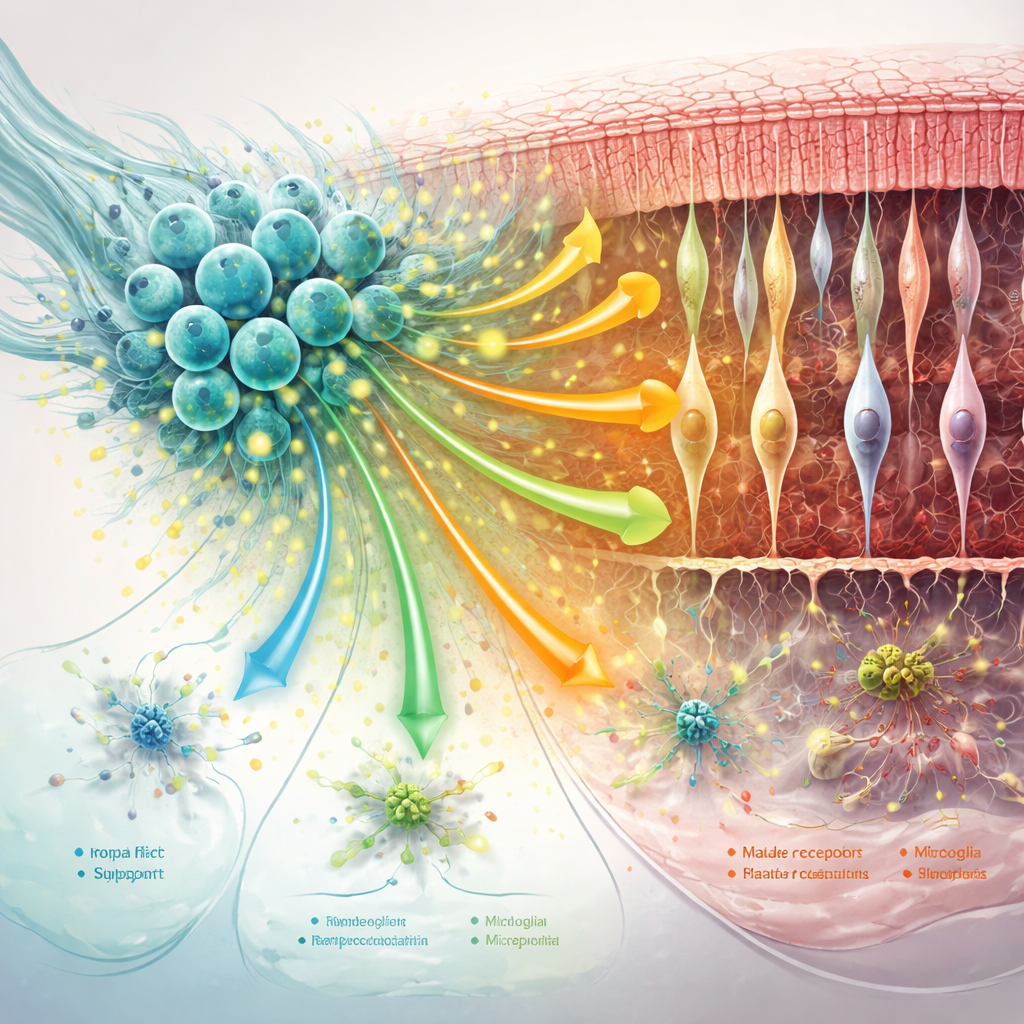
Acalmando as células de suporte e remodelando o ambiente retinal
A rede de suporte da retina — glia de Müller, microglia e a matriz proteica ao redor — exerce um papel importante em agravar ou retardar a degeneração. O estudo constatou que o tratamento com hNPCs reduziu marcadores-chave de mudanças “reativas” nocivas nas células de Müller e deslocou a microglia de estados excessivamente inflamatórios, especialmente em pontos temporais mais precoces. Ao mesmo tempo, sinais de comunicação que ajudam a estabilizar sinapses, manter a adesão entre células e preservar o arcabouço ao redor dos fotorreceptores foram fortalecidos. À medida que a doença avançou, alguns desses benefícios diminuíram: a comunicação entre células enfraqueceu, certas vias protetoras — incluindo a sinalização relacionada à MANF — declinaram, e as células de suporte adotaram perfis mais voltados ao estresse e à resposta imune.
O que isso significa para terapias oculares futuras
Para o leitor não especializado, a mensagem principal é que células progenitoras neurais humanas transplantadas podem agir como “socorristas” no local em uma retina em degeneração. Elas não reconstróem a retina do zero, mas liberam moléculas protetoras, ajustam o metabolismo, acalmam inflamações prejudiciais e ajudam a manter a estrutura local intacta — tudo isso retardando a perda de visão. No entanto, esse efeito protetor diminui com o tempo à medida que o ambiente se torna mais hostil e o diálogo entre enxerto e células do hospedeiro enfraquece. Os autores sugerem que potencializar fatores-chave como MANF e melhorar a saúde da retina hospedeira — possivelmente por meio de engenharia genética do enxerto ou tratamentos combinados — pode ser essencial para transformar um alívio temporário em preservação duradoura da visão.
Citação: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
Palavras-chave: retinite pigmentosa, terapia com células-tronco, degeneração retinal, neuroproteção, sequenciamento de RNA de célula única