Clear Sky Science · pt
Limitações da clonagem serial em mamíferos
Por que copiar mamíferos não é tão simples quanto parece
Durante décadas, a ideia de copiar animais — até o nível do seu DNA — fascinou o público, de Dolly, a ovelha, aos sonhos de ressuscitar espécies extintas. Mas os mamíferos podem realmente se sustentar apenas pela clonagem, geração após geração, como fazem algumas plantas e animais simples? Este estudo acompanhou uma linhagem de camundongos produzida inteiramente por clonagem ao longo de quase 20 anos para descobrir. Os resultados explicam por que, apesar de nossos avanços técnicos, a natureza ainda depende fortemente da reprodução sexual para manter os mamíferos saudáveis a longo prazo.
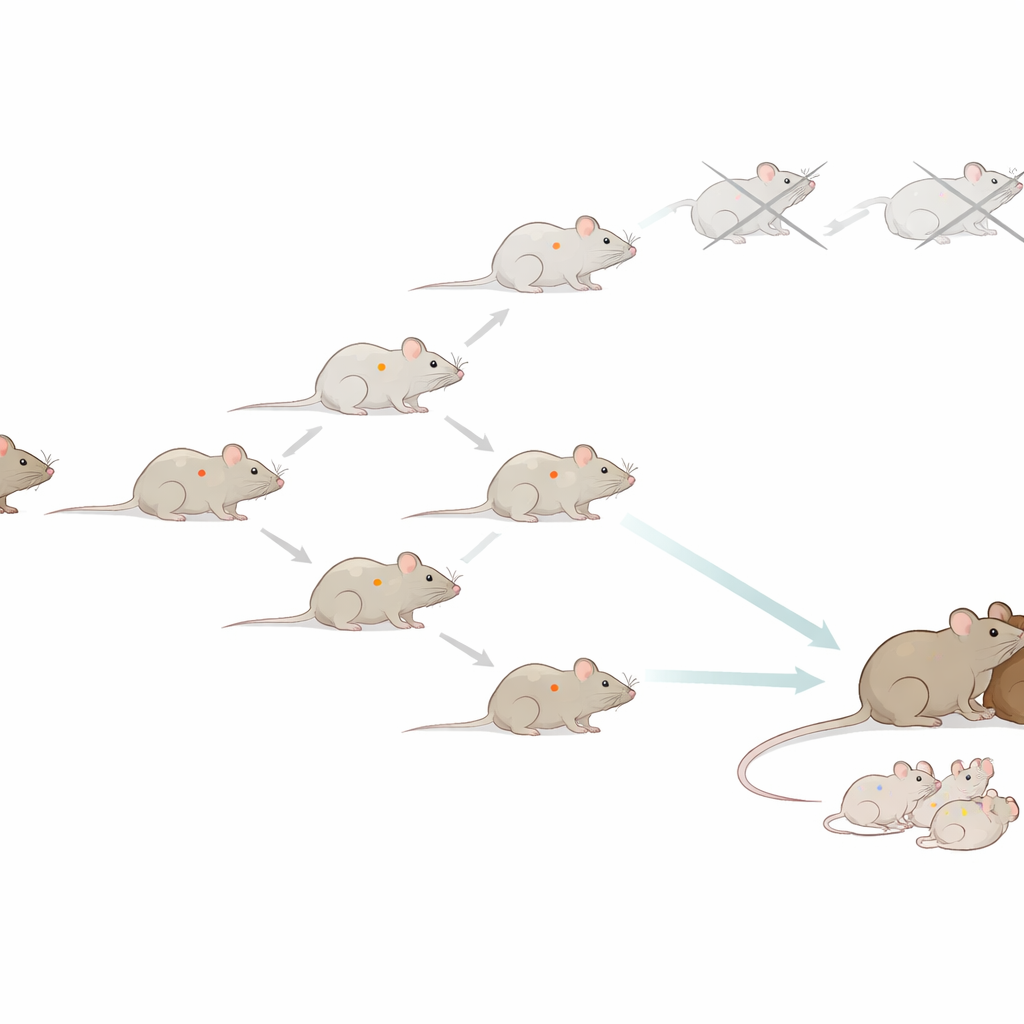
Acompanhando uma linhagem de camundongos por vinte anos
Os pesquisadores começaram com uma única fêmea e usaram suas células somáticas para criar um camundongo clonado. Quando esse primeiro clone cresceu, eles retiraram células dele para fazer o próximo clone, repetindo o processo sucessivamente. No total, foram tentados mais de 30.000 procedimentos de transferência nuclear e produzidos mais de 1.200 animais clonados, alcançando 58 gerações a partir da doadora original. Muitos desses camundongos pareciam e comportavam-se como animais comuns, com expectativa de vida em torno de dois anos e pesos corporais semelhantes. A princípio, a taxa de sucesso da clonagem até melhorou a cada geração, sugerindo que a clonagem serial de mamíferos poderia ser prática a longo prazo.
Corpos saudáveis, mas danos ocultos
Na superfície, os camundongos clonados pareciam bem. Seus órgãos internos e, especialmente, suas placentas exibiram as peculiaridades conhecidas de experimentos de clonagem, como serem maiores que as de camundongos concebidos naturalmente, mas essas anomalias não pioraram a cada geração. A equipe também avaliou o desenvolvimento de embriões em laboratório e examinou os padrões de marcas químicas nas proteínas que empacotam o DNA — características que frequentemente falham na clonagem. Embriões iniciais de clones de gerações tardias se assemelhavam muito aos da primeira geração clonada. Isso sugeriu que os problemas de “reprogramação” conhecidos na clonagem não estavam se acumulando de forma constante ao longo do tempo.
Mutações se infiltram a cada cópia
A história real emergiu quando os cientistas sequenciaram os genomas de camundongos de diferentes gerações de clonagem. A cada rodada de cópia, surgiam novas alterações no DNA: em média cerca de 70 mutações de uma única base e uma a duas alterações estruturais por geração, incluindo grandes rearranjos e perdas cromossômicas. Muitas dessas alterações lembravam mutações naturais observadas na reprodução comum, mas a diferença crucial é que, na clonagem, não há a recombinação de cromossomos via acasalamento que ajuda a eliminar variantes deletérias. Com o tempo, especialmente após cerca da 25ª geração, mutações danosas — como a perda de um cromossomo X inteiro ou quebras e trocas entre cromossomos — começaram a se acumular. A proporção de mutações com probabilidade de interromper genes importantes quase dobrou nas gerações posteriores.
Óvulos revelam o ponto de ruptura
Para ver como esse dano oculto afetava a reprodução, a equipe concentrou-se nos óvulos de fêmeas clonadas de gerações tardias. Quando esses óvulos foram induzidos a se desenvolver sem espermatozoide, quase nenhum progrediu para embriões iniciais saudáveis, indicando que muitos carregavam combinações letais de mutações. A fertilização com espermatozoides de machos normais melhorou o desenvolvimento em parte, mas o sucesso ainda caiu acentuadamente nas gerações posteriores. Experimentos que trocaram o núcleo e o material citoplasmático entre óvulos de camundongos normais e de clones tardios mostraram que tanto o material genético quanto o citoplasma dos óvulos estavam comprometidos. Eventualmente, na 58ª geração, todos os descendentes clonados morreram pouco depois do nascimento e a linha de clonagem não pôde ser continuada.
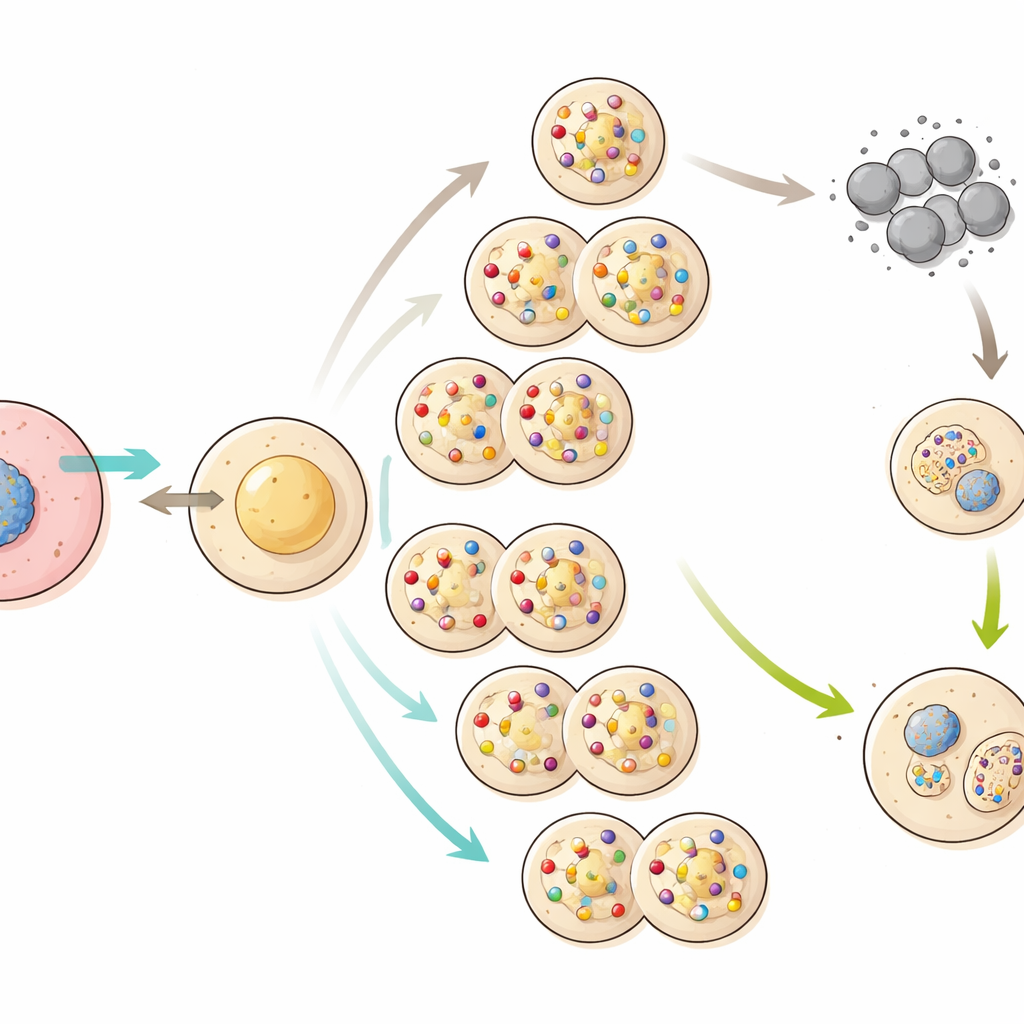
A reprodução sexual como sistema de reparo
Quando os cientistas permitiram que camundongos clonados de gerações tardias se acasalassem naturalmente com machos normais, apareceu um padrão diferente. Embora essas mães clonadas tivessem ninhadas pequenas, alguns de seus filhotes — e especialmente seus netos — estavam muito mais saudáveis. As placentas da geração seguinte encolheram em direção a um tamanho mais próximo do normal e o desenvolvimento geral melhorou. Isso sugere que a mistura e a triagem de cromossomos durante a formação de óvulos e espermatozoides, seguida pela fertilização, pode separar combinações de mutações deletérias e eliminar muitas das piores alterações. Em outras palavras, o sexo atuou como um sistema de limpeza embutido que a clonagem pura não tem.
O que isso significa para o futuro da clonagem
Ao rastrear cuidadosamente uma única linhagem clonada de camundongo por 57 gerações bem-sucedidas, este trabalho demonstra que os mamíferos não podem depender apenas da clonagem para sustentar uma linhagem indefinidamente. Saúde visível e expectativa de vida normal podem mascarar um declínio genético lento, à medida que mutações se acumulam silenciosamente até que a reprodução falhe. Embora a clonagem permaneça uma ferramenta poderosa — para resgatar animais em risco, multiplicar animais de criação valiosos ou preservar recursos genéticos — é improvável que substitua a reprodução sexual como estratégia de longo prazo para a sobrevivência dos mamíferos. O estudo fornece forte respaldo experimental à ideia de que, em animais complexos, o sexo não é apenas uma forma de gerar descendentes — é manutenção essencial do genoma.
Citação: Wakayama, S., Ito, D., Inoue, R. et al. Limitations of serial cloning in mammals. Nat Commun 17, 2495 (2026). https://doi.org/10.1038/s41467-026-69765-7
Palavras-chave: clonagem animal, mutações genéticas, reprodução de camundongos, reprodução assexuada, evolução do sexo