Clear Sky Science · pt
TCL1A media defeitos de metilação do DNA em mola hidatiforme recorrente com variantes patogênicas de NLRP7
Por que isso importa para a saúde das mulheres
Algumas gestações dão errado muito cedo, transformando‑se em uma massa de tecido placentário anormal em vez de um feto em desenvolvimento. Essa condição, chamada mola hidatiforme, pode se repetir em algumas mulheres e, às vezes, progredir para câncer. Este estudo investiga uma causa genética importante desses eventos raros, porém graves, e revela como uma única salvaguarda defeituosa no óvulo pode desregular os “selos” químicos que orientam o desenvolvimento saudável.
Um problema de gravidez enraizado no óvulo
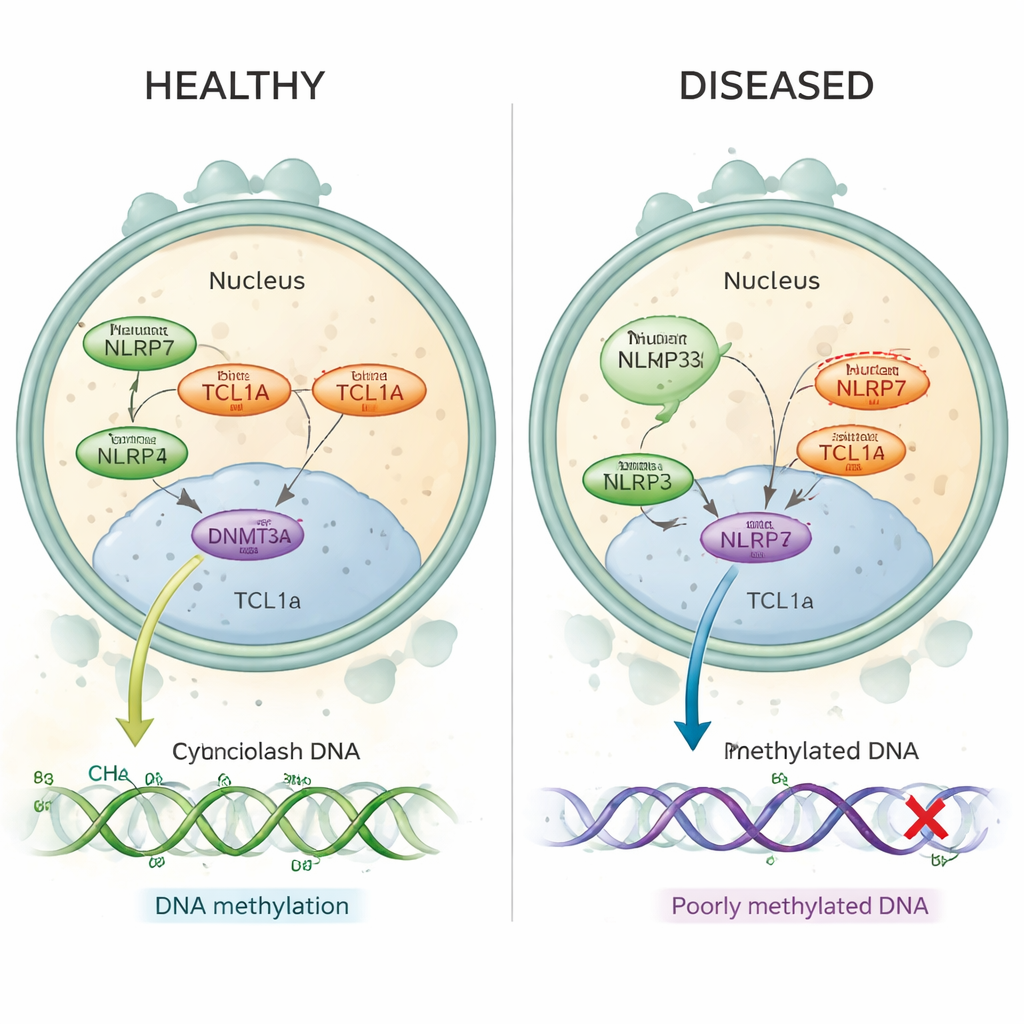
A mola hidatiforme recorrente é um distúrbio em que mulheres experimentam gestações molares repetidas, frequentemente sem nenhuma gestação normal entre elas. Muitos desses casos são agora conhecidos por serem causados por alterações prejudiciais em um gene chamado NLRP7, que é ativo no óvulo antes e logo após a fertilização. Nesses casos, trechos-chave do DNA que deveriam carregar “imprints” maternos carecem das marcas normais de metilação — pequenas etiquetas químicas que ajudam a ligar ou desligar genes no momento certo. Até agora, os cientistas não entendiam como uma proteína que fica no citoplasma do óvulo, como a NLRP7, poderia controlar a metilação que ocorre no DNA embalado dentro do núcleo.
Encontrando um parceiro que faltava
Para resolver esse quebra-cabeça, os pesquisadores examinaram óvulos humanos descartados e embriões muito precoces de clínicas de fertilidade. Eles precipitaram NLRP7 e seus parceiros conhecidos dessas células e identificaram outras proteínas que vêm junto. Uma se destacou: TCL1A, já conhecida em cânceres sanguíneos como uma proteína que pode entrar no núcleo e interferir com enzimas metiltransferases do DNA chamadas DNMT3A e DNMT3B. TCL1A é incomumente abundante em óvulos humanos, o que sugere que desempenha um papel importante ali. Testes detalhados de interação mostraram que TCL1A se liga de forma forte e específica à NLRP7, mas não a proteínas intimamente relacionadas, e que esse complexo está integrado em uma estrutura maior específica do óvulo chamada complexo materno subcortical.
Vendo o abraço molecular
A equipe então usou crio‑microscopia eletrônica para visualizar a estrutura tridimensional do complexo NLRP7–TCL1A. Eles descobriram que duas moléculas de NLRP7 se emparelham e cada uma envolve um dímero de TCL1A ao longo de uma superfície curva de motivos repetidos. Esse arranjo explica por que muitas alterações causadoras de doença em NLRP7 se concentram ao longo dessa superfície: alterar pontos de contato críticos enfraquece ou destrói o abraço com TCL1A. Quando os pesquisadores recriaram mais de 50 variantes conhecidas de pacientes em células, a maioria das versões ligadas a gestações molares recorrentes ou desestabilizou a NLRP7 ou reduziu drasticamente sua capacidade de ligar a TCL1A.
Como proteínas deslocadas perturbam as marcas do DNA
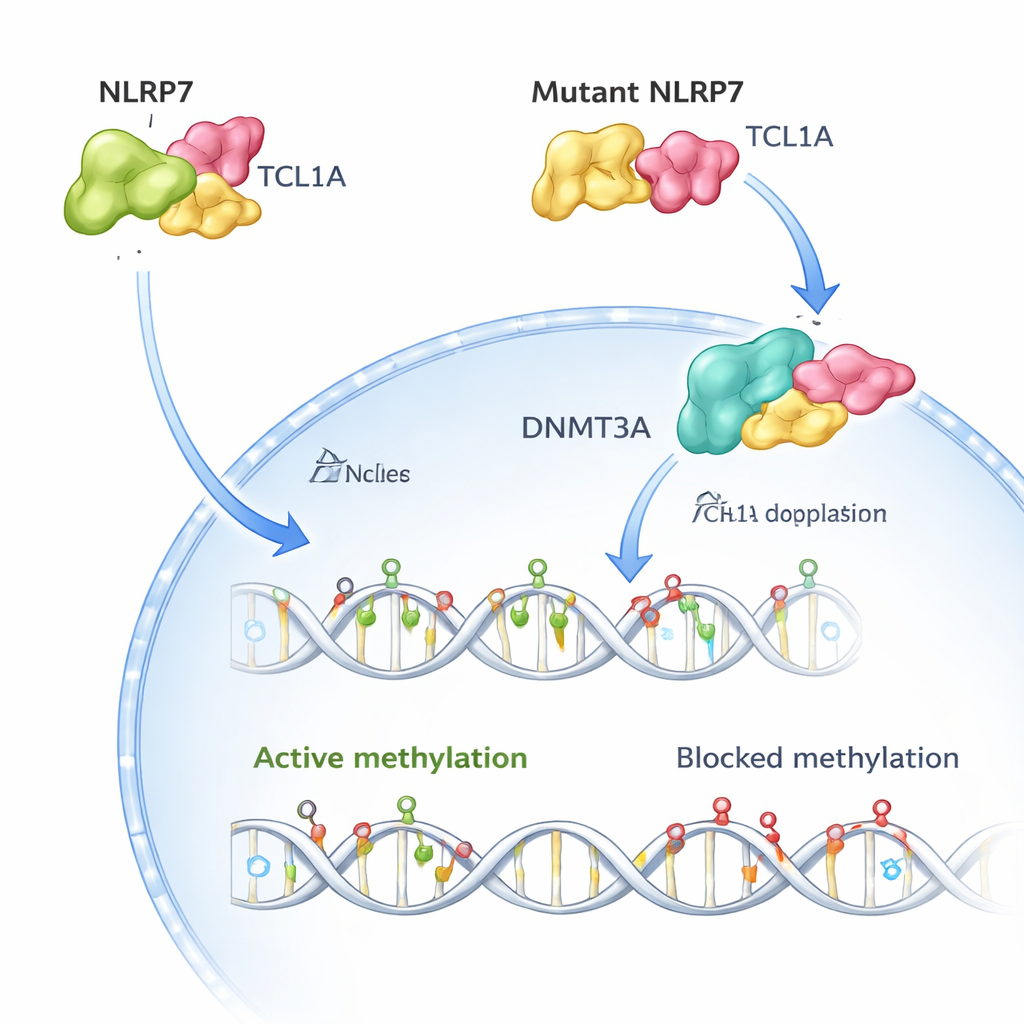
Em óvulos humanos saudáveis, tanto NLRP7 quanto TCL1A são encontrados principalmente no citoplasma, com apenas uma pequena quantidade de TCL1A alcançando o núcleo. Os autores mostram que NLRP7 atua efetivamente como um porteiro: quando consegue segurar a TCL1A, esta permanece fora do núcleo. Quando NLRP7 está mutada e não consegue mais se ligar bem, TCL1A vaza para o núcleo. Lá, ela se associa à DNMT3A, a principal enzima que deposita novas marcas de metilação nos óvulos, e diminui sua atividade. Em modelos de células‑tronco que normalmente ganham metilação à medida que amadurecem, a superexpressão de TCL1A causou uma perda dramática de metilação em todo o genoma, enquanto a coexpressão de NLRP7 resgatou parcialmente esse defeito. Juntos, esses achados sustentam um quadro simples: NLRP7 normal mantém um “freio” de metilação (TCL1A) preso no citoplasma para que a DNMT3A possa rotular o DNA adequadamente; NLRP7 defeituosa deixa esse freio escapar para o núcleo e bloqueia o processo.
Do mecanismo ao diagnóstico
Além de explicar como surgem as gestações molares recorrentes, o estudo sugere uma maneira prática de julgar se uma alteração recém‑descoberta em NLRP7 em uma paciente é realmente prejudicial. Os autores comparam três abordagens — testes laboratoriais da ligação NLRP7–TCL1A, previsões por computador e ferramentas de pontuação genética padrão — e mostram que a perda da ligação com TCL1A se alinha estreitamente com variantes que causam doença. Eles também identificam uma variante prejudicial previamente não reconhecida, L766R, em famílias com molas recorrentes, confirmando que ela tanto enfraquece a proteína quanto redireciona TCL1A para o núcleo.
O que isso significa em termos simples
Este trabalho revela uma reação em cadeia molecular por trás de um distúrbio de gravidez raro, porém devastador. Em essência, óvulos de mulheres afetadas carregam uma proteína “guarda‑costas” quebrada, NLRP7, que não consegue manter sua parceira TCL1A fora do núcleo. Uma vez lá dentro, TCL1A interfere com a enzima que escreve etiquetas químicas vitais no DNA. Sem essas etiquetas, a placenta precoce cresce de forma anormal e um bebê não pode se formar. Ao traçar essa via passo a passo, o estudo esclarece por que certas alterações genéticas nas mães podem sabotar repetidamente as gestações e aponta para aconselhamento genético e diagnóstico mais precisos para mulheres com molas hidatiformes recorrentes.
Citação: Gao, Z., Liu, Q., Li, L. et al. TCL1A mediates DNA methylation defects in recurrent hydatidiform mole with NLRP7 pathogenic variants. Nat Commun 17, 2160 (2026). https://doi.org/10.1038/s41467-026-69744-y
Palavras-chave: metilação do DNA, mola hidatiforme recorrente, NLRP7, TCL1A, imprinting genômico