Clear Sky Science · pt
GCN5 impulsiona a progressão da MASLD via via de sinalização LXRα/SREBP1c–mediada pela lipogênese de novo
Por que essa história do fígado importa
A doença hepática esteatótica associada à disfunção metabólica (MASLD), anteriormente chamada de doença hepática gordurosa não alcoólica, agora afeta cerca de uma em cada quatro pessoas no mundo. Frequentemente se desenvolve de forma silenciosa, mas pode evoluir para fibrose, câncer de fígado e sérios problemas metabólicos. Este estudo revela um “botão de volume” molecular que contribui para o acúmulo nocivo de gordura no fígado e mostra como reduzi‑lo pode tanto proteger o fígado quanto potencialmente tornar mais seguras estratégias terapêuticas já usadas no tratamento cardíaco.
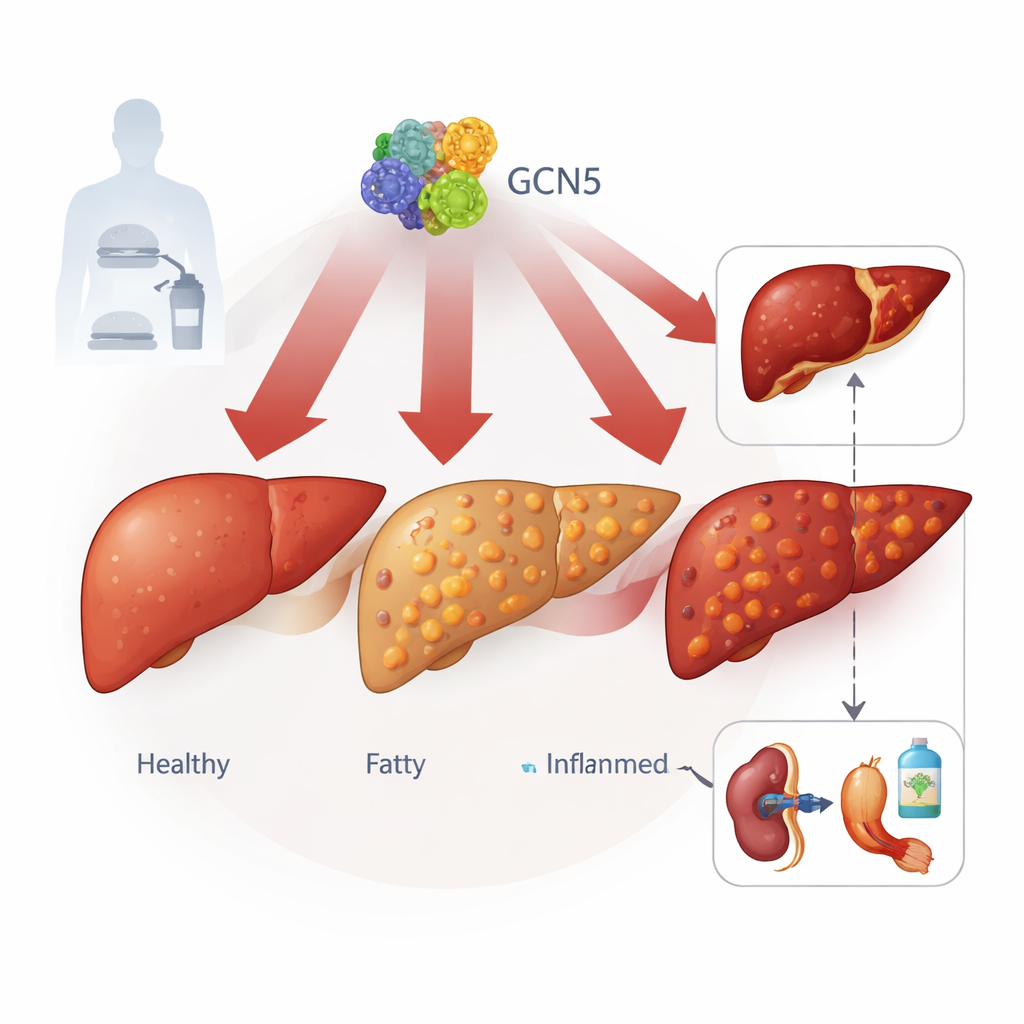
Um interruptor oculto dentro das células do fígado
Os autores se concentraram em uma proteína chamada GCN5, mais conhecida por regular o grau de compactação do DNA. Ao estudar tecido hepático de mais de 100 pessoas, que iam de saudáveis a casos graves de MASLD, e em vários modelos murinos de fígado gorduroso induzido por dieta, eles descobriram que os níveis de GCN5 nas células do fígado aumentam de forma contínua à medida que a doença piora. Uma proteína intimamente relacionada, PCAF, não mostrou esse padrão, sugerindo que GCN5 desempenha um papel específico. Altos níveis de GCN5 acompanharam maior gordura hepática, lipídios sanguíneos mais elevados e sinais mais fortes de lesão hepática, ligando esse interruptor molecular à gravidade clínica da doença.
Aumentando ou diminuindo GCN5 em animais
Para testar causa e efeito, a equipe aumentou geneticamente ou removeu GCN5 especificamente nas células do fígado de camundongos. Quando GCN5 foi elevado, os animais submetidos a uma dieta rica em gordura desenvolveram fígados mais pesados e gordurosos, níveis sanguíneos de lipídios mais altos e mais dano às células hepáticas, mesmo sem comerem mais ou ganharem peso corporal extra. Células do fígado cultivadas em placas comportaram‑se de forma semelhante: excesso de GCN5 levou a gotículas lipídicas maiores e mais numerosas. Por outro lado, camundongos projetados para não expressar GCN5 apenas nas células hepáticas ficaram fortemente protegidos. Em vários modelos dietéticos que imitam a MASLD humana e sua forma inflamatória mais severa, esses animais acumularam menos gordura no fígado, apresentaram níveis menores de lipídios e enzimas hepáticas no sangue e desenvolveram menos inflamação e fibrose.
Como GCN5 estimula a produção de gordura pelo fígado
Ao mergulhar no metabolismo, os pesquisadores mediram muitos ácidos graxos e seus blocos de construção no fígado. A perda de GCN5 reduziu principalmente os lipídios que o fígado sintetiza do zero, um processo conhecido como lipogênese de novo, enquanto deixou relativamente inalterados os ácidos graxos poli‑insaturados derivados da dieta. Experimentos de expressão gênica e rastreamento com isótopos mostraram que GCN5 atua acima de um regulador mestre da lipogênese chamado SREBP1c. Quando GCN5 estava ativo, genes que constroem e modificam ácidos graxos eram ativados, e a taxa interna de fabricação de gordura do fígado aumentava. Remover ou bloquear GCN5 reduziu esse programa, cortando o fluxo de carbono do açúcar para a nova gordura hepática.
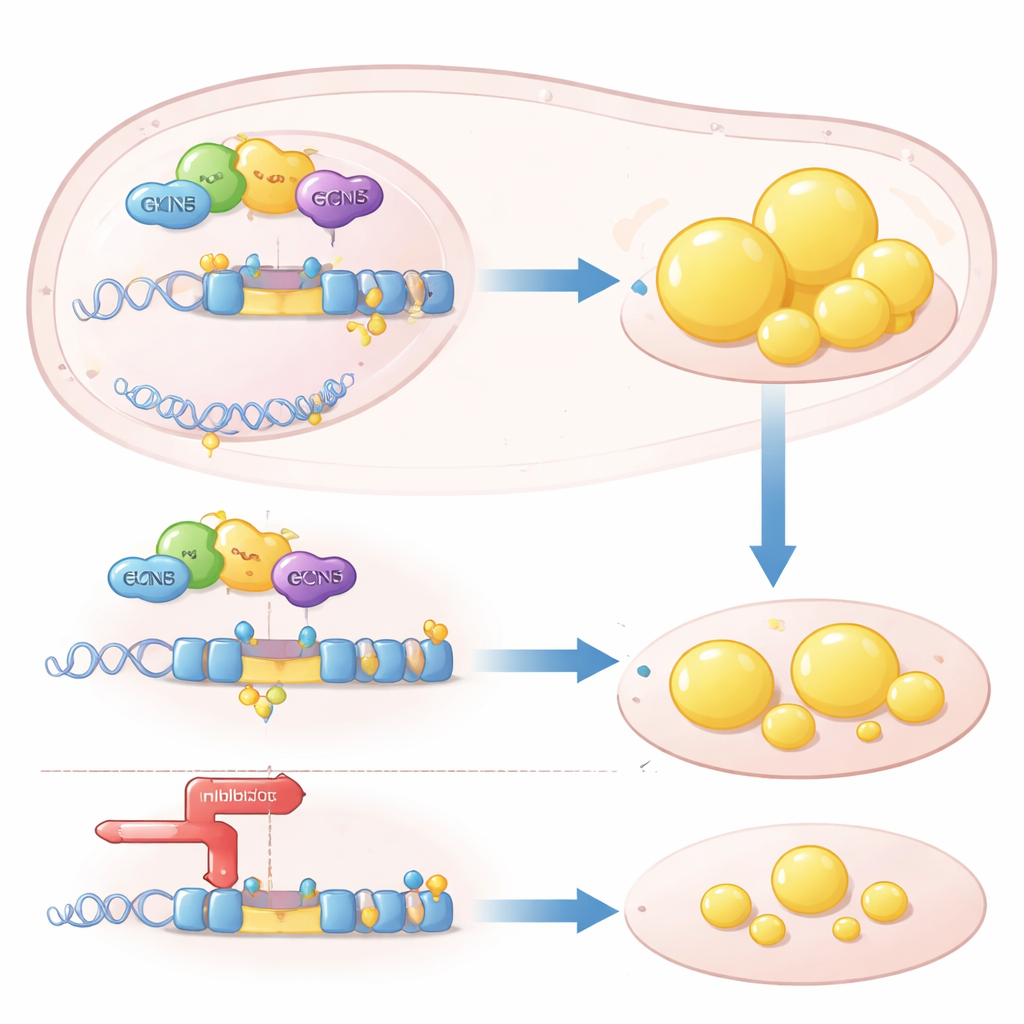
Uma alavanca epigenética sobre um gene-chave da gordura
Mecanisticamente, GCN5 atua como uma alavanca “epigenética”: modifica quimicamente proteínas histonas no DNA para tornar certos genes mais fáceis de serem lidos. Os autores demonstraram que GCN5 é recrutado à região de controle do gene SREBP1c juntamente com um receptor nuclear chamado LXRα, que detecta moléculas relacionadas ao colesterol. Uma vez lá, GCN5 adiciona marcas de acetilação à histona H3, afrouxando a cromatina local e estimulando a transcrição de SREBP1c. Esse efeito foi altamente seletivo: GCN5 ampliou a capacidade de LXRα de ativar SREBP1c, mas não outro alvo de LXR, o ABCA1, que ajuda a remover colesterol dos tecidos. Sem GCN5, LXRα não conseguia engajar eficientemente o promotor de SREBP1c, e o programa downstream de síntese de lipídios estagnou.
Um candidato a fármaco e uma combinação promissora
A equipe então testou o CPTH2, um inibidor de pequena molécula de GCN5 que se concentra no fígado. Em modelos murinos já submetidos a dietas gordurosas, o CPTH2 reduziu o tamanho do fígado, o teor de gordura e marcadores de lesão sem toxicidade óbvia ou mudanças na ingestão de alimento. Em células hepáticas humanas e murinas cultivadas, o CPTH2 diminuiu gotículas de gordura e triglicerídeos somente quando GCN5 estava presente, confirmando que sua ação é específica. Importante, tanto em células quanto em camundongos tratados com compostos ativadores de LXR (projetados para melhorar a remoção de colesterol e combater a aterosclerose), o CPTH2 bloqueou seletivamente o aumento indesejado da produção de gordura dirigida por SREBP1c enquanto preservava genes que promovem o transporte reverso de colesterol. Quando combinado com um agonista de LXR em camundongos alimentados com dieta rica em gordura, o CPTH2 reduziu ainda mais os lipídios sanguíneos nocivos e o colesterol hepático e preveniu o acúmulo adicional de gordura no fígado.
O que isso significa para os pacientes
O estudo posiciona GCN5 como um motor central do acúmulo de gordura hepática na MASLD ao conectar sinais dietéticos e hormonais ao interruptor de produção de gordura SREBP1c. Como GCN5 parece ser dispensável para o braço benéfico de LXR que limpa colesterol, fármacos que inibem GCN5 — como o CPTH2 ou sucessores mais avançados — poderiam controlar a gordura e a inflamação hepáticas ao mesmo tempo em que permitem que terapias que protegem o coração funcionem. Para pessoas em risco tanto de doença hepática gordurosa quanto de doença cardiovascular, mirar esse interruptor epigenético pode um dia oferecer uma maneira de proteger o fígado sem sacrificar os benefícios do melhor manejo do colesterol.
Citação: Xiao, HT., Song, P., Jin, J. et al. GCN5 drives MASLD progression through LXRα/SREBP1c signaling pathway–mediated de novo lipogenesis. Nat Commun 17, 2821 (2026). https://doi.org/10.1038/s41467-026-69736-y
Palavras-chave: doença hepática gordurosa, epigenética, metabolismo lipídico, metabolismo hepático, receptores nucleares