Clear Sky Science · pt
Controle não‑quelante em alquilações de cetonas α‑oxi usando allylatranes do grupo 14
Construindo formas moleculares com maior precisão
Muitos medicamentos e produtos naturais funcionam apenas quando seus átomos estão arranjados em uma forma tridimensional muito específica. Quimistas, portanto, dedicam enorme esforço a aprender como “empurrar” novos fragmentos em uma molécula vindo de um lado ou de outro. Este artigo descreve uma nova maneira de anexar grupos allyl—cadeias curtas de três carbonos—a uma classe comum de moléculas, permitindo o acesso a estruturas imagem‑espelho que eram muito difíceis de obter até agora.
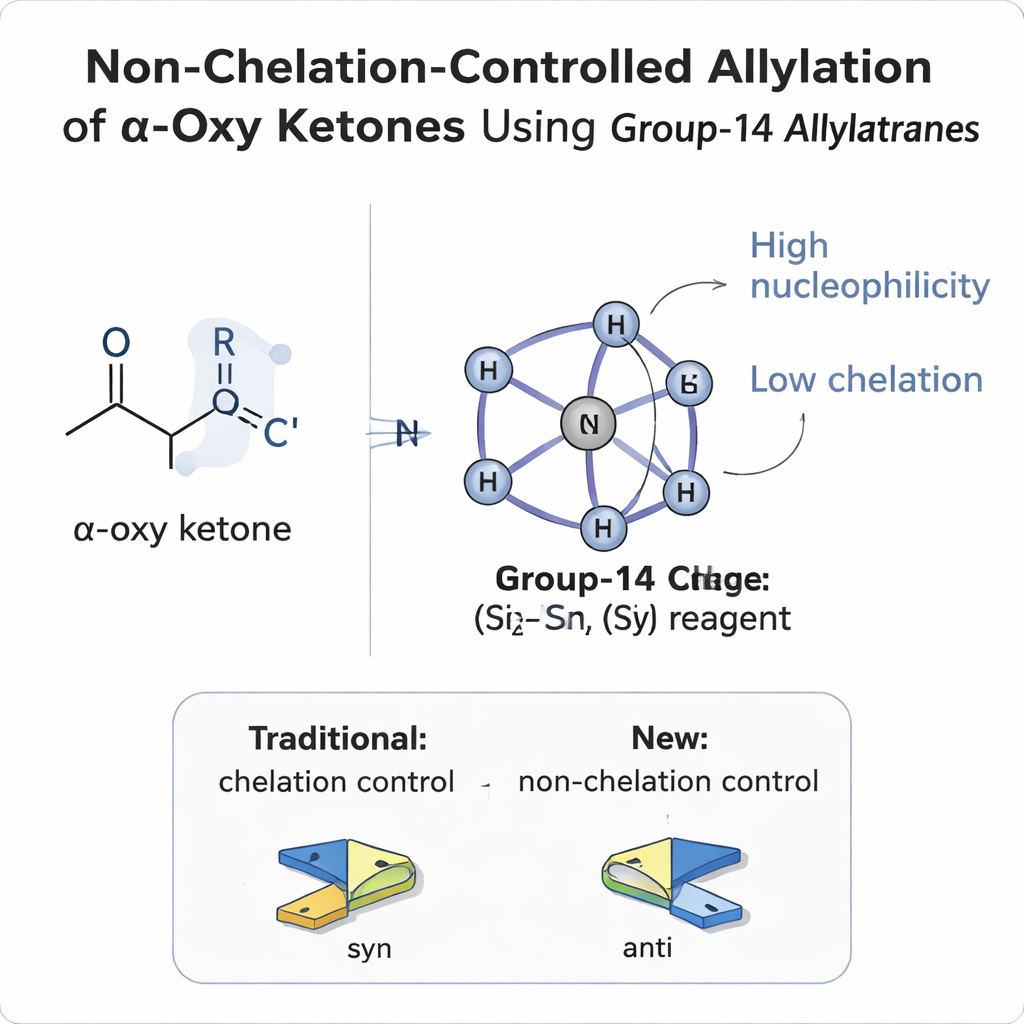
Por que controlar os lados de uma molécula é tão difícil
Quando um novo grupo é adicionado a uma ligação carbono–oxigênio dupla plana (um carbonila), ele pode atacar de qualquer uma das faces, como uma bola atingindo uma moeda por cima ou por baixo. Se já existe um substituinte vizinho no carbono adjacente (a posição α), o resultado são dois produtos tridimensionais possíveis, chamados diastereômeros. Durante décadas, os químicos dependeram de modelos simples—Felkin–Anh, polar Felkin–Anh, Cram e modelos de quelatação—para prever qual face um reagente preferirá. Em compostos carbonílicos α‑oxi, onde esse substituinte vizinho contém oxigênio (como um éter ou éster), o oxigênio costuma agir como uma garra que se liga a reagentes metálicos. Essa “quelatação” prende a molécula em uma conformação e quase sempre leva a produtos chamados sin, nos quais os grupos alcoóis recém‑formados ficam do mesmo lado da cadeia carbônica.
O problema de longa data com vizinhos oxigenados
Embora a via de quelatação seja muito útil, ela também é limitadora: ela favorece fortemente reações rumo a produtos sin e torna muito difícil obter o arranjo oposto, anti, em que os dois grupos alcoóis apontam para lados opostos. Para aldeídos α‑oxi—moléculas em que o carbono carbonílico está ligado a pelo menos um hidrogênio—algumas estratégias engenhosas usando reagentes especiais de silício e ácidos de Lewis cuidadosamente escolhidos conseguiram entregar produtos anti. Mas para cetonas α‑oxi, que são menos reativas e mais comuns em alvos complexos, o desafio é maior. Nucleófilos mais fortes tendem a ser mais ácidos de Lewis, o que por sua vez incentiva exatamente a quelatação que o químico quer evitar. Assim, equilibrar “reativo o suficiente” com “não excessivamente atraente” para o oxigênio tem sido um problema central não resolvido.
Um reagente em forma de gaiola que quebra a regra
Os autores introduzem uma nova família de reagentes chamados allylatranes, construídos em torno de elementos do grupo 14—silício, germânio e estanho—mantidos em uma estrutura rígida, em forma de gaiola. Nesses compostos, um átomo de nitrogênio interno alcança através da gaiola para se ligar ao átomo central, criando um centro fortemente coordenado, quase encapsulado. Esse desenho tem dois efeitos cruciais. Primeiro, aumenta a nucleofilicidade do fragmento allyl ligado, tornando‑o ansioso para formar uma nova ligação carbono–carbono. Segundo, doma a acidez de Lewis do átomo central, fazendo com que ele tenha muito menos tendência a se ligar fortemente aos oxigênios do substrato. Cálculos quântico‑químicos e dados de ressonância magnética nuclear confirmam que a carga fica localizada no fragmento allyl enquanto a comunicação eletrônica com o centro de silício é reduzida, explicando como o reagente pode ser ao mesmo tempo potente e relutante em quelar.
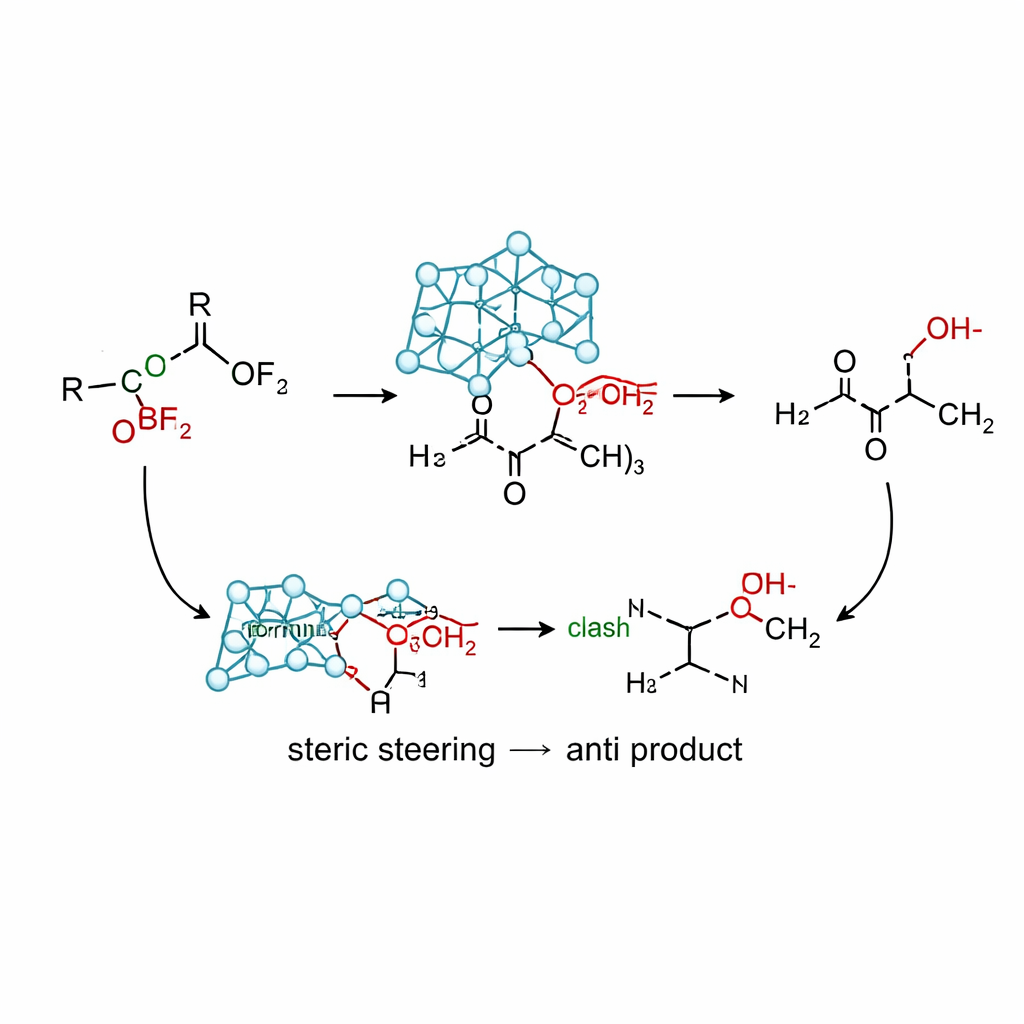
Como a nova reação funciona na prática
Usando a versão de silício desse reagente, o allylsilatrane, juntamente com um ácido de Lewis suave (trifluoreto de boro), a equipe desenvolveu condições que fornecem altos rendimentos de álcoois anti‑homoalílicos a partir de uma ampla gama de cetonas α‑oxi. Experimentos de referência mostram que muitas fontes tradicionais de allyl—baseadas em estanho, índio, magnésio, lítio e silanos simples—ou favorecem o produto sin, dão misturas ou se decompõem. Em contraste, o allylsilatrane rotineiramente entrega razões anti/sin acima de 95:5 em substratos contendo metoxi, isopropoxi, fenoxi, acetoxi, silyloxi e aminoxi, bem como diversos anéis aromáticos e cetonas cíclicas. Cálculos sugerem uma via não‑quelante na qual a volumosa estrutura atrane orienta a aproximação do grupo allyl em uma conformação semelhante ao modelo de Cram: o substituinte oxigênio fica oposto ao carbonila enquanto a repulsão estérica entre a gaiola e anéis fenólicos próximos favorece a trajetória que leva ao produto anti.
Implicações para síntese de fármacos e produtos naturais
O método também funciona para sistemas cíclicos mais rígidos, onde a massa do allylsilatrane incentiva o ataque de posições menos obstruídas, e para derivados especializados que transferem grupos allyl substituídos com seletividade anti igualmente alta. Como os anti‑1,2‑dióis com um fragmento homoalílico são motivos comuns em moléculas biologicamente ativas, incluindo candidatos a moduladores enzimáticos, essa transformação oferece aos químicos uma via confiável para acessar variantes estruturais que antes exigiam sequências multietapa ou eram simplesmente pouco práticas. É importante notar que os mesmos substratos podem ser direcionados para dar produtos sin ou anti alternando entre um sistema quelante à base de estanho e o novo sistema não‑quelante silatrano, concedendo controle preciso sobre a forma molecular.
O que isso significa em termos simples
Essencialmente, os pesquisadores construíram uma ferramenta inteligente de entrega do grupo allyl que atinge o carbono alvo pelo lado “menos favorecido” sem ficar presa por átomos de oxigênio vizinhos. Ao projetar cuidadosamente uma gaiola ao redor do silício, eles desacoplaram força e aderência: o reagente é forte o bastante para formar uma nova ligação, mas não tão aderente a ponto de agarrar átomos ao redor e arruinar a geometria desejada. Para não especialistas, isso significa que os químicos agora têm um controle muito melhor sobre a escultura de estruturas moleculares tridimensionais que sustentam muitos medicamentos e produtos naturais, ampliando o espaço de projeto para futuros fármacos e moléculas sintéticas complexas.
Citação: Tsutsui, Y., Shiga, K., Konishi, A. et al. Non-chelation control in allylations of α-oxy ketones using group-14 allylatranes. Nat Commun 17, 2019 (2026). https://doi.org/10.1038/s41467-026-69732-2
Palavras-chave: alquilação estereosseletiva, cetonas alfa‑oxi, allylsilatrano, controle não‑quelante, álcoois homoalílicos