Clear Sky Science · pt
A região N-Myc MB0–MBI interage de forma específica e dinâmica com o lobo N da quinase Aurora A
Por que isso importa para o tratamento do câncer
Muitos cânceres infantis agressivos dependem de uma proteína chamada N-Myc para manter as células tumorais proliferando. A própria N-Myc é difícil de bloquear com fármacos porque se comporta mais como um pedaço de espaguete flexível do que como uma fechadura rígida na qual uma chave pode se encaixar. Este estudo revela, com detalhes sem precedentes, como a N-Myc se agarra a outra proteína, a enzima quinase Aurora A (AurA), para aumentar sua atividade e ajudar as células cancerosas a sobreviver. Ao mapear essa parceria, os pesquisadores descobrem uma via realista para interrompê-la com pequenas moléculas.
Um causador de problemas flexível encontra um parceiro sólido
A N-Myc pertence à família MYC de interruptores mestres que controlam crescimento celular, metabolismo e divisão. Quando superproduzidos, esses interruptores se tornam potentes motores do câncer, especialmente em tumores do sistema nervoso, como o neuroblastoma de alto risco em crianças. Ao contrário de muitas enzimas ou receptores, a N-Myc não se dobra em uma forma 3D fixa por conta própria; é uma proteína “intrinsecamente desordenada” que se contorce e remodela constantemente. Essa flexibilidade a torna adaptável, mas também notoriamente difícil de atingir com drogas. A AurA, em contraste, é uma enzima bem estruturada que ajuda a organizar a divisão celular. Trabalhos anteriores mostraram que a AurA ajuda a estabilizar a N-Myc em células tumorais e que as duas proteínas interagem fisicamente, mas a natureza exata e a importância dos pontos de contato permaneciam pouco claras.
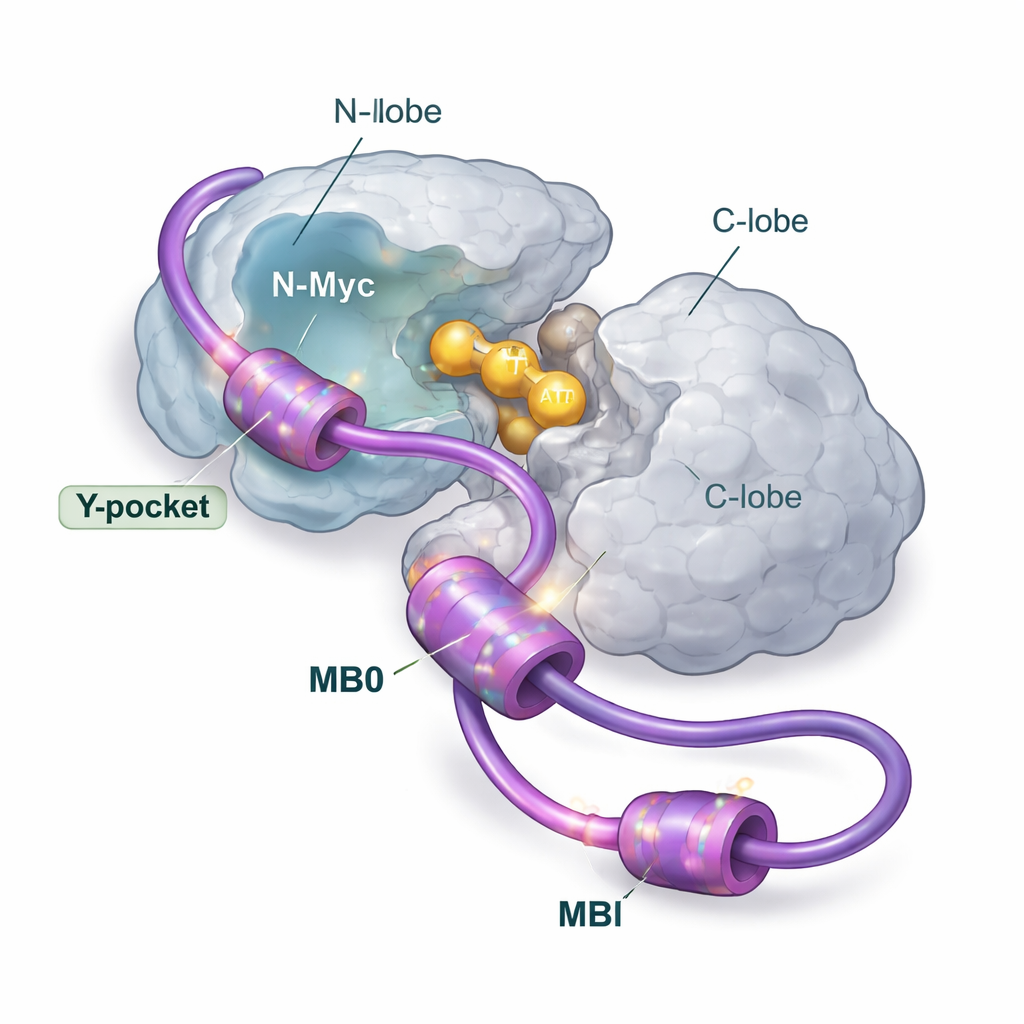
Múltiplos pontos de apreensão, um principal ponto de aterrissagem
Usando um amplo conjunto de métodos estruturais e biofísicos, incluindo ressonância magnética nuclear, espalhamento de raios X, espectrometria de massa, calorimetria e modelagem computacional, os autores dissecam como a N-Myc e a AurA se reúnem em solução. Eles se concentraram na extremidade frontal da N-Myc, que contém duas regiões conservadas chamadas MB0 e MBI. Esses trechos curtos são ricos em blocos aromáticos (como fenilalanina, tirosina e triptofano) que tendem a aderir a bolsões gordurosos em proteínas parceiras. A equipe mostra que a N-Myc se liga à AurA principalmente como um par 1:1, com MB0 e MBI atuando como as zonas de contato primárias. Outro trecho da N-Myc que havia chamado atenção em estruturas cristalinas anteriores acaba desempenhando apenas um papel menor quando a região completa MB0–MBI está presente.
Um aperto dinâmico que liga a enzima
Em vez de encaixar-se em uma única pose rígida, a N-Myc permanece em grande parte desordenada quando ligada à AurA. Os dados apontam para um complexo “fuzzy”: vários segmentos da N-Myc se alternam ao contatar diferentes manchas no lobo N da AurA, especialmente um sulco conhecido como Y-pocket e um loop próximo que liga sinais ao sítio ativo. Apesar dessa frouxidão, o efeito é claro — a ligação de MB0 e MBI estabiliza o lobo N da AurA e aumenta sua atividade quinase, ou seja, sua eficiência em transferir grupos fosfato para seus alvos. Quando os pesquisadores substituíram sistematicamente resíduos aromáticos-chave em MB0 e MBI por alanina, o complexo N-Myc–AurA enfraqueceu, a enzima ficou menos estabilizada e sua atividade caiu. Isso mostra que “âncoras” aromáticas específicas na cadeia por outro lado flexível da N-Myc são essenciais para ativar a AurA.
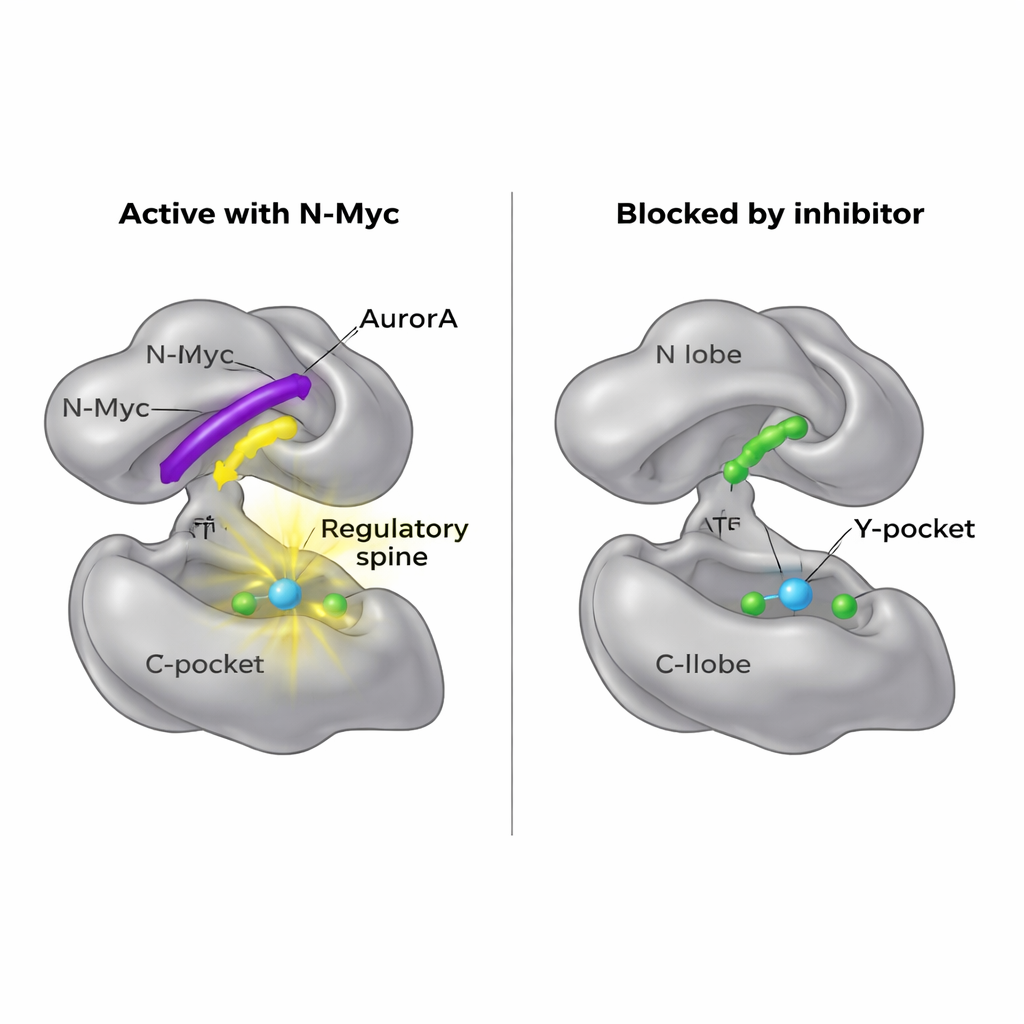
Abrindo uma nova entrada para drogas
Como a própria N-Myc é difícil de atingir com fármacos, os pesquisadores perguntaram se poderiam bloquear em vez disso seu sítio de ancoragem na AurA. Seus mapas estruturais revelaram que MB0 e MBI ocupam a mesma região geral do lobo N que outra proteína parceira, TPX2, usa para ativar a AurA. Uma pequena molécula chamada AurkinA já é conhecida por se alojar no Y-pocket e deslocar a TPX2. Em experimentos de ligação, a AurkinA competiu efetivamente com a N-Myc pelo lobo N da AurA também, impedindo que os fragmentos N-Myc1–69 e N-Myc1–100 se anexassem. Esse resultado demonstra que a superfície do lobo N, e especialmente o Y-pocket, é um ponto quente “druggable” que controla não apenas reguladores clássicos como a TPX2, mas também oncoproteínas desordenadas como a N-Myc.
O que isso significa para terapias futuras
Este trabalho refraseia a parceria N-Myc–AurA como um abraço dinâmico de múltiplos contatos centrado no lobo N da AurA, em vez de um único sítio de ligação rígido. Para não especialistas, a mensagem-chave é que mesmo uma proteína cancerígena sem forma como a N-Myc pode ser enfrentada indiretamente ao mirar uma placa de ancoragem sólida na sua enzima parceira. Ao mostrar que compostos já existentes que se ligam ao lobo N podem deslocar a N-Myc da AurA, o estudo abre um caminho claro rumo a drogas que interrompam seletivamente essa interação. Tais agentes poderiam enfraquecer um suporte crítico para a N-Myc em tumores infantis de alto risco e, com desenvolvimento adicional, oferecer uma nova via de tratamento para cânceres há muito considerados “indrugáveis”.
Citação: Hultman, J., Morad, V., Tanner, E. et al. The N-Myc MB0-MBI region interacts specifically and dynamically with the N-lobe of Aurora kinase A. Nat Commun 17, 2016 (2026). https://doi.org/10.1038/s41467-026-69725-1
Palavras-chave: N-Myc, quinase Aurora A, proteínas intrinsecamente desordenadas, neuroblastoma, inibidores de interação proteína–proteína