Clear Sky Science · pt
Um atlas espacialmente resolvido de glioblastoma humano revela padrões celulares e moleculares distintos de nichos anatômicos
Por que este mapa do câncer cerebral é importante
O glioblastoma é um dos cânceres cerebrais mais letais, em parte porque cada tumor é um mosaico de diferentes tipos celulares e microambientes. Exames padrão e testes de laboratório costumam enxergar o tumor como uma massa única. Este estudo constrói um “atlas” de alta resolução que mostra onde cada tipo celular principal se localiza dentro de glioblastomas humanos, como essas células se agrupam em bairros distintos e como alguns desses bairros podem ajudar a impulsionar o crescimento tumoral e reduzir a sobrevida dos pacientes.
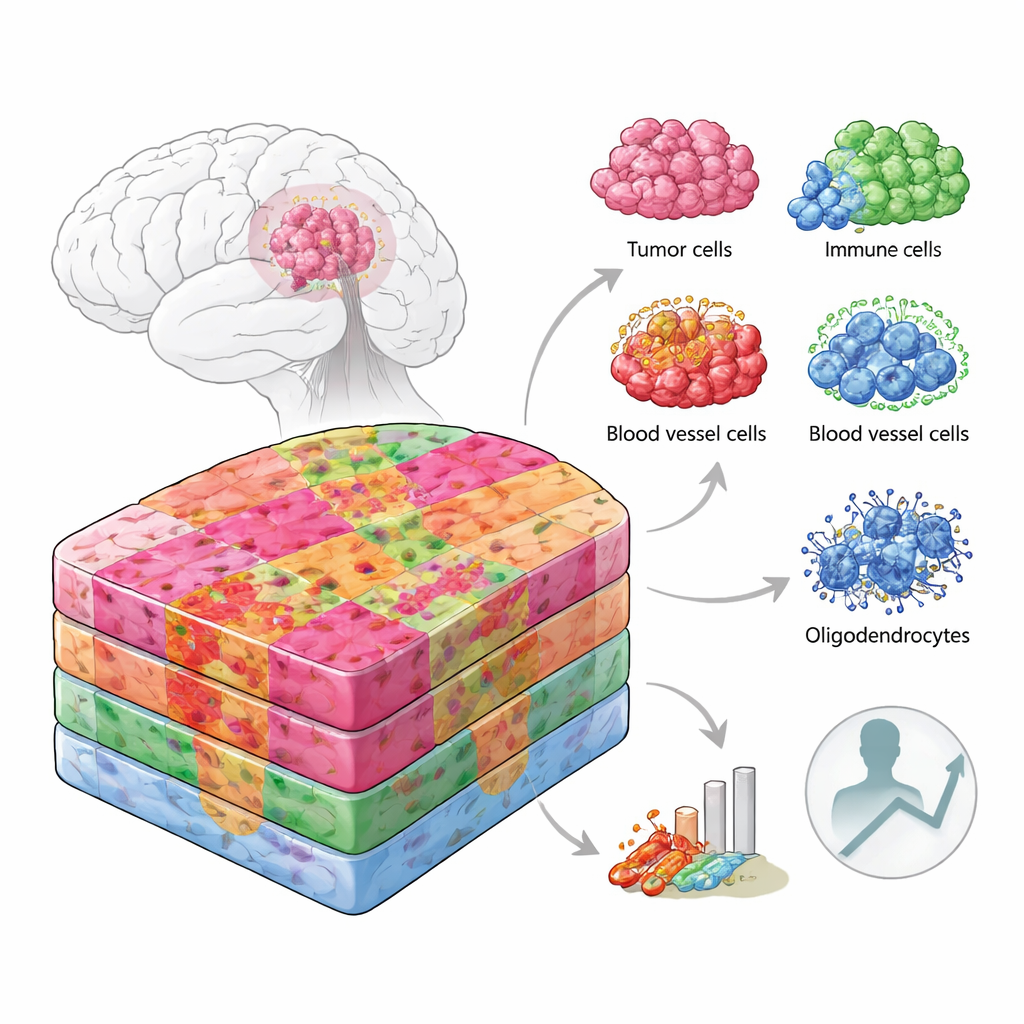
Olhando para tumores como mapas de cidades
Em vez de tratar uma lâmina tumoral como uniforme, os pesquisadores a abordaram como um mapa de cidade, onde cada distrito tem sua própria configuração e habitantes. Eles combinaram várias técnicas de ponta que leem a atividade gênica em milhares de pequenos pontos ao longo do tecido tumoral e casaram esses dados com informações de células únicas e medições de proteínas. Importante, isso foi feito não só em amostras frescas congeladas da sala de cirurgia, mas também em tecido hospitalar rotineiramente arquivado em parafina, que é o que a maioria dos laboratórios de patologia realmente guarda. No total, analisaram mais de 100.000 regiões espacialmente codificadas e mais de 220.000 células individuais de pacientes de idades e antecedentes genéticos variados, cobrindo tanto o núcleo denso do tumor quanto suas bordas mais difusas.
Bairros ocultos dentro do glioblastoma
Ao sobrepor a atividade gênica em imagens de microscópio de alta ampliação, a equipe dividiu cada tumor em “nichos” anatômicos, como a borda de invasão onde as células cancerosas infiltram o cérebro normal, as zonas centrais densas, áreas ricas em vasos sanguíneos e regiões ao redor de tecido morto ou com falta de oxigênio. Cada nicho revelou abrigar sua própria mistura de tipos celulares. A borda tumoral no córtex cinzento era rica em neurônios e células de suporte típicas, enquanto a borda na substância branca continha muitos oligodendrócitos, as células que normalmente isolam as fibras nervosas. Certos nichos vasculares estavam repletos de células especializadas dos vasos e células de suporte, enquanto outros eram dominados por células imunes e tecido tipo cicatriz. Zonas hipóxicas próximas a tecido necrosado continham majoritariamente células tumorais agressivas, de tipo mesenquimal, e macrófagos, com bem menos diversidade celular.
Um papel surpreendente para células de suporte
Uma das descobertas mais marcantes envolveu os oligodendrócitos, geralmente vistos como “isolantes” silenciosos no cérebro. O atlas revelou quatro estados distintos de oligodendrócitos, incluindo um tipo antes subestimado que apareceu quase exclusivamente nos núcleos dos glioblastomas. Essas células haviam perdido muitos de seus genes relacionados à mielina e, em vez disso, ativaram genes ligados à inflamação e ao estresse, assemelhando‑se a oligodendrócitos associados a doenças observados em esclerose múltipla e outros transtornos cerebrais. Espacialmente, essa população oligodendrocitária com perfil imune se agrupou em um “nicho imune‑glial” ao lado de microglia ativada, macrófagos, células vasculares anormais e células tumorais de tipo mesenquimal, mas notavelmente não nas regiões mais desprovidas de oxigênio.
Ligando padrões microscópicos ao desfecho dos pacientes
Os autores então investigaram se os programas gênicos que definem esses estados de oligodendrócitos aparecem em grandes coleções de amostras tumorais vinculadas a registros clínicos. Em dois coortes independentes de glioma, uma assinatura de oligodendrócitos convencionais produtores de mielina associou‑se a melhor sobrevida, mesmo após ajustar por idade e marcadores genéticos de risco importantes. Em contraste, a assinatura de oligodendrócitos ativados imune correlacionou‑se com pior sobrevida e foi mais proeminente em tumores agressivos e resistentes ao tratamento, especialmente naqueles que recidivaram após terapia e não apresentavam uma alteração de metilação ligada à reparação do DNA comum. Isso sugere que a reprogramação dos oligodendrócitos dentro do tumor e sua localização relativa a células tumorais e imunes pode influenciar a resposta ao tratamento e a probabilidade de recidiva.
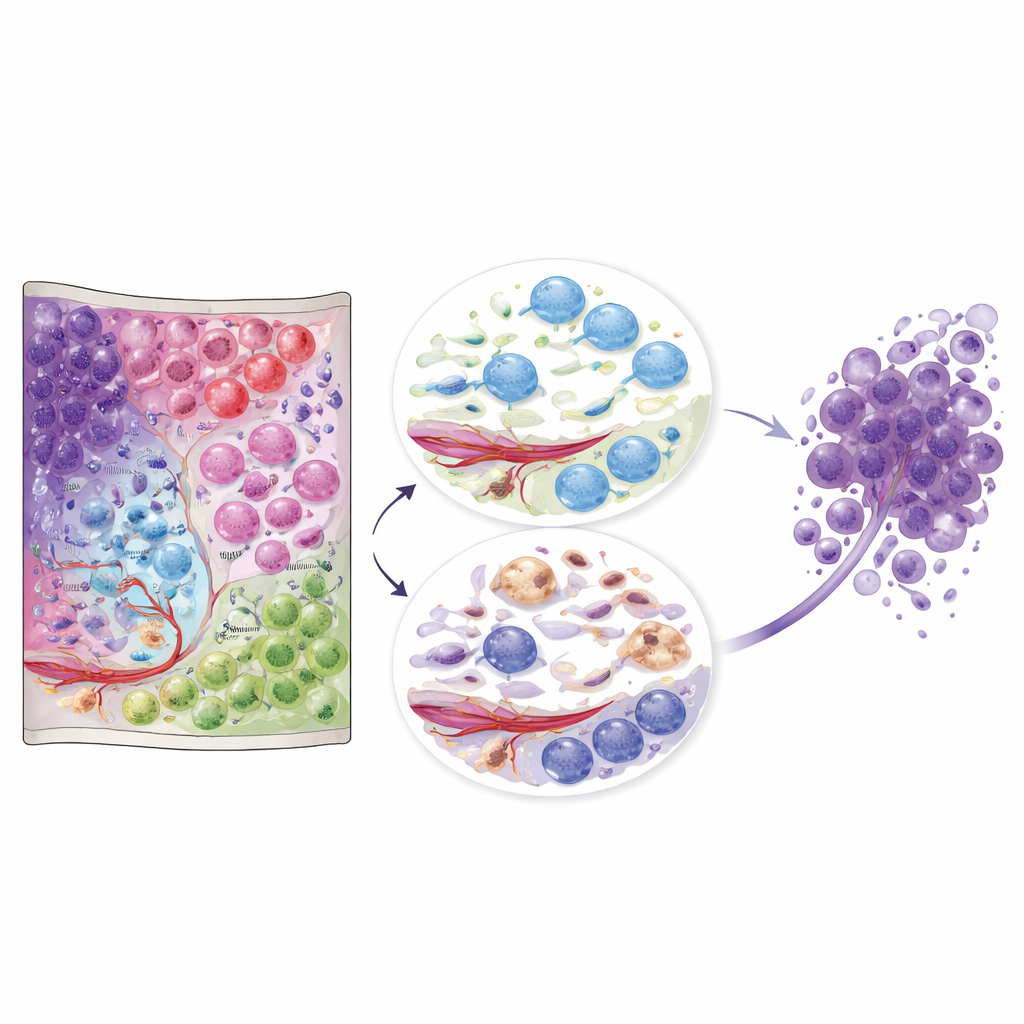
O que este atlas significa para o cuidado futuro
Juntos, esses dados transformam o glioblastoma de uma massa borrada em uma paisagem detalhada de comunidades celulares interagentes. Para não especialistas, a mensagem chave é que localização e vizinhança importam: os mesmos tipos celulares amplos comportam‑se de maneira muito diferente dependendo do nicho que ocupam. O atlas publicamente disponível oferece uma referência que outros pesquisadores e clínicos podem usar para situar suas próprias amostras nesse contexto espacial. A longo prazo, terapias podem ser projetadas não apenas para matar células tumorais, mas para desorganizar nichos nocivos — como regiões de cicatriz imune ou bolsões de oligodendrócitos ativados pelo sistema imune — que parecem favorecer a sobrevivência tumoral e a recidiva.
Citação: Sonpatki, P., Park, H.J., Xing, Y.L. et al. A spatially resolved human glioblastoma atlas reveals distinct cellular and molecular patterns of anatomical niches. Nat Commun 17, 2951 (2026). https://doi.org/10.1038/s41467-026-69716-2
Palavras-chave: glioblastoma, transcriptômica espacial, microambiente tumoral, oligodendrócitos, atlas do câncer cerebral