Clear Sky Science · pt
Spatial perturb-seq: genômica funcional de célula única dentro da arquitetura tecidual intacta
Ver os genes em ação em circuitos cerebrais vivos
Muitas doenças cerebrais, da doença de Alzheimer ao mal de Parkinson, estão associadas a genes de risco, mas ainda sabemos pouco sobre como esses genes afetam células individuais dentro do cérebro vivo. Este estudo apresenta uma forma poderosa de observar o que acontece quando genes específicos são desligados em células únicas, enquanto essas células permanecem em seus bairros naturais dentro do tecido cerebral. A abordagem, chamada Spatial Perturb-Seq, ajuda a conectar o risco genético a comportamentos celulares perturbados e à comunicação entre células no cérebro intacto.
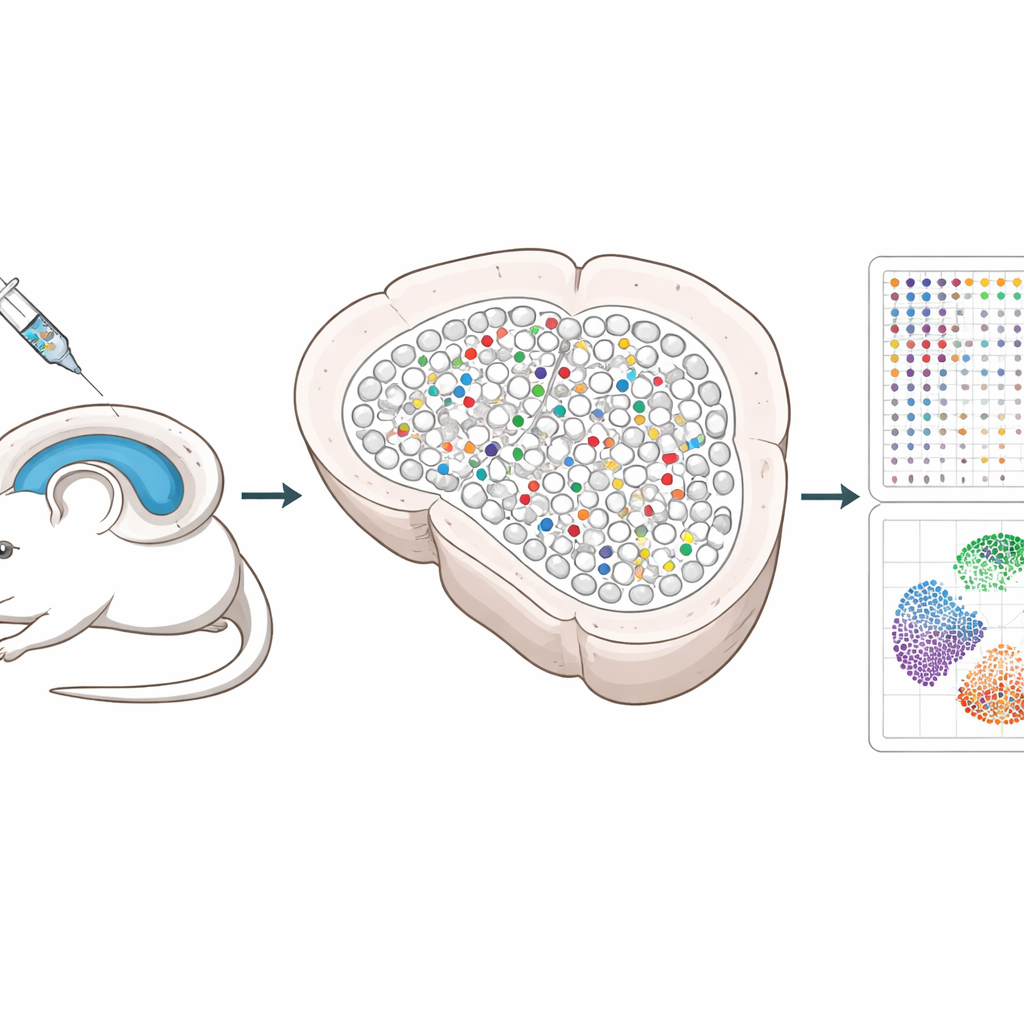
Uma nova maneira de testar muitos genes ao mesmo tempo
Os pesquisadores construíram um sistema que usa ferramentas de edição genética CRISPR entregues por vírus inofensivos ao hipocampo, uma região cerebral importante para a memória. Cada vírus carrega três guias que desativam um gene escolhido, junto com um “código de barras” de DNA único e um marcador fluorescente para que as células editadas possam ser localizadas depois. Ao misturar esses vírus e injetá-los em baixa dose, apenas uma pequena e dispersa fração de células é editada, e a maioria dos vizinhos permanece intacta. Esse padrão esparso permite aos cientistas separar as mudanças que ocorrem dentro das células editadas daquelas que acontecem nas células saudáveis próximas.
Preservando o mapa do cérebro
Os métodos tradicionais de célula única exigem que os tecidos sejam dissociados, o que destrói as posições precisas das células e pode até perder neurônios frágeis. Spatial Perturb-Seq, em vez disso, lê a atividade gênica diretamente em fatias finas do cérebro, de modo que a localização de cada célula é preservada. Usando uma tecnologia chamada Stereo-seq, a equipe capturou perfis completos de expressão gênica de mais de 200.000 células, ao mesmo tempo em que leu os códigos de barras CRISPR e registrou as coordenadas de cada célula no tecido. Em seguida, usaram algoritmos avançados baseados em imagem para contornar cada célula e ferramentas computacionais para identificar tipos celulares e bairros locais, com foco especial nos neurônios do hipocampo e seus contatos próximos.
Como células editadas influenciam seus vizinhos
Com o mapa tecidual em mãos, os cientistas compararam neurônios editados com neurônios não editados e, separadamente, com os vizinhos não editados que cercam cada célula editada. Isso lhes permitiu distinguir efeitos “celular-autônomos” (dentro da célula editada) de efeitos “não celular-autônomos” (no microambiente circundante). A inativação de 18 genes diferentes, muitos ligados ao risco de doenças neurodegenerativas, produziu padrões distintos de alterações gênicas dentro dos neurônios editados. Algumas edições, como as que afetaram o gene Cfap410, também desencadearam fortes mudanças na atividade gênica em células vizinhas, refletindo sinalização local e suporte alterados.
Pistas sobre vias de doenças neurodegenerativas
Vários genes forneceram insights especialmente intrigantes. A desativação de Lrrk2, um importante gene de risco para Parkinson, causou grandes alterações nos neurônios editados, incluindo níveis reduzidos de Bc1, uma molécula de RNA importante para ajustar a produção proteica nas sinapses. Ao mesmo tempo, células vizinhas mostraram expressão alterada de genes envolvidos na estrutura sináptica, transporte de proteínas e manejo de cálcio, sugerindo que problemas ligados a Lrrk2 reverberam pelos circuitos locais. A inativação de outro gene, Srf, perturbou uma rede de genes associada ao crescimento e à plasticidade neuronal, e enfraqueceu vias específicas de sinalização ligante–receptor entre neurônios, indicando comunicação célula-a-célula comprometida. Ao pontuar sistematicamente esses pares de sinalização, a equipe conseguiu identificar quais rotas de comunicação foram mais afetadas para cada gene.
Ferramentas flexíveis para mapear efeitos genéticos
Para demonstrar que o Spatial Perturb-Seq não está preso a uma única plataforma, os pesquisadores também o adaptaram a um sistema baseado em imagem chamado Xenium. Lá, painéis de sondas pré-desenhados e sondas de código de barras personalizadas lêem genes selecionados e códigos de barras diretamente no tecido. Embora essa abordagem direcionada cubra menos genes que o Stereo-seq de transcriptoma completo, os padrões de alteração gênica para edições-chave como Lrrk2 e Srf concordaram bem entre os dois métodos e com um grande atlas cerebral externo. Essa verificação cruzada apoia a robustez dos efeitos observados nos genes e nos bairros locais.
O que isso significa para a pesquisa em saúde cerebral
Em termos práticos, o Spatial Perturb-Seq permite que cientistas desliguem muitos genes diferentes em células cerebrais individuais e depois observem como essas células e seus vizinhos imediatos reagem, tudo isso enquanto o diagrama de conexões do tecido permanece intacto. Isso torna possível traçar como fatores de risco genético perturbam não apenas células isoladas, mas também as conversas entre elas, que são cruciais para o funcionamento saudável do cérebro. Com o tempo, à medida que o sequenciamento ficar mais barato e experimentos maiores forem realizados, essa abordagem poderá ajudar a revelar quais genes e circuitos locais são mais importantes em estágios iniciais de transtornos como Alzheimer, Parkinson e ELA, orientando estratégias de tratamento mais precisas.
Citação: Shen, K., Seow, W.Y., Keng, C.T. et al. Spatial perturb-seq: single-cell functional genomics within intact tissue architecture. Nat Commun 17, 3018 (2026). https://doi.org/10.1038/s41467-026-69677-6
Palavras-chave: genômica espacial, triagens CRISPR, sequenciamento de célula única, neurodegeneração, comunicação entre células