Clear Sky Science · pt
FLEXTAG: um sistema pequeno e autorrenovável de marcação de proteínas para imagens super-resolução multicoloridas resistentes ao desbotamento
Ver o invisível dentro das células
Muita da biologia moderna depende de fotografar as moléculas que mantêm nossas células vivas. Mas até os melhores microscópios ópticos enfrentam um problema simples: as marcas luminosas usadas para destacar proteínas desbotam rapidamente, e é difícil marcar diversos alvos ao mesmo tempo sem perturbar o funcionamento celular. Este trabalho apresenta o FLEXTAG, uma nova família de marcadores pequenos e renováveis que permanecem brilhantes por muito mais tempo, suportam múltiplas cores e funcionam com os microscópios mais potentes que os cientistas usam para ver a arquitetura interna das células.
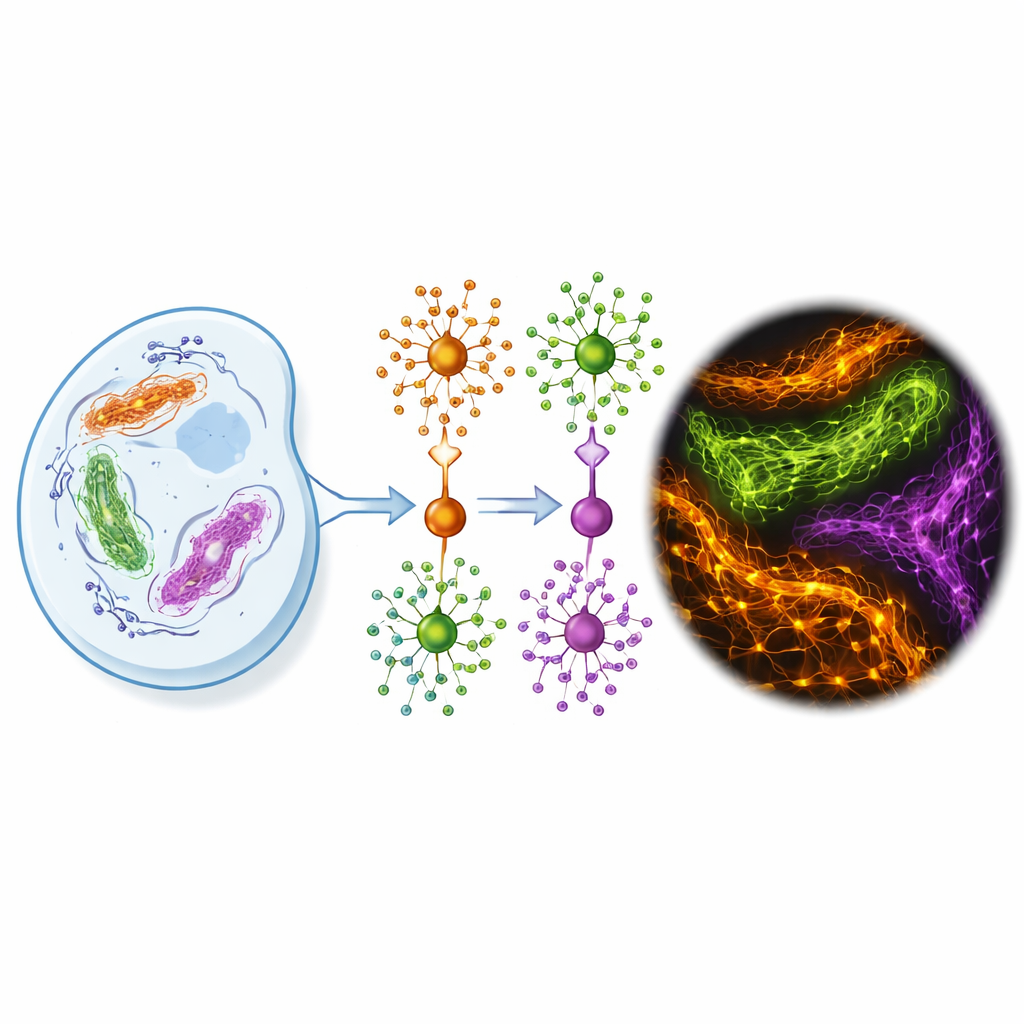
Por que fotos celulares mais nítidas são tão difíceis
Microscópios de fluorescência convencionais podem revelar estruturas com cerca de um quarto de micrômetro, o que ainda é muito maior do que a maioria das proteínas individuais. Métodos de super-resolução extraem mais detalhes, chegando a alguns nanômetros, mas somente se os marcadores fluorescentes se comportarem perfeitamente. Os marcadores de proteínas populares atualmente são ou anticorpos volumosos, proteínas fluorescentes pouco brilhantes, ou etiquetas químicas cujos corantes se desgastam rapidamente sob a luz intensa necessária para essas técnicas. Fixar células com produtos químicos para imagens detalhadas também pode unir proteínas de maneiras que impedem os corantes de alcançar seus alvos, e moléculas de corante soltas podem aderir de forma inespecífica, turvando a imagem com brilho de fundo.
Um novo tipo de etiqueta de proteína reabastecível
Os autores projetaram o FLEXTAG (abreviação de Fluorescent Labeling for Exchangeable, X-resilient Tagging in Advanced Generic Nanoscopy) para enfrentar essas limitações diretamente. FLEXTAG não é uma única etiqueta, mas um trio coordenado—FLEXTAG1, FLEXTAG2 e FLEXTAG3—cada um uma pequena proteína engenheirada (12–18 quilodaltons, aproximadamente metade do tamanho de etiquetas clássicas como GFP e bem menor que HaloTag). Cada FLEXTAG liga-se a um ligante de pequena molécula correspondente que carrega um corante orgânico brilhante. Crucialmente, essa ligação é reversível: moléculas corante–ligante entram e saem continuamente. Quando um fluoróforo é danificado pela luz, um novo vindo da solução circundante ocupa seu lugar, de modo que o sinal efetivamente se “autorenova” em vez de desvanecer continuamente.
Construindo três etiquetas compactas e confiáveis
Para criar FLEXTAG1–3, a equipe reaproveitou três scaffolds proteicos bem conhecidos da biologia celular e do desenho de fármacos, e então usou modelagem estrutural e ensaios baseados em imagem para remodelar seu comportamento. FLEXTAG1 deriva de uma proteína bromodomain que reconhece uma pequena molécula modificada; os autores introduziram mutações para evitar sua tendência a dimerizar e formar agregados, preservando, porém, forte afinidade pelo ligante. FLEXTAG2 vem da diidrofolato redutase bacteriana. Ao adicionar uma ponte dissulfeto estratégica e ajustar conectores flexíveis, eles estabilizaram a proteína e aumentaram dramaticamente a fração de etiquetas carregadas com corante em qualquer momento, mantendo a ligação reversível. FLEXTAG3 baseia-se em uma proteína humana FKBP usada em biologia química; aqui, a equipe equilibrou força de ligação e velocidade para que os corantes saiam rápido o suficiente para serem substituídos, mas ainda se liguem com força suficiente para produzir imagens brilhantes e evitar agregação excessiva.
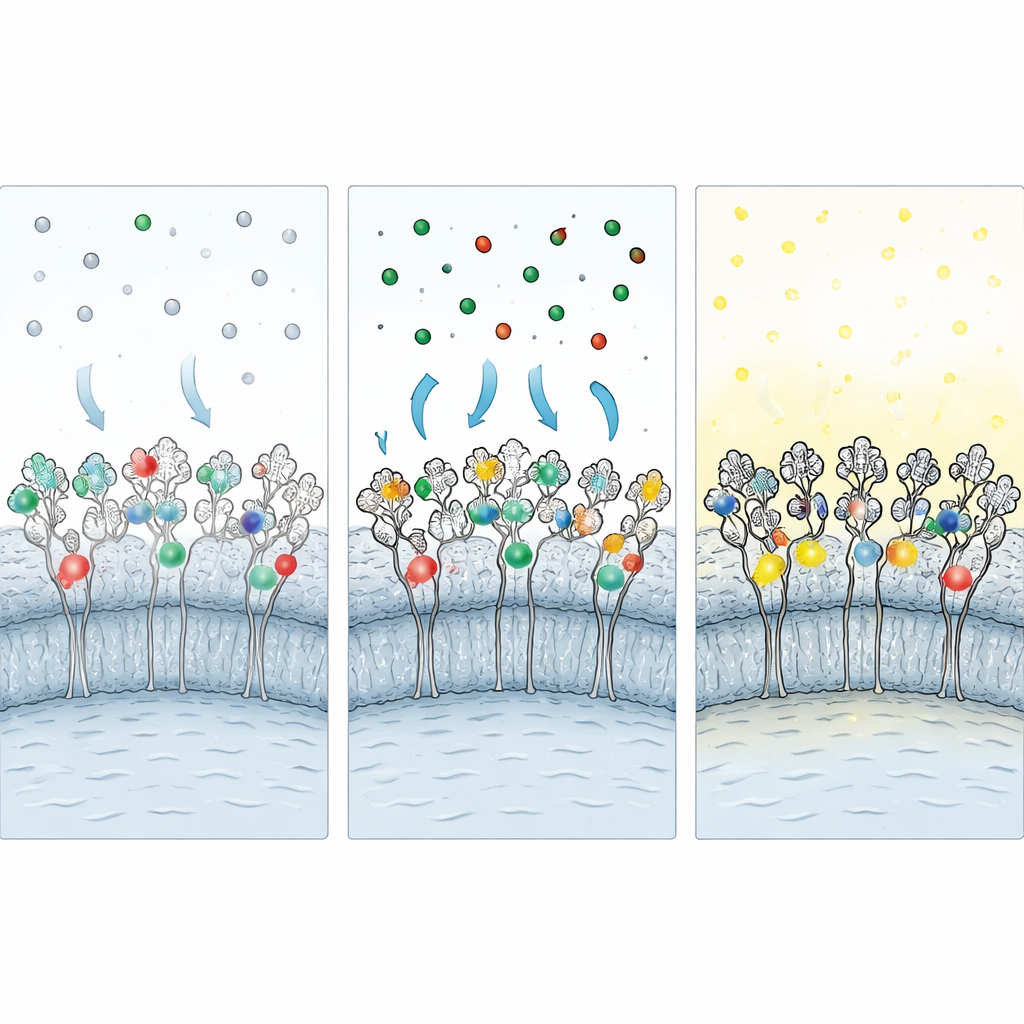
Protegendo etiquetas durante a fixação e reduzindo o brilho de fundo
Como muitos experimentos importantes exigem imagem de células fixadas, os pesquisadores desenvolveram uma estratégia de “fixação protetora”. Antes de adicionar fixadores aldeídos, eles saturam as células vivas com versões não marcadas de cada ligante, ocupando o bolso de ligação da etiqueta. Durante a fixação, esses ligantes protetores protegem aminoácidos vulneráveis de ligações cruzadas químicas. Após a fixação, os ligantes protetores são lavados e substituídos por ligantes fluorescentes, restaurando o acesso à etiqueta. Etapas adicionais—redução química para neutralizar grupos reativos remanescentes e um coquetel bloqueador contendo albumina, detergente e um sal caotrópico—reduzem ainda mais a ligação inespecífica e pegajosa de corantes livres. Em conjunto, essas medidas preservam cerca de 60–70% da marcação observada em células vivas ao mesmo tempo que melhoram acentuadamente a razão sinal/ruído.
Filmes mais nítidos e duradouros em muitos métodos
Com a estrutura FLEXTAG estabelecida, os autores a testaram nas principais famílias de microscopia de super-resolução. Em métodos de iluminação padronizada, como SIM e STED, os FLEXTAGs permitiram imagens multicoloridas de mitocôndrias, microtúbulos, retículo endoplasmático e actina com muito menos desbotamento do que etiquetas covalentes padrão; ao longo de dezenas de ciclos de imagem, o sinal de etiquetas convencionais caiu pela metade ou mais, enquanto os sinais FLEXTAG permaneceram quase constantes. Em métodos de molécula única, como PAINT e STORM, a troca rápida de ligantes on–off dos FLEXTAGs produziu fluxos ricos e estáveis de localizações que puderam ser convertidos em mapas tridimensionais multicoloridos de estruturas subcelulares, mesmo em células vivas por vários minutos. FLEXTAG2 mostrou cinéticas particularmente favoráveis para PAINT, enquanto FLEXTAG3 se destacou em filmes STORM de longa duração. Como as etiquetas são ortogonais entre si e compatíveis com uma ampla paleta de corantes, pesquisadores podem marcar várias proteínas ao mesmo tempo e então escolher o modo de imagem que melhor responda à sua pergunta sem mudar os constructos subjacentes.
O que isso significa para olhar dentro das células
FLEXTAG oferece uma espécie de conector universal e reabastecível entre proteínas e corantes brilhantes. Seu tamanho reduzido diminui o risco de que a etiqueta altere o destino ou a função da proteína, e seus corantes autorrenováveis ajudam a contornar o problema de longa data do fotobranqueamento em microscópios de alta potência. Ao combinar essas etiquetas com fixação protetora e química de supressão de fundo, os pesquisadores podem obter vistas mais limpas, duradouras e mais coloridas de como as proteínas estão organizadas e se movimentam dentro das células. Em termos práticos, isso significa mapas melhores da arquitetura celular, rastreamento mais confiável de interações moleculares ao longo do tempo e um conjunto de ferramentas versátil que deve beneficiar tanto a biologia celular básica quanto estudos translacionais que dependem de observar mudanças relacionadas a doenças na escala nanométrica.
Citação: Zhang, H., Yao, Y., Wang, X. et al. FLEXTAG: a small and self-renewable protein labeling system for anti-fading multi-color super-resolution imaging. Nat Commun 17, 2156 (2026). https://doi.org/10.1038/s41467-026-69658-9
Palavras-chave: microscopia de super-resolução, marcação com proteínas fluorescentes, imagens em células vivas, resistência ao fotobranqueamento, arquitetura celular