Clear Sky Science · pt
Upcycling eficiente do metanol para etilenoglicol e glicolaldeído via síntese divergente de acoplamento C−C
Transformando um Combustível Simples em Blocos de Construção Úteis
O metanol, um álcool simples que pode ser produzido a partir de dióxido de carbono, gás natural, carvão ou biomassa, já é um combustível e produto químico importante. Este estudo mostra como feixes de luz e nanomateriais cuidadosamente projetados podem transformar metanol em moléculas mais complexas e de maior valor—enquanto liberam gás hidrogênio como um vetor de energia limpa. O trabalho revela uma nova forma de direcionar um único material de partida para dois produtos úteis diferentes apenas mudando como átomos individuais de metal estão organizados na superfície de um catalisador minúsculo. 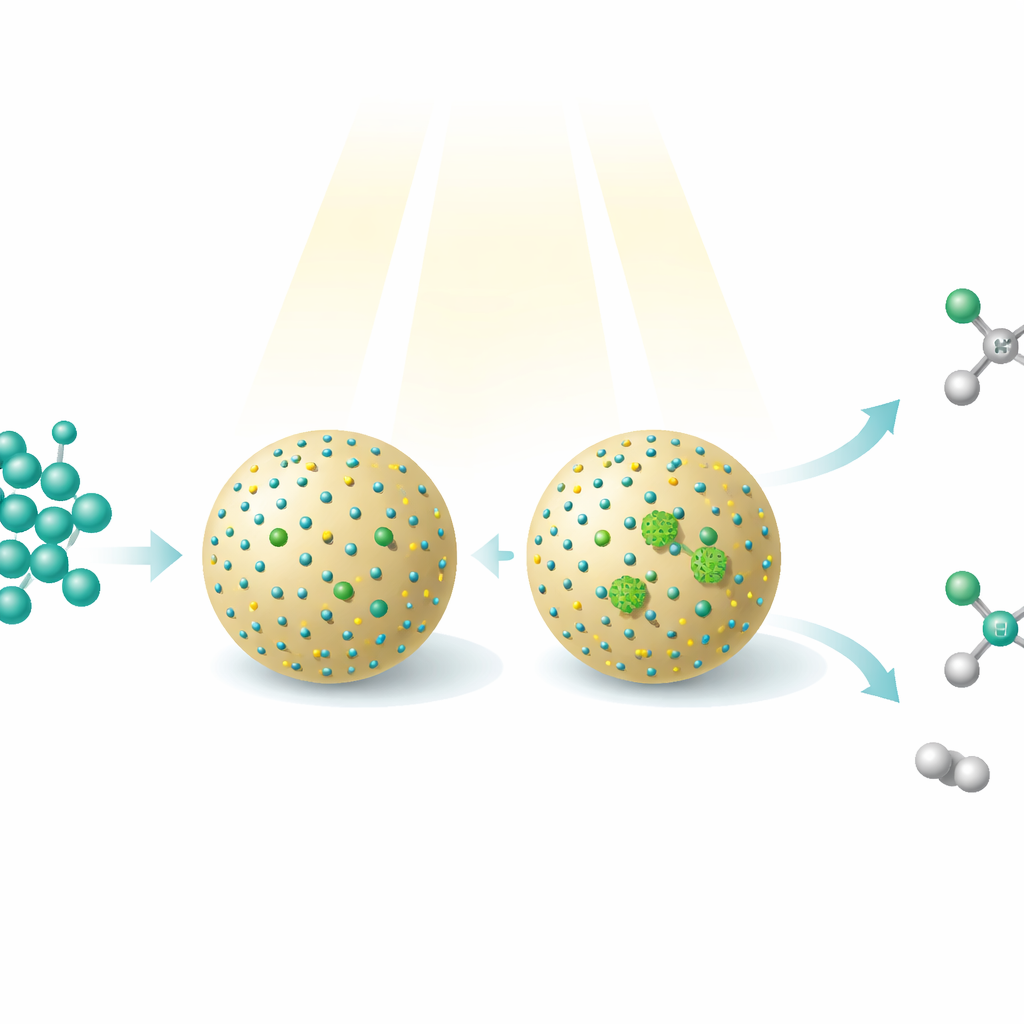
Por que Atualizar o Metanol é Importante
À medida que o mundo busca alternativas ao petróleo, o metanol emergiu como um líquido atraente que pode armazenar energia e carbono. No entanto, a maioria dos processos industriais que convertem metanol em moléculas maiores são ferramentas pouco precisas: exigem altas temperaturas, dependem de rotas fósseis e frequentemente geram muitos subprodutos indesejados. Os químicos desejam acoplar moléculas de metanol com alta precisão para poder produzir seletivamente apenas os compostos desejados. Fazer isso sob condições brandas, usando luz em vez de calor, facilitaria a integração da produção química com energia renovável.
Nanofolhas Ativadas por Luz Fazem o Trabalho
Os pesquisadores construíram um fotocatalisador—literalmente um catalisador acionado por luz—decorando pequenos pontos quânticos de sulfeto de cádmio sobre partículas esféricas de sílica. Esses pontos quânticos absorvem luz e geram elétrons e lacunas energéticas que podem arrancar átomos de hidrogênio do metanol, formando fragmentos altamente reativos. Átomos de níquel foram então depositados sobre os pontos quânticos de duas maneiras distintas. Em um material, o níquel existia principalmente como átomos únicos isolados; no outro, o níquel formava aglomerados muito pequenos de vários átomos. Embora a composição geral mal se alterasse, essa diferença sutil na organização do níquel alterou dramaticamente quais reações ocorriam na superfície.
Dois Projetos de Níquel, Dois Produtos Limpos
Quando o catalisador com átomos únicos de níquel foi exposto à luz em metanol, favoreceu o pareamento de dois fragmentos idênticos derivados do metanol, levando principalmente ao etilenoglicol—um diol de dois carbonos amplamente usado em anticongelantes e plásticos. Essa via atingiu cerca de 90% de seletividade, o que significa que quase todo o metanol convertido terminou como esse único produto, enquanto gás hidrogênio foi produzido em quantidades correspondentes a partir dos hidrogênios removidos. Por outro lado, o catalisador com aglomerados de níquel canalizou os mesmos fragmentos de metanol por um caminho diferente. Aqui, uma porção do metanol foi oxidada adicionalmente formando um intermediário de curta duração similar ao formaldeído, que então se combinou com outro fragmento para formar glicolaldeído, outro composto de dois carbonos com muitas aplicações em produtos finos e potencialmente em processos bio-based. Essa via entregou glicolaldeído com 96% de seletividade, novamente acompanhado de hidrogênio. O suporte de sílica ajudou os pontos quânticos a colherem a luz de forma mais eficiente e tornou as partículas mais robustas ao longo de muitos ciclos de uso. 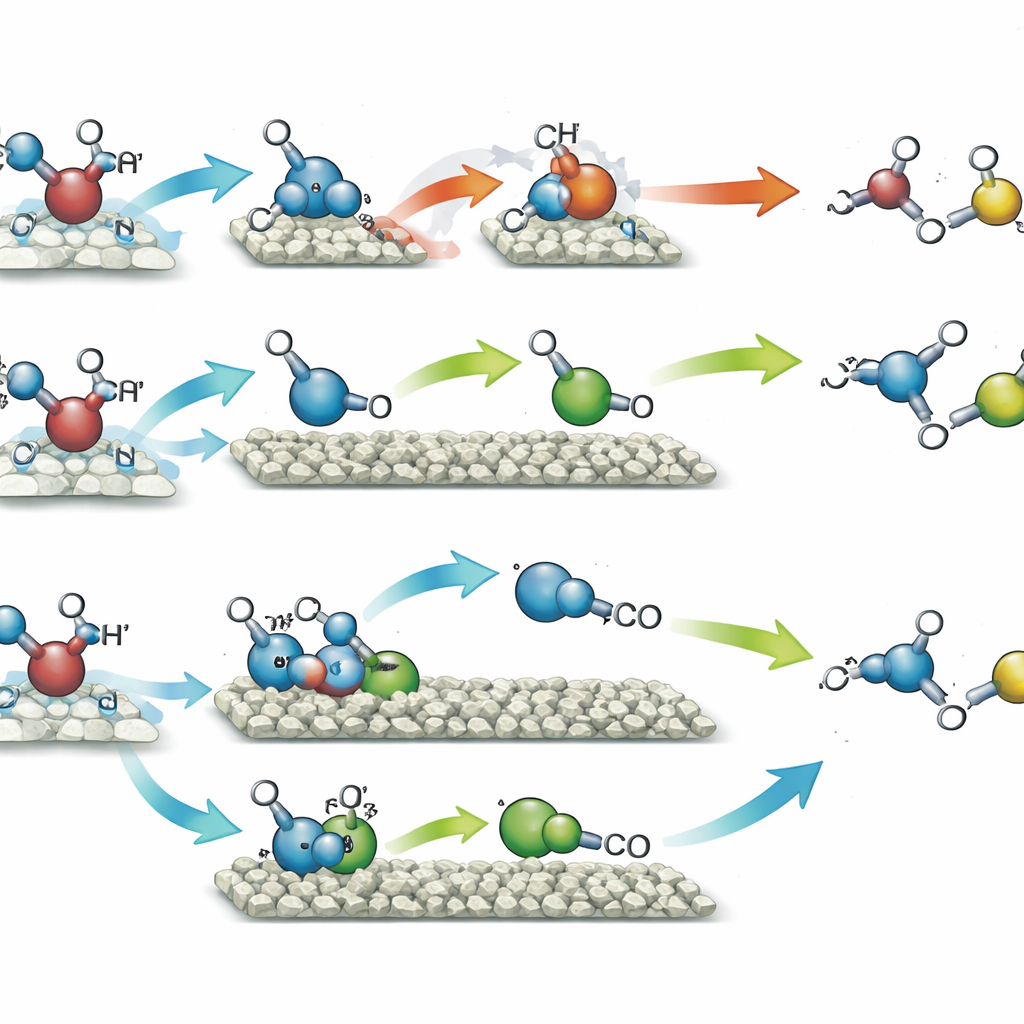
Olhando Por Trás do Capô da Reação
Para entender por que as duas arrumações de níquel se comportaram tão diferente, a equipe combinou um conjunto de medições avançadas com simulações por computador. Experimentos de ressonância paramagnética eletrônica mostraram que ambos os catalisadores geraram radicais derivados do metanol sob luz, mas o catalisador com aglomerados também promoveu a quebra da ligação oxigênio–hidrogênio, levando a fragmentos reacionais mais diversos e ao intermediário de formaldeído. Testes resolvidos no tempo confirmaram que esse intermediário aumentava e depois diminuía em concentração conforme era consumido para formar glicolaldeído. Cálculos quântico-químicos mapearam os custos energéticos de cada pequeno passo. Em átomos únicos de níquel, o acoplamento direto de dois radicais idênticos para formar etilenoglicol foi a rota mais fácil. Em aglomerados de níquel, esse mesmo acoplamento prendia demais o produto, dificultando sua liberação, enquanto a via que primeiro formava o intermediário assimétrico e depois o glicolaldeído tornava-se energeticamente preferida.
Uma Nova Alavanca para uma Produção Química Mais Limpa
Em termos práticos, este trabalho mostra que “onde” cada átomo de níquel se situa em uma superfície na escala nanométrica pode decidir “em que” molécula o metanol se transforma quando iluminado. Ao alternar entre átomos únicos e pequenos aglomerados de níquel, os pesquisadores podem inverter o produto principal de etilenoglicol para glicolaldeído, ambos produzidos de forma eficiente e limpa junto com combustível de hidrogênio. Essa estratégia de arquitetar catalisadores átomo por átomo oferece uma rota promissora para atualizar insumos simples e renováveis como o metanol em uma gama de produtos químicos úteis sem depender de petróleo, condições severas ou reações secundárias desperdiçadoras.
Citação: Qi, MY., Tan, CL., Tang, ZR. et al. Efficient methanol upcycling to ethylene glycol and glycolaldehyde via divergent C−C coupling synthesis. Nat Commun 17, 2835 (2026). https://doi.org/10.1038/s41467-026-69656-x
Palavras-chave: upcycling de metanol, fotocatálise, átomos únicos de níquel, etilenoglicol, glicolaldeído