Clear Sky Science · pt
Assinaturas de inclusão de éxons permitem estimar com precisão a atividade de fatores de splicing
Lendo as Marcas Ocultas de Edição da Célula
Cada célula do nosso corpo edita constantemente suas mensagens de RNA antes de transformá‑las em proteínas. Essa edição, chamada splicing, ajuda a decidir se uma célula permanece saudável ou se transforma em cancerosa. O estudo por trás deste artigo mostra que, ao examinar com atenção quais trechos de RNA são mantidos ou ignorados — chamadas assinaturas de inclusão de éxons — os cientistas podem inferir com precisão a atividade dos "editores" moleculares que controlam o splicing, mesmo em doenças complexas como o câncer.
Como as Células Cortam e Colam Suas Mensagens
Os genes não são lidos em um trecho contínuo. Em vez disso, as células removem segmentos não codificantes e unem as partes codificantes, conhecidas como éxons, para construir a mensagem final de RNA. Proteínas especializadas chamadas fatores de splicing guiam esse processo de cortar e colar, decidindo quais éxons são incluídos. Seu comportamento é influenciado por várias camadas de regulação: quanto de seu próprio RNA e proteína é produzido, como são modificados quimicamente, onde se localizam dentro da célula e como interagem com outras proteínas. Como tantas alavancas podem alterar o comportamento dos fatores de splicing, medir apenas um tipo de dado — por exemplo, expressão gênica — frequentemente não revela o que esses fatores estão realmente fazendo.
Transformando Padrões de Éxons em Medidas de Atividade
Inspirados por trabalhos anteriores sobre fatores de transcrição, os autores propuseram uma estratégia diferente: em vez de tentar medir fatores de splicing diretamente, ler sua atividade a partir de seus efeitos. Quando um fator de splicing muda, a inclusão de seus éxons-alvo varia em padrões reconhecíveis. A equipe compilou centenas de experimentos nos quais fatores de splicing individuais foram silenciados, nocauteados ou superexpressos, e usou esses dados para construir "redes empíricas" ligando cada fator aos éxons que ele afeta claramente. Em seguida, adaptaram uma estrutura computacional chamada VIPER para ler uma nova assinatura de inclusão de éxons e atribuir uma pontuação de quão ativo cada fator de splicing deve estar para explicar o padrão observado.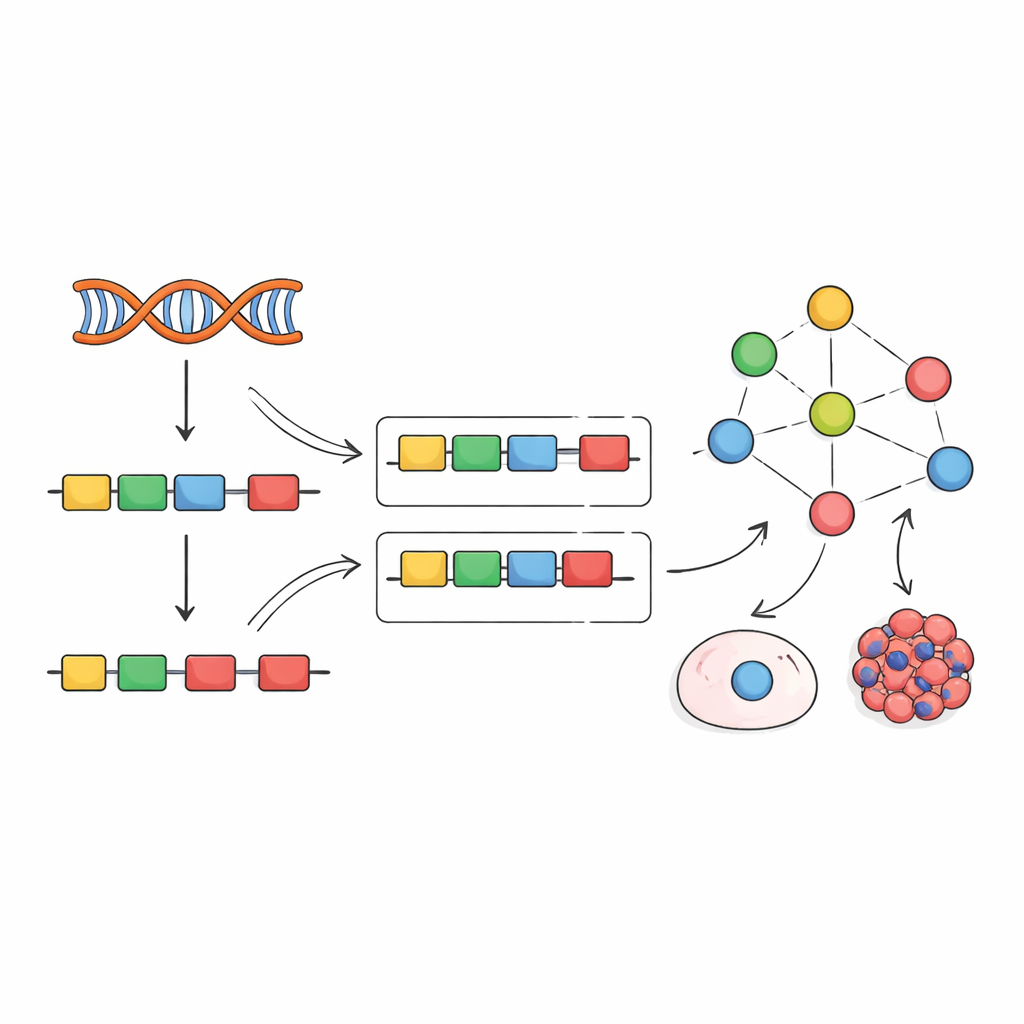
Testando o Método em Perturbações do Mundo Real
Para verificar se essa abordagem funciona, os pesquisadores compararam várias formas de construir redes e calcular pontuações de atividade. Redes empíricas derivadas diretamente de experimentos de perturbação, combinadas com a análise de enriquecimento do VIPER, superaram claramente alternativas baseadas apenas em inferência estatística. O método identificou corretamente o fator de splicing perturbado experimentalmente na maioria dos testes, mesmo entre diferentes tipos celulares e estudos. Também captou mecanismos regulatórios mais sutis. Por exemplo, um medicamento anticâncer chamado Indisulam desencadeia a degradação da proteína do fator de splicing RBM39 enquanto seus níveis de RNA aumentam, em algo que parece ser uma tentativa de compensação. Análises tradicionais de expressão sugeririam, de forma enganosa, que RBM39 está mais ativo, mas a pontuação de atividade baseada em éxons revelou corretamente uma forte perda de função, compatível com a ação conhecida do fármaco.
Descobrindo Programas Ocultos de Splicing no Câncer
Com essa ferramenta, os autores voltaram-se para o The Cancer Genome Atlas, analisando dados ao nível de éxons de múltiplos tipos tumorais e tecidos saudáveis correspondentes. Eles descobriram dois programas de splicing amplos e recorrentes. Um programa consiste de fatores de splicing que tendem a estar mais ativos em tumores e está associado a pior sobrevida dos pacientes — um programa com caráter oncogênico. O outro apresenta fatores sistematicamente menos ativos em tumores e ligados a melhores desfechos, assemelhando‑se a supressores de tumor. Esses programas afetam genes envolvidos em características fundamentais do câncer, como divisão celular rápida e a capacidade dos tumores de escapar do sistema imunológico. Por exemplo, alguns éxons regulados pelo programa de caráter supressor de tumor parecem influenciar quão bem os pacientes respondem a terapias com checkpoint imunológico, apontando para novos marcadores ou pontos de intervenção.
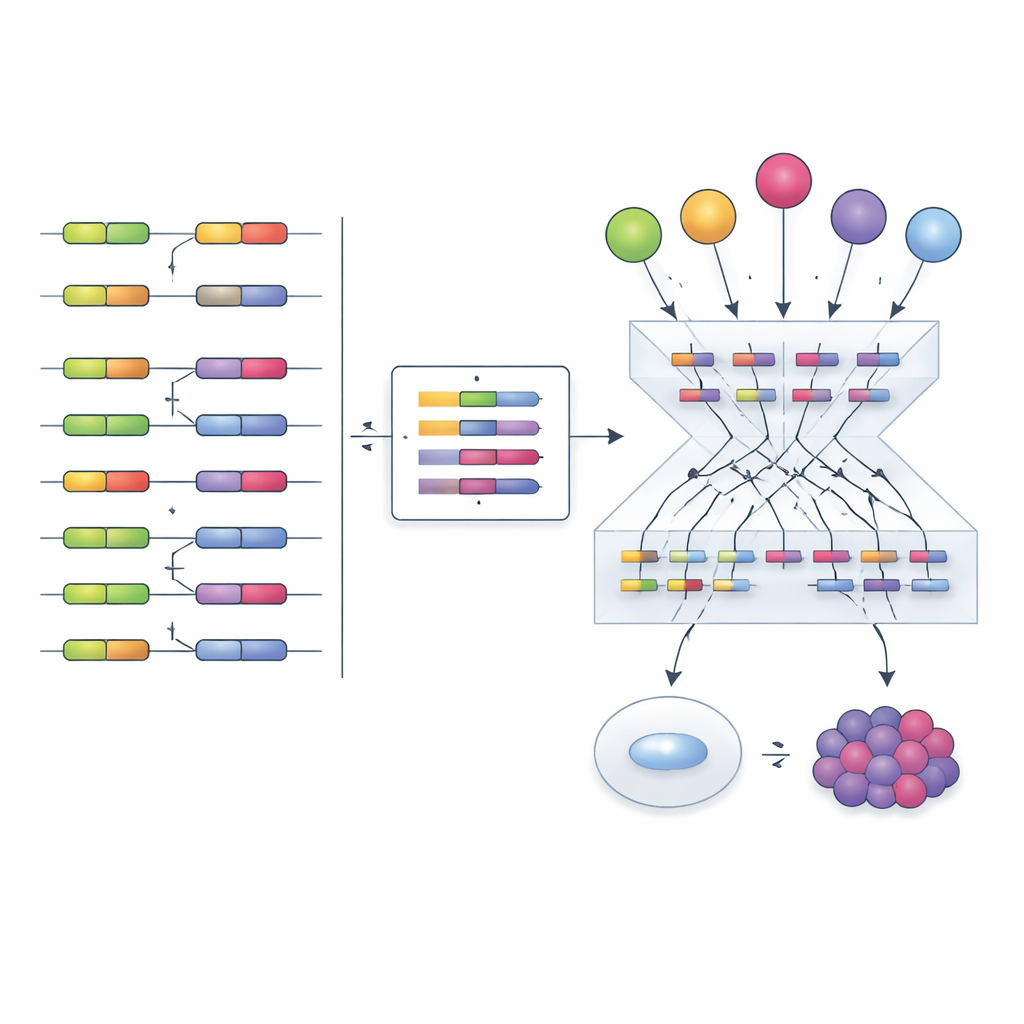
Acompanhando as Mudanças de Splicing no Caminho para o Câncer
A equipe também examinou um modelo passo a passo de células humanas progredindo de normal para imortalizada, formadora de tumor e, finalmente, metastática. Eles acharam que o programa de splicing com perfil oncogênico torna‑se mais ativo à medida que as células adquirem mutações que dirigem o câncer, enquanto o programa com perfil de supressor de tumor se enfraquece. Ao integrar múltiplas camadas de dados — níveis de RNA, abundância proteica, modificações químicas e mudanças de splicing dentro dos próprios fatores de splicing — identificaram um conjunto focalizado de eventos moleculares candidatos que podem impulsionar essas mudanças de programa, oferecendo uma lista priorizada para testes experimentais futuros.
Por Que Isso Importa para Pacientes e Pesquisas Futuras
Em essência, o estudo mostra que o comportamento complexo dos fatores de splicing pode ser destilado em uma única pontuação de atividade interpretável, derivada de como os éxons são incluídos ou excluídos. Isso torna possível estudar a regulação do splicing em grandes coortes de pacientes e em experimentos diversos usando apenas dados padrão de sequenciamento de RNA, sem exigir perfis multiômicos caros. Para um leitor leigo, a mensagem principal é que os padrões de como os genes são cortados e colados carregam informações ricas sobre os sistemas de controle ocultos da célula, e que decodificar esses padrões pode revelar novos condutores do câncer, melhorar o prognóstico e guiar a busca por tratamentos mais precisos.
Citação: Anglada-Girotto, M., Segura-Morales, C., Moakley, D.F. et al. Exon inclusion signatures enable accurate estimation of splicing factor activity. Nat Commun 17, 1994 (2026). https://doi.org/10.1038/s41467-026-69642-3
Palavras-chave: splicing de RNA, fatores de splicing, genômica do câncer, transcriptômica, inferência de atividade proteica