Clear Sky Science · pt
Engenharia gênica do microambiente tumoral induzida por LOAd703 em combinação com atezolizumabe no melanoma maligno metastático: ensaio de fase I/II
Por que este novo estudo sobre melanoma é importante
Para pessoas com melanoma cutâneo avançado que não respondem mais às potentes imunoterapias atuais, as opções de tratamento são limitadas e muitas vezes severas. Este estudo testa uma ideia diferente: usar um vírus geneticamente modificado injetado diretamente nos tumores, em conjunto com um medicamento imunomodulador já existente, para reativar as defesas do organismo e recuperar o controle sobre o câncer. Os resultados iniciais sugerem que essa abordagem pode ser administrada com segurança e pode ajudar uma parcela significativa de pacientes cuja doença havia resistido ao tratamento padrão.
Um câncer de pele persistente que dribla o tratamento
O melanoma é um dos cânceres de pele graves mais comuns em países ocidentais, e sua incidência aumentou fortemente nas últimas décadas. Os modernos medicamentos que bloqueiam pontos de controle imunológicos — que liberam o freio das células T — transformaram os desfechos, elevando a sobrevida em cinco anos no melanoma avançado para cerca de metade dos pacientes. Ainda assim, muitos tumores acabam deixando de responder. Frequentemente, esses cânceres resistentes estão cercados por um ambiente “frio” de células e moléculas que mantêm as células imunes fora ou as desligam. Encontrar maneiras de reconfigurar esse microambiente tumoral para que as células T possam novamente reconhecer e atacar o câncer é uma prioridade importante na pesquisa.
Um vírus projetado para reconfigurar o entorno do tumor
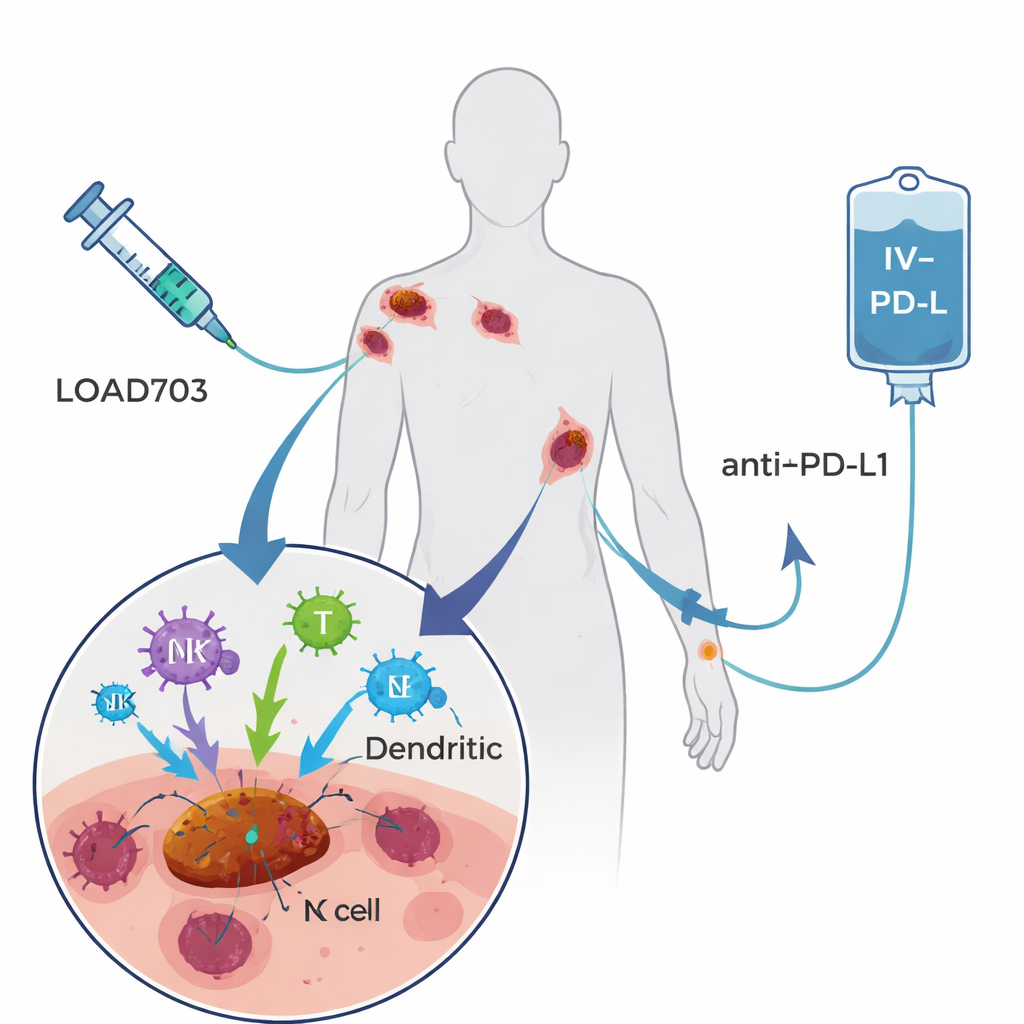
O tratamento testado aqui, chamado LOAd703, é um adenovírus modificado — um tipo de vírus do resfriado comum — projetado para desempenhar duas funções. Primeiro, ele prefere se replicar em células tumorais e destruí‑las, uma estratégia conhecida como viroterapia oncolítica. Segundo, carrega instruções genéticas para dois sinais potentes que estimulam o sistema imune expressos nas células infectadas. Esses sinais, CD40L e 4‑1BBL, ajudam sentinelas profissionais do sistema imune (células dendríticas) a amadurecer e apresentar fragmentos tumorais, além de fortalecer e expandir células T e células natural killer que combatem o câncer. Os pacientes no ensaio receberam LOAd703 injetado diretamente em um ou mais tumores a cada três semanas, juntamente com atezolizumabe, um anticorpo estabelecido administrado por via intravenosa que bloqueia a freada PD‑L1 nas células T. A esperança era que o vírus transformasse os tumores em fábricas de vacina dentro do corpo, enquanto o anticorpo mantinha as células T reativadas em atividade.
Quem foi tratado e como se saíram
O ensaio de fase I/II incluiu 24 pessoas com melanoma em estágio IV que claramente progrediram apesar de pelo menos um tratamento prévio com bloqueador de PD‑1; muitos tinham recebido várias linhas de imunoterapia e drogas-alvo. Foram testados dois níveis de dose do vírus. No geral, a combinação foi bem tolerada. Os efeitos colaterais mais comuns associados ao vírus — febre, calafrios, náusea e sintomas gripais — foram em sua maioria leves e temporários. Apenas dois pacientes apresentaram reações mais sérias, mas reversíveis, na dose mais alta, e ninguém precisou interromper o tratamento por problemas relacionados ao vírus. Ao analisar as respostas tumorais, quatro pacientes (17%) tiveram redução mensurável de seus cânceres, e mais da metade manteve pelo menos doença estável por algum tempo. Dois anos após a inclusão no estudo, quase metade dos participantes ainda estava viva, incluindo alguns cujos exames mostraram controle prolongado ou eliminação completa de doença detectável após o término da terapia.
Sinais de que o sistema imune foi reengajado
Para entender o que ocorria dentro dos tumores e na corrente sanguínea, a equipe analisou biópsias de tecido e amostras de sangue coletadas antes do tratamento e cerca de nove semanas após o início. Nos tumores injetados, observaram maior atividade de genes ligados a respostas imunes do tipo 1, incluindo marcadores de células T ativadas e células natural killer, e moléculas que ajudam essas células a entrar nos tumores a partir de vasos sanguíneos próximos. Sinais associados à apresentação de antígenos — o processo pelo qual fragmentos tumorais são exibidos às células T — também aumentaram, sugerindo que a terapia viral estava transformando o microambiente tumoral de supressor para mais favorável ao sistema imune. No sangue, várias proteínas relacionadas ao sistema imune, incluindo a própria PD‑L1, aumentaram após a terapia, compatível com uma ativação ampla de vias imunes. Pacientes que sobreviveram por mais tempo tenderam a apresentar padrões gênicos ligados a função robusta de células T e proteção antiviral, enquanto aqueles com sobrevida mais curta mostraram padrões associados a tipos celulares supressores e sinais de remodelamento tecidual.
O que isso pode significar para cuidados futuros
Este foi um estudo pequeno, com braço único e sem grupo de comparação, de modo que suas taxas de sobrevida e resposta devem ser interpretadas com cautela. Ainda assim, a combinação de boa tolerabilidade, ativação imune nos tumores e controle encorajador da doença em pacientes fortemente pré‑tratados sugere que vírus oncolíticos geneticamente modificados como o LOAd703 podem ajudar a ressensibilizar o melanoma ao bloqueio de checkpoints — ou mesmo manter tumores sob controle por conta própria. Os resultados apoiam a realização de ensaios maiores e controlados, potencialmente combinando o vírus com medicamentos adicionais que atuem no sistema imune, para esclarecer quais pacientes mais se beneficiam e como integrar melhor essa estratégia ao tratamento do melanoma.
Citação: Hamid, O., Ekström-Rydén, V., Mehmi, I. et al. LOAd703-induced tumor microenvironment gene engineering in combination with atezolizumab in metastatic malignant melanoma: a phase I/II trial. Nat Commun 17, 1760 (2026). https://doi.org/10.1038/s41467-026-69629-0
Palavras-chave: melanoma, imunoterapia, vírus oncolítico, microambiente tumoral, resistência a inibidores de checkpoint