Clear Sky Science · pt
Sensoriamento massivamente paralelo baseado em nanoporo para perfilagem de peptídeos e identificação de proteínas
Lendo proteínas uma molécula de cada vez
Proteínas são as protagonistas do trabalho nas nossas células, e saber exatamente quais estão presentes, como são modificadas e como interagem é central para entender saúde e doença. As ferramentas padrão de hoje para estudar proteínas são poderosas, mas muitas vezes lentas, caras e difíceis de escalar. Este artigo descreve uma nova forma de escutar fragmentos individuais de proteína enquanto passam por um orifício minúsculo em uma membrana, usando inteligência artificial para transformar esses sinais em impressões digitais detalhadas. A abordagem pode abrir caminho para testes mais rápidos e baratos para rastrear marcadores de doença e verificar quão bem anticorpos de pesquisa e diagnóstico realmente funcionam.
Transformando proteínas em pedaços legíveis
Os pesquisadores constroem sobre a tecnologia de nanoporo, originalmente desenvolvida para sequenciamento de DNA. No sistema deles, proteínas naturais são primeiro cortadas em fragmentos mais curtos chamados peptídeos e modificadas suavemente para que cada pedaço possa ser ligado em ambas as extremidades a trechos curtos de DNA. Isso cria uma estrutura "Oligo–Peptídeo–Oligo" que se comporta bem em dispositivos de nanoporo originalmente projetados para DNA. A equipe usa uma enzima de corte específica que tende a deixar um aminoácido particular, lisina, na extremidade de cada fragmento, tornando a química mais previsível e compatível com muitas proteínas diferentes. O resultado final é uma biblioteca purificada de muitos desses constructos peptídeo–DNA preparada em apenas algumas horas.
Escutando com muitos nanoporos ao mesmo tempo
Para realmente detectar esses fragmentos de peptídeo, os autores usam um arranjo de nanoporos biológicos — orifícios minúsculos feitos de proteínas inseridos em uma membrana e conectados a eletrodos. Quando uma voltagem é aplicada, as estruturas DNA‑peptídeo‑DNA são puxadas, uma a uma, através de cada poro por um motor molecular. À medida que o peptídeo passa pela parte mais estreita, ele bloqueia parcialmente o fluxo de íons, mudando a corrente elétrica. Como a plataforma usa 256 poros em paralelo e pode coletar mais de 100.000 desses eventos a partir de uma única biblioteca em menos de duas horas, ela produz um fluxo maciço de sinais de moléculas individuais que capturam como cada peptídeo específico interage com o poro. 
De sinais ruidosos a impressões digitais distintas
Na superfície, esses traços de corrente parecem ruidosos e variáveis; o mesmo peptídeo pode entrar em orientações diferentes e adotar conformações distintas. Medidas resumidas tradicionais, como corrente média e duração do evento, frequentemente se sobrepõem entre peptídeos semelhantes. O avanço chave neste trabalho é um pipeline de inteligência artificial em dois passos. Primeiro, uma rede neural convolucional profunda é treinada em grande número de traços para classificar qual peptídeo produziu qual padrão. Segundo, a equipe cria “matrizes de densidade” que resumem como o sinal tende a variar ao longo do evento, essencialmente transformando nuvens de traços ruidosos em impressões digitais 2D estáveis. Apenas leituras cujos padrões temporais detalhados correspondem a essas impressões digitais são mantidas. Essa estratégia CNN-plus-fingerprint aumenta a precisão para cerca de 99% em peptídeos de teste e consegue distinguir de forma confiável fragmentos que difere por um único aminoácido, certos isômeros e muitas modificações químicas comuns que proteínas adquirem nas células.
Verificando anticorpos e identificando proteínas inteiras
Como anticorpos reconhecem trechos curtos de proteínas, os autores aplicam sua plataforma para mapear quais fragmentos vários anticorpos comerciais realmente ligam. Misturando peças de peptídeos sobrepostas de um precursor hormonal, enriquecendo aquelas ligadas por cada anticorpo e então lendo-as com o sistema de nanoporo, eles podem localizar regiões de ligação preferidas e mostrar quando pares de anticorpos recomendados pelo fornecedor realmente reconhecem o mesmo sítio e são mal pareados para ensaios do tipo sandwich. Em outro teste, examinam uma sequência de etiqueta bem conhecida e quatro variantes quase idênticas, mostrando que o número relativo de leituras por nanoporo para cada peptídeo acompanha de perto a força de ligação do anticorpo, coerente com medições de superfície mais trabalhosas. Por fim, demonstram identificação de proteínas: treinam o sistema em impressões digitais de peptídeos de três proteínas humanas, então digerem às cegas as proteínas completas e mostram que o padrão combinado de peptídeos classificados é suficiente para identificar corretamente qual proteína é qual, mesmo diante de alguns fragmentos ambíguos ou ausentes. 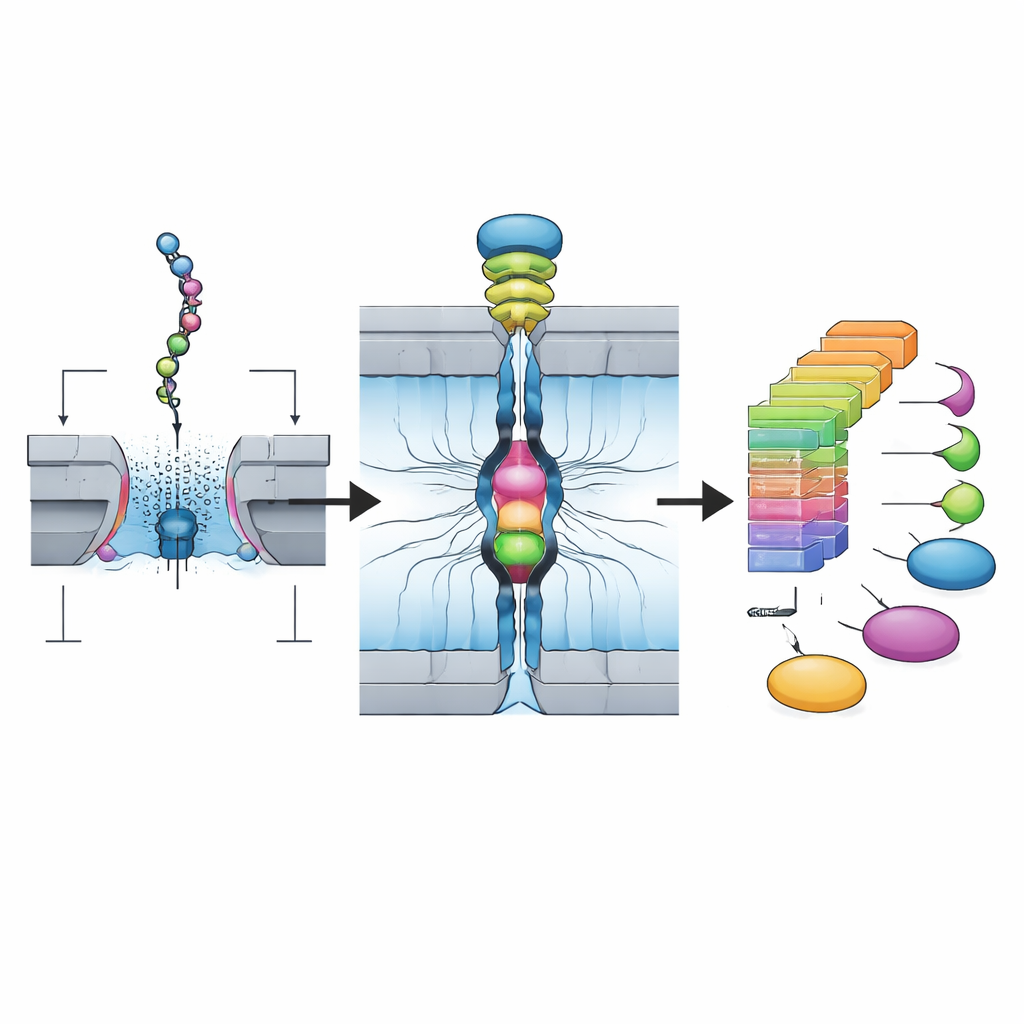
Por que isso importa para testes futuros
Em termos simples, o estudo mostra que um sequenciador estilo DNA baseado em nanoporo, acoplado a química inteligente e IA, pode atuar como um "estetoscópio" altamente paralelo para fragmentos de proteínas. Em vez de precisar ler cada aminoácido em ordem, o sistema baseia-se em impressões digitais estatísticas ricas de milhares de eventos de molécula única para distinguir diferenças sutis em carga, tamanho e modificação. Isso possibilita checagens rápidas e de baixo custo da qualidade de anticorpos e oferece um caminho para reconhecer proteínas inteiras a partir de seus padrões de peptídeos. Embora ainda existam limites — como dificuldades com certos tipos de peptídeos e a necessidade de bons dados de treinamento — o trabalho descreve um pipeline de ponta a ponta que pode ajudar a aproximar análises de proteínas de alto rendimento das rotinas dos laboratórios de pesquisa e, eventualmente, da prática diagnóstica clínica.
Citação: Wang, J., Chen, J., Pan, H. et al. Nanopore-based massively parallel sensing for peptide profiling and protein identification. Nat Commun 17, 3058 (2026). https://doi.org/10.1038/s41467-026-69628-1
Palavras-chave: sensoriamento por nanoporo, proteômica, impressão digital de peptídeos, validação de anticorpos, identificação de proteínas