Clear Sky Science · pt
Drogas “presas” liberam óxido nítrico e anestésicos por foto-catálise dupla para analgesia antibacteriana
Combater germes e dor ao mesmo tempo
Infecções bacterianas não apenas ameaçam nossa saúde; elas também causam dor — muita dor. Tratamentos padrão costumam mirar apenas nos microrganismos, deixando os pacientes dependentes de analgésicos separados, que podem perder efeito rapidamente ou causar efeitos colaterais. Este estudo apresenta um medicamento controlado por luz que pretende matar bactérias e aliviar a dor em um único passo coordenado, oferecendo um vislumbre de cuidados para infecções mais inteligentes e confortáveis.
Uma ideia de medicamento dois em um
Os pesquisadores basearam sua abordagem na tetracaína, um anestésico local conhecido usado para anestesiar pele e nervos. Eles ligaram quimicamente o óxido nítrico, uma pequena molécula gasosa conhecida por suas fortes ações antibacterianas e anti-inflamatórias, à tetracaína. Isso criou um “pró-fármaco” chamado TTC-NO que é em grande parte inativo até ser acionado. O TTC-NO foi então embalado, junto com uma molécula auxiliadora sensível à luz, em pequenas bolhas poliméricas chamadas micelas que podem viajar em ambientes aquosos como sangue ou fluido tecidual. 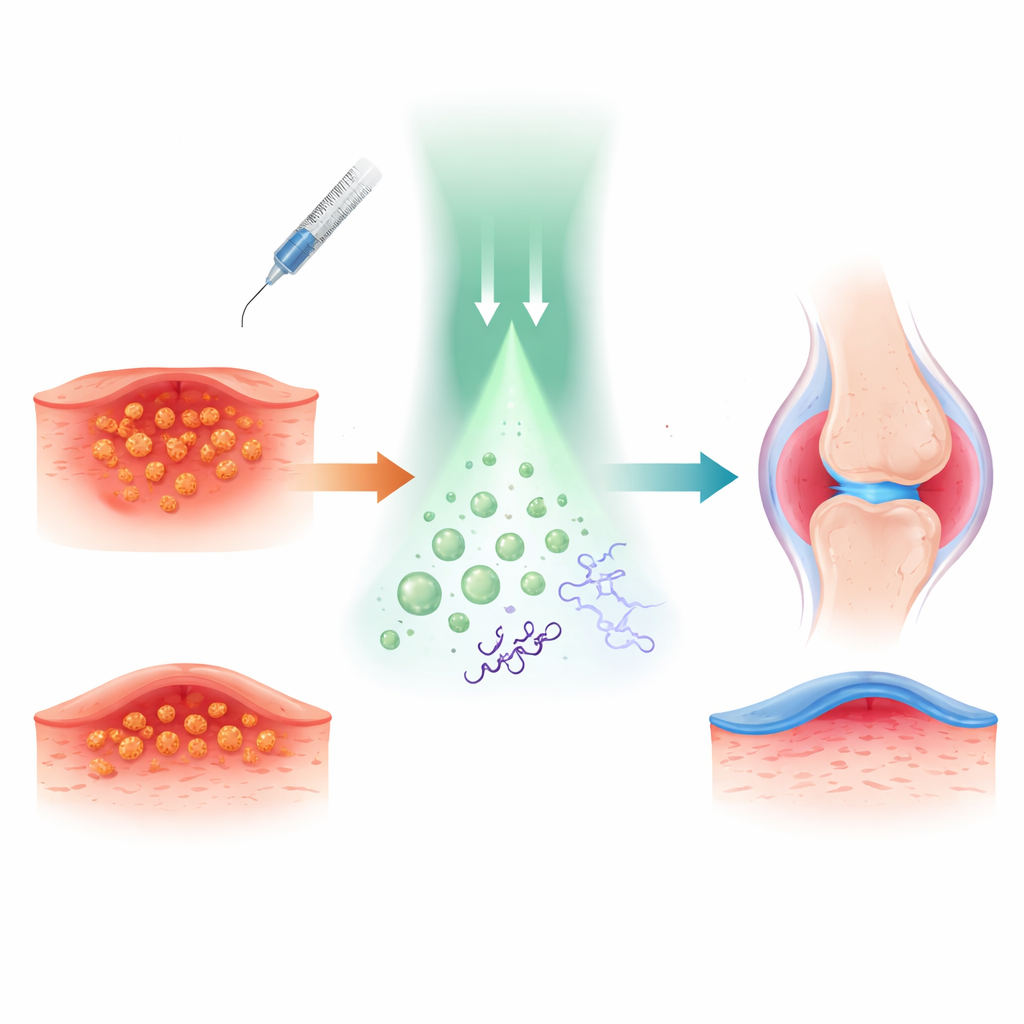
Ativando o medicamento com luz suave
Para entender como esse interruptor luminoso funciona, a equipe estudou a química em solução. Demonstraram que um fotocatalisador à base de irídio pode transferir um elétron para o TTC-NO quando iluminado com luz verde. Isso enfraquece uma ligação específica, causando a liberação do óxido nítrico e restaurando a tetracaína à sua forma ativa. Medições por espectroscopia e cromatografia confirmaram que o TTC-NO é quase completamente convertido em tetracaína e óxido nítrico nessas condições, enquanto permanece essencialmente inalterado no escuro. Quando os dois componentes foram encapsulados em micelas, as partículas permaneceram estáveis, com cerca de 80 nanômetros de diâmetro, e liberaram seu conteúdo apenas quando irradiadas, provando que o conceito de “fármaco preso em fármaco” pode ser controlado de fora do corpo com luz.
Ajudando feridas infectadas a cicatrizarem mais rápido
A equipe então passou para camundongos com feridas na pele deliberadamente infectadas com Staphylococcus aureus resistente à meticilina (MRSA), uma bactéria problemática em hospitais. Algumas feridas receberam tratamentos padrão, como um antibiótico ou fator de crescimento, enquanto outras foram tratadas com as micelas de TTC-NO, com ou sem luz. Quando a luz foi ligada, o sistema TTC-NO reduziu drasticamente a contagem bacteriana, acalmou a inflamação, incentivou o crescimento de novos vasos sanguíneos e aumentou a deposição de colágeno, todos essenciais para a reparação adequada. As feridas tratadas dessa forma fecharam mais rápida e completamente do que as tratadas apenas com tetracaína ou com micelas mantidas no escuro, e seu desempenho foi comparável ao de um antibiótico de primeira linha. Importante, checagens de segurança não mostraram danos significativos aos órgãos ou à química sanguínea.
Aliviando a dor e silenciando sinais nervosos
Como a infecção e a lesão tecidual ativam fortemente as vias da dor, os cientistas mediram cuidadosamente comportamentos relacionados à dor no mesmo modelo de ferida. A tetracaína tradicional aumentou brevemente a força necessária para desencadear uma resposta dolorosa, mas perdeu efeito em poucas horas. Em contraste, as micelas TTC-NO ativadas por luz proporcionaram alívio por até 12 horas. Estudos microscópicos de aglomerados nervosos próximos à medula espinhal e gravações de atividade no córtex sensorial do cérebro revelaram que o tratamento combinado reduziu o disparo de neurônios sensoriais de dor muito tempo depois de a tetracaína pura ter perdido seu efeito. Experimentos adicionais sugeriram que a duração extra vem da redução da carga bacteriana e da inflamação pelo óxido nítrico, não apenas do entorpecimento dos nervos.
Protegendo articulações infectadas e dolorosas
Os pesquisadores também testaram o sistema em camundongos com artrite séptica, uma infecção grave por MRSA dentro da articulação do joelho que causa inchaço, perda óssea e dor intensa. Micelas TTC-NO ativadas por luz reduziram a largura da articulação, diminuíram o número de bactérias e protegeram a estrutura óssea, conforme observado por varreduras de alta resolução. Os níveis de moléculas inflamatórias nocivas no sangue caíram, enquanto moléculas sinalizadoras protetoras aumentaram. Comportamentalmente, os animais tratados toleraram maior pressão mecânica na pata afetada e se moveram mais livremente em um arena aberta, novamente mostrando alívio de mais longa duração do que a tetracaína isolada. Medidas nervosas e cerebrais espelharam esses ganhos comportamentais, indicando um amplo abafamento das vias da dor sem toxicidade local ou sistêmica óbvia. 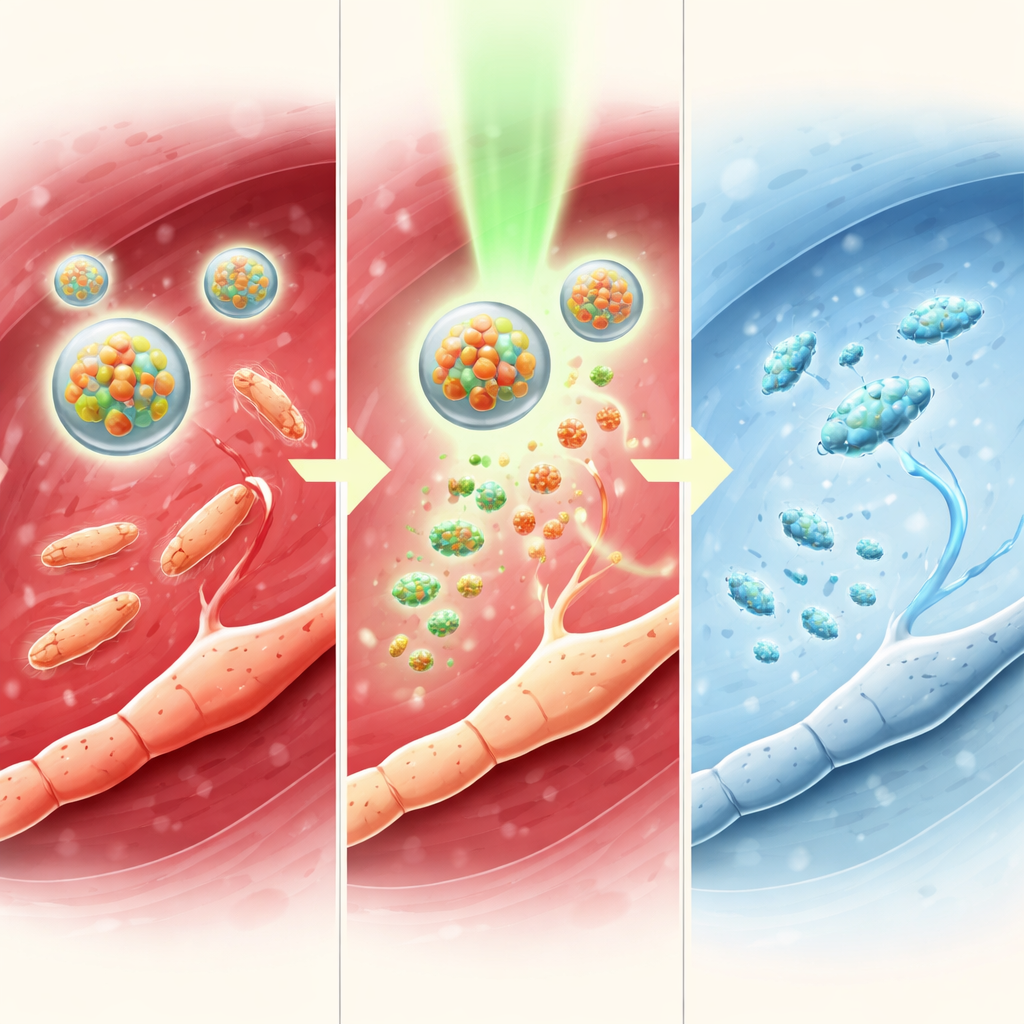
O que isso pode significar para pacientes
Em conjunto, o trabalho demonstra um único nanosistema ativado por luz que pode tanto eliminar infecções bacterianas persistentes quanto reduzir significativamente a dor associada. Ao “prender” quimicamente um anestésico dentro de uma estrutura liberadora de óxido nítrico e empacotá-lo em micelas, os autores alcançam liberação localizada e sob demanda de dois agentes úteis usando luz visível suave. Em modelos animais de feridas cutâneas e infecções articulares, esse desenho acelera a cicatrização e prolonga o alívio da dor além do que um anestésico local convencional pode oferecer. Embora muitos testes ainda sejam necessários antes do uso humano, o estudo destaca como medicamentos inteligentes e com interruptor podem, um dia, tornar os tratamentos de infecção mais eficazes e confortáveis.
Citação: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
Palavras-chave: terapia com óxido nítrico, fármacos ativados por luz, analgesia antibacteriana, nanomedicina, infecções por MRSA