Clear Sky Science · pt
O eixo Treg-γδ determina a dimorfia sexual na hepatocarcinogênese
Por que alguns cânceres de fígado atingem mais os homens
Os médicos sabem há muito tempo que o câncer de fígado atinge os homens cerca de duas vezes mais do que as mulheres, mas as razões vão além das diferenças simples em hormônios sexuais. Este estudo investiga as células imunes presentes dentro dos tumores hepáticos e revela uma conversa oculta entre dois tipos de células T que ajuda a explicar por que os fígados masculinos são mais vulneráveis — e como esse conhecimento pode apontar para tratamentos novos e mais personalizados.
A disputa imune dentro dos tumores hepáticos
O câncer de fígado, particularmente o carcinoma hepatocelular, cresce num microambiente complexo de células imunes, vasos sanguíneos e tecido cicatricial. Os autores compararam tumores de homens e mulheres, tanto em pacientes quanto em modelos de camundongos, e encontraram um desequilíbrio marcante: tumores masculinos abrigavam mais células T reguladoras, ou Tregs, um tipo celular que normalmente ajuda a conter reações imunes excessivas. Ao mesmo tempo, o número total de outros tipos comuns de células T não diferiu muito entre os sexos. Como níveis elevados de Tregs se associaram a pior sobrevida, a equipe suspeitou que essas células não eram meros espectadores, mas cúmplices ativas que ajudam o tumor a escapar do ataque imune. 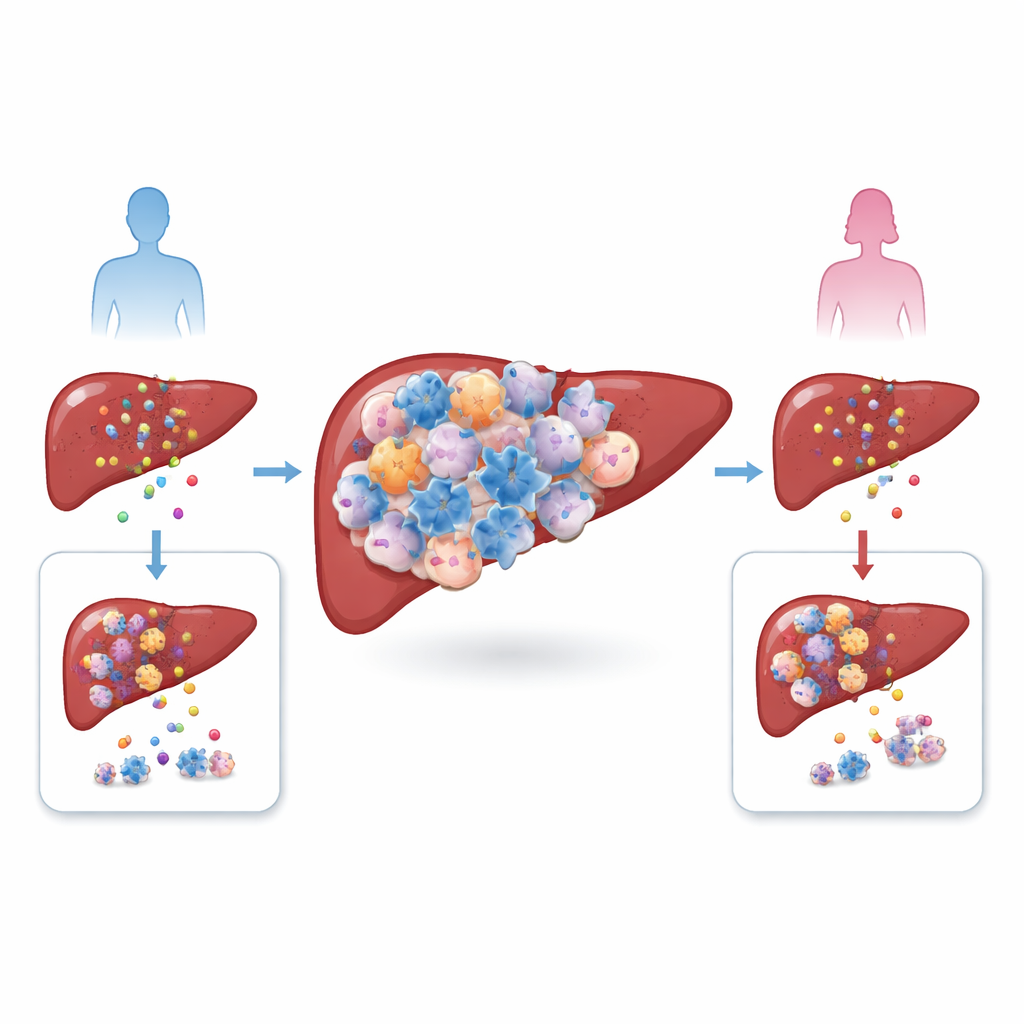
Como hormônios masculinos recrutam células supressoras
Para entender por que tumores masculinos atraem mais Tregs, os pesquisadores focaram nos sinais químicos produzidos pelas células cancerígenas. Eles descobriram que tumores hepáticos masculinos produziam maiores quantidades de uma molécula chamada Ccl2, enquanto as Tregs apresentavam mais de seu receptor correspondente, Ccr2. Esse pareamento age como um farol de homing, atraindo Tregs para o tumor. Quando o sinal Ccl2 ou o receptor Ccr2 foi eliminado em camundongos, os tumores diminuíram e bem menos Tregs infiltraram o fígado, especialmente nos machos. A equipe então mostrou que a testosterona, o principal hormônio sexual masculino, impulsiona esse processo: ela ativa uma cascata de proteínas nas células do câncer hepático que liga o gene Ccl2, intensificando o chamado químico que convoca as Tregs. Camundongos machos castrados, que produzem menos testosterona, apresentaram menor Ccl2 em seus tumores e menos Tregs infiltrantes.
Células guardiãs que poderiam combater o câncer — mas são contidas
Outro tipo de célula T, conhecido como células T gama-delta, pode atuar como "guardiãs" de resposta rápida que reconhecem e matam células tumorais sem a maquinaria habitual de apresentação de antígenos. No fígado saudável, essas células são relativamente escassas, mas no câncer hepático podem ser combatentes tumorais potentes. O estudo encontrou que tumores femininos continham mais dessas células gama-delta e que elas estavam mais ativas e melhor equipadas com moléculas tóxicas. A remoção dos hormônios sexuais masculinos em camundongos aumentou o número e o vigor das células gama-delta nos tumores, enquanto as células T CD8 clássicas permaneceram em grande parte inalteradas. Em culturas de laboratório, células gama-delta lesionaram prontamente células de câncer hepático, mas esse efeito foi enfraquecido quando Tregs foram adicionadas, sugerindo que as Tregs reprimem especificamente essa população anti-tumoral promissora.
Hipóxia, pacotes secretos e defensores silenciados
Avançando na investigação, os pesquisadores perguntaram como as Tregs conseguem suprimir as células T gama-delta. Dentro dos tumores, o oxigênio frequentemente é escasso, um estado chamado hipóxia. Sob essas condições de baixo oxigênio, as Tregs em tumores masculinos começaram a produzir grandes quantidades de uma proteína chamada S100a4. Em vez de atuar diretamente como molécula livre, S100a4 foi empacotada em pequenas partículas membranosas conhecidas como vesículas extracelulares. Essas vesículas brotavam das Tregs e eram captadas pelas células T gama-delta vizinhas. Uma vez dentro, S100a4 reprogramou os sistemas de controle genético das células: reduziu a acessibilidade de regiões do DNA que controlam moléculas-chave de sinalização e de citotoxicidade e diminuiu sua atividade. As células gama-delta tornaram-se menos capazes de responder via seus receptores de célula T e menos aptas a liberar proteínas tóxicas e citocinas, embotando efetivamente sua lâmina anti-câncer. 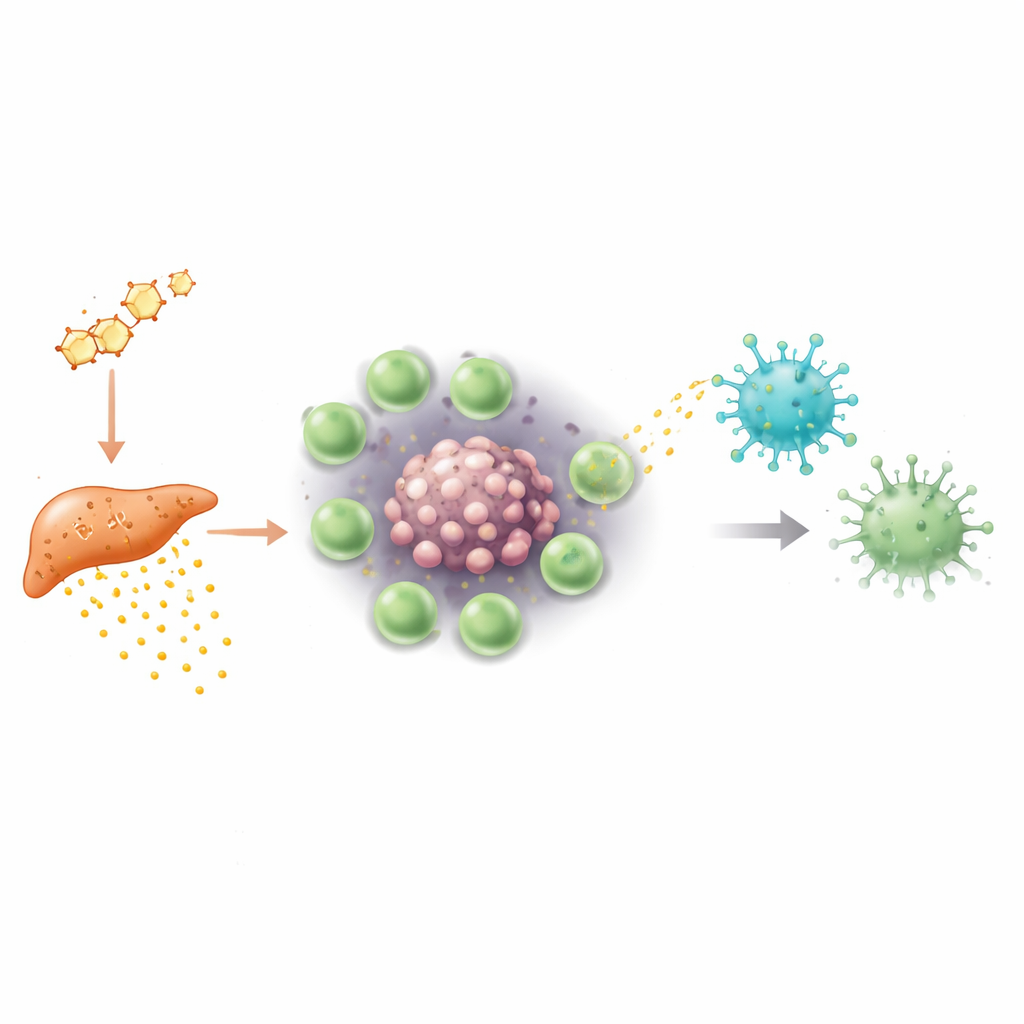
Quebrando o circuito nocivo
Por fim, a equipe testou o que ocorre se esse eixo Treg–S100a4–gama-delta for interrompido. Em camundongos geneticamente modificados para que as Tregs não produzam S100a4, os tumores hepáticos masculinos encolheram, o nível geral de S100a4 nos tumores caiu e as células T gama-delta tornaram-se mais abundantes e mais ativas. Notavelmente, o número de Tregs no tumor não diminuiu — apenas seu impacto supressivo sobre as células gama-delta foi levantado. Essa mudança praticamente eliminou a diferença habitual na gravidade tumoral entre camundongos machos e fêmeas, ressaltando o quão central essa via é para as diferenças sexuais no câncer de fígado.
O que isso significa para tratamentos futuros
Em termos acessíveis, o estudo mostra que hormônios masculinos induzem células do câncer hepático a emitir sinais "de boas-vindas" mais fortes para Tregs supressoras. Uma vez dentro do tumor — e sob o estresse da baixa oxigenação — essas Tregs enviam vesículas cheias de S100a4 que desarmam silenciosamente as células T gama-delta próximas, que de outra forma poderiam manter o câncer sob controle. Ao visar tanto o sinal Ccl2 que traz as Tregs quanto as mensagens de S100a4 que silenciam as células gama-delta, terapias futuras poderiam restaurar as defesas do próprio corpo, especialmente em homens. Este trabalho sugere que o tratamento do câncer de fígado pode se beneficiar de uma abordagem sensível ao sexo e de aproveitar, em vez de ignorar, as forças únicas das células T gama-delta.
Citação: Liang, Q., Zhang, Q., Zhang, W. et al. Treg-γδ T cell axis determines sexual dimorphism in hepatocarcinogenesis. Nat Commun 17, 2640 (2026). https://doi.org/10.1038/s41467-026-69603-w
Palavras-chave: carcinoma hepatocelular, células T reguladoras, células T gama-delta, diferenças entre sexos, imunologia tumoral