Clear Sky Science · pt
Sinalização de cálcio pirimidinérgica conecta o metabolismo tubular à fibrose em doenças renais
Por que a cicatrização renal importa
A doença renal crônica afeta silenciosamente centenas de milhões de pessoas no mundo e frequentemente termina com os rins endurecidos e cicatrizados. Uma vez estabelecida essa cicatrização, chamada fibrose, recuperar a função renal perdida é difícil. Ainda assim, os médicos carecem de fármacos que interrompam especificamente a fibrose. Este estudo faz uma pergunta básica, porém crucial: como danos de curta duração nos túbulos renais gradualmente se transformam em tecido cicatricial duradouro, e interromper essa cadeia de eventos poderia retardar ou prevenir a insuficiência renal?
Túbulos renais atarefados e sua química oculta
Os túbulos proximais do rim são operários microscópicos que recuperam a maior parte da água e dos nutrientes filtrados do sangue. Para alimentar essa função, sua atividade química é incomum. Ao analisar dados de expressão gênica em célula única de rins de camundongos, os pesquisadores descobriram que essas células tubulares são particularmente ricas em genes envolvidos no processamento de pirimidinas, uma família de pequenas moléculas que normalmente ajudam a montar e reparar DNA e RNA. Em túbulos lesionados, uma enzima de uma via de “salvamento”, a citidina desaminase, foi fortemente aumentada, sugerindo que células danificadas reorganizam o uso de pirimidinas para manter certos blocos de construção ricos em energia — incluindo um composto chamado UDP — em níveis elevados.
Sinais que vazam de células danificadas
Quando a equipe lesionou células humanas semelhantes a túbulos em cultura com toxinas que imitam quimioterapia ou overdose de ácido fólico, as células liberaram UDP no fluido ao redor. Em rins de camundongo expostos a lesão, colorações de fatias de tecido mostraram tanto altos níveis da enzima de processamento de pirimidinas nos túbulos quanto sinais de que células de suporte vizinhas, chamadas fibroblastos, estavam se ativando e mudando de forma. Fibroblastos normalmente permanecem discretos entre os túbulos, mas, quando ativados, multiplicam-se e ajudam a depositar colágeno e outras fibras que engrossam e endurecem o tecido renal. Essas observações sugerem uma ideia simples: túbulos lesionados podem “vazar” sinais químicos de perigo que fibroblastos vizinhos conseguem detectar.
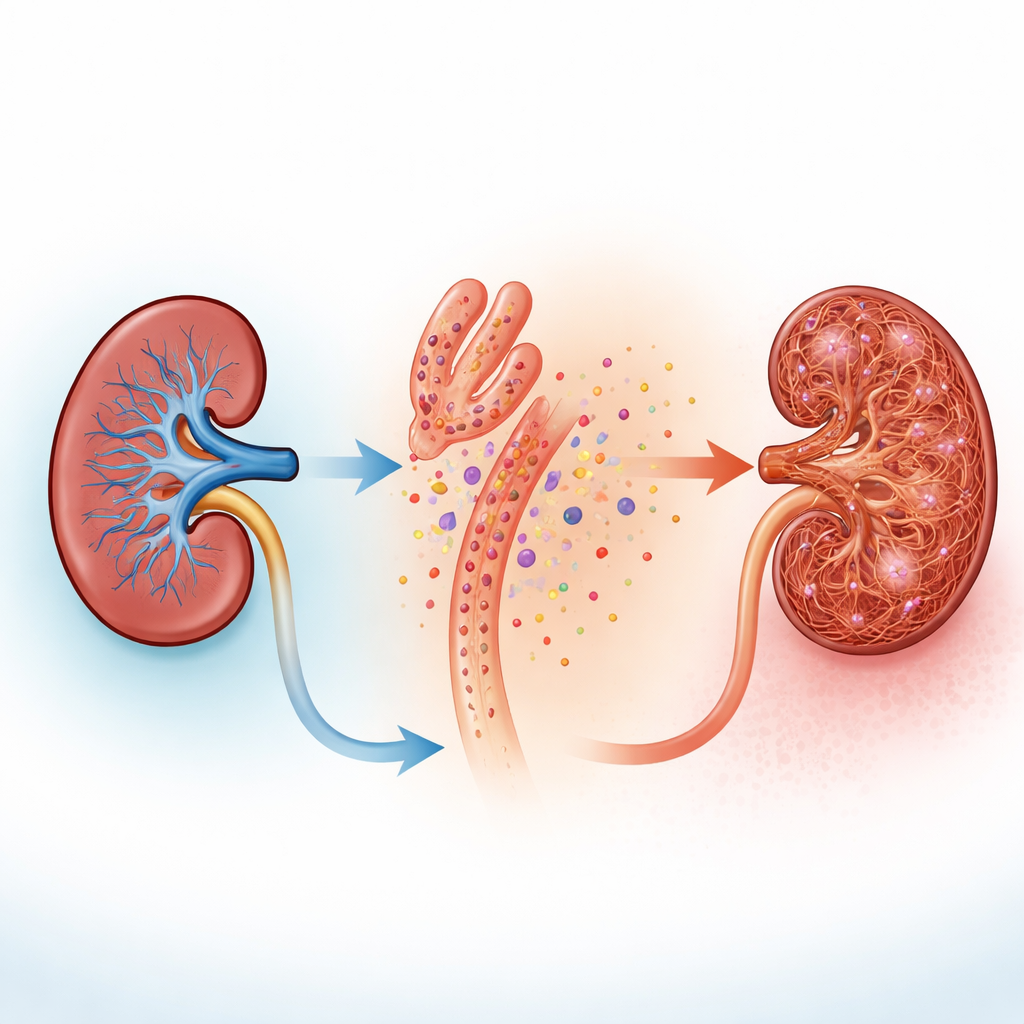
Como os fibroblastos escutam com lampejos de cálcio
Os supostos “ouvidos” dos fibroblastos são os receptores P2Y6, proteínas de superfície que respondem ao UDP. Ao explorar vários conjuntos de dados de célula única, os autores viram que o P2Y6 aparecia em células do estroma e aumentava ainda mais em modelos murinos de doença renal crônica. Medições em rins inteiros confirmaram aumentos marcantes nos níveis de P2Y6 em dois modelos distintos de cicatrização. Em fatias renais frescas e em fibroblastos renais em cultura projetados para acender quando o cálcio intracelular sobe, a adição de UDP ou de um fármaco ativador de P2Y6 produziu surtos rápidos de cálcio. Esses lampejos começaram nos longos e finos prolongamentos que envolvem os túbulos e então varreram o corpo celular, desaparecendo quando o P2Y6 foi bloqueado ou quando o cálcio foi quimicamente sequestrado. Em camundongos vivos, microscopia intravital de alta resolução mostrou que fibroblastos ao redor dos túbulos exibem atividade de cálcio frequente e irregular que aumenta dramaticamente quando os túbulos são lesionados, mesmo quando as próprias células tubulares ficam silenciosas.
De sinais breves a cicatrizes duradouras
Explosões de cálcio dentro de uma célula não são apenas fogos de artifício; podem reprogramar o comportamento celular. Quando fibroblastos em cultura foram expostos a um composto ativador de P2Y6, eles se multiplicaram mais rápido, migraram com maior facilidade e ativaram genes associados a um estado mais agressivo, de “miofibroblasto”. Esses genes codificam proteínas como fibronectina, vimentina e colágeno, que contribuem diretamente para a formação de cicatriz. Bloquear o P2Y6 ou impedir a elevação do cálcio eliminou essas mudanças, e reduzir a expressão do gene do receptor atenuou a resposta. Em camundongos, duas formas distintas de lesão renal — obstrução ureteral e nefropatia por ácido fólico — mostraram o mesmo padrão: rins lesionados apresentaram mais fibroblastos proliferando, mais marcadores de miofibroblastos, mais colágeno e áreas maiores de fibrose.
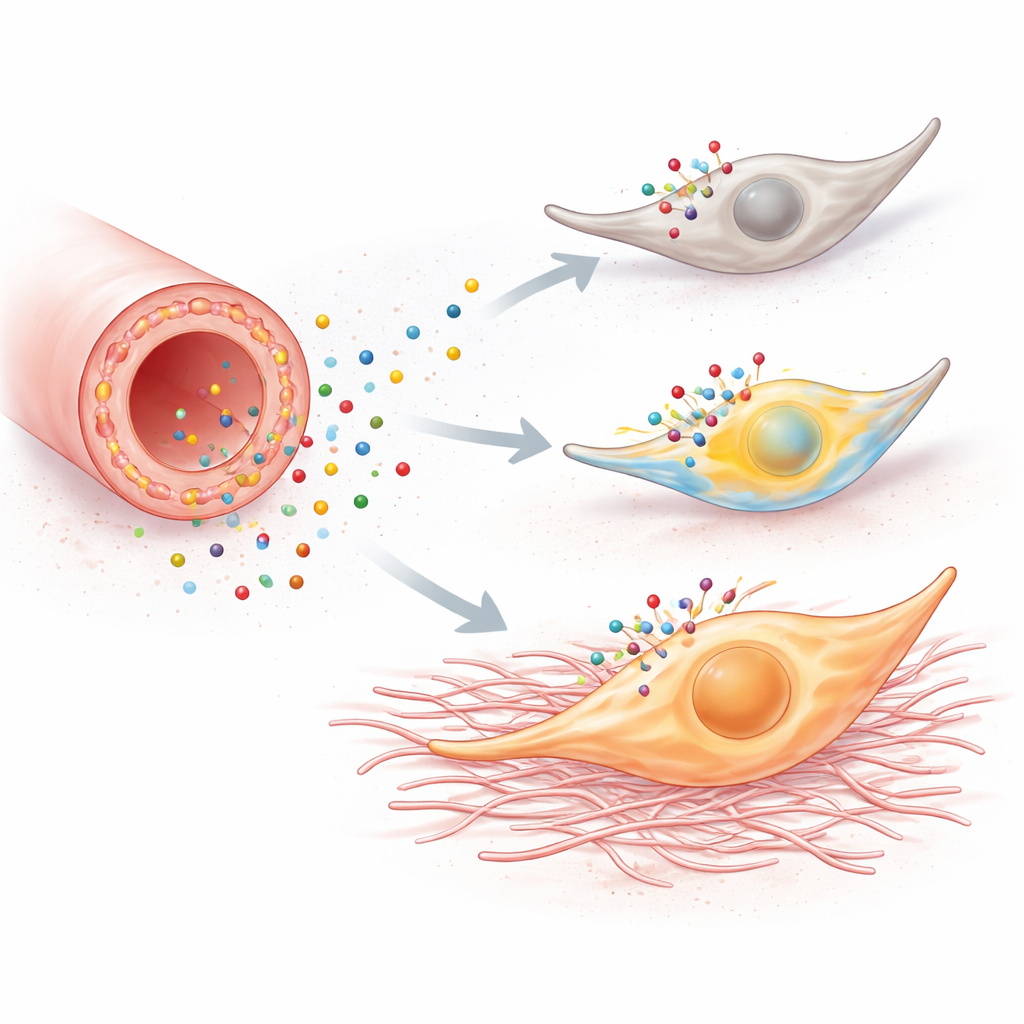
Diminuindo o volume do sinal nocivo
Para testar se essa via é não apenas presente, mas realmente prejudicial, os pesquisadores removeram o P2Y6 geneticamente ou o bloquearam com um fármaco. Camundongos sem o receptor desenvolveram menos fibrose renal após obstrução ureteral ou lesão por ácido fólico: seus fibroblastos proliferaram menos, depositaram menos matriz fibrosa e recrutaram menos células inflamatórias. Exames sanguíneos mostraram que esses animais knock-out também mantiveram melhor a função de filtração renal. Tratar camundongos normais com um composto bloqueador de P2Y6 produziu proteção comparável, incluindo atividade de cálcio reduzida nos fibroblastos e cicatrização diminuída, embora as melhorias nos marcadores sanguíneos fossem mais variáveis.
O que isso significa para tratamentos futuros
Em conjunto, o trabalho revela uma cadeia de eventos simples, porém poderosa. Quando as células dos túbulos renais são lesionadas, elas mudam sua química interna e liberam UDP no tecido circundante. Fibroblastos próximos detectam essa molécula por meio de seus receptores P2Y6, respondem com explosões de cálcio intracelular e então mudam para um modo de cicatrização — multiplicando-se, migrando e depositando colágeno. Interromper essa sinalização de cálcio baseada em pirimidina, especialmente no passo do P2Y6, reduz substancialmente a fibrose em vários modelos murinos. Para pacientes, isso sugere um novo tipo de alvo farmacológico: compostos que bloqueiem seletivamente o P2Y6 no rim podem ajudar a romper a ligação entre lesões renais comuns e a cicatrização lenta e irreversível que leva à doença renal crônica.
Citação: Figurek, A., Jankovic, N., Kollar, S. et al. Pyrimidinergic calcium signaling links tubular metabolism to fibrosis in kidney disease. Nat Commun 17, 3004 (2026). https://doi.org/10.1038/s41467-026-69602-x
Palavras-chave: doença renal crônica, fibrose renal, sinalização de fibroblastos, metabolismo de pirimidina, receptor P2Y6