Clear Sky Science · pt
Recrutamento duplo de duas moléculas CCM2 ao KRIT1 suprime a expressão de KLF4
Por que os vasos sanguíneos do cérebro precisam de controle cuidadoso
Os vasos sanguíneos do cérebro precisam manter um equilíbrio delicado: devem ser suficientemente robustos para evitar vazamentos, mas flexíveis o bastante para responder às necessidades do corpo. Quando esse equilíbrio falha, as pessoas podem desenvolver malformações cavernosas cerebrais — aglomerados de vasos frágeis em forma de bolha que podem sangrar e causar convulsões ou derrames. Este estudo revela um aperto de mão molecular antes desconhecido entre três proteínas que ajuda a manter os vasos cerebrais estáveis, e mostra como a ruptura desse mecanismo pode levar à doença.
Os guardiões da saúde dos vasos
As células que revestem os vasos sanguíneos dependem de um conjunto de interruptores mestres, chamados KLF2 e KLF4, para controlar genes que mantêm a resistência e a identidade dos vasos. Se esses interruptores são ativados em excesso, os vasos tornam-se anormais e suscetíveis a danos. Outras duas proteínas, KRIT1 e CCM2, são conhecidas por proteger esse sistema. Pessoas que herdam versões defeituosas de qualquer uma dessas proteínas têm alto risco de malformações cavernosas cerebrais. Até agora, porém, os cientistas não entendiam exatamente como KRIT1 e CCM2 atuavam em conjunto para manter KLF4 sob controle.
Uma equipe surpreendente de três
Os pesquisadores usaram células endoteliais humanas cultivadas em laboratório e reduziram seletivamente a quantidade de CCM2 ou KRIT1 com ferramentas genéticas. Quando qualquer uma das proteínas foi depletada, os níveis de KLF4 dispararam, ecoando o que se vê em modelos animais e em pacientes. Restaurar CCM2 ou KRIT1 aos níveis normais reduziu KLF4 — mas somente se as proteínas restauradas ainda pudessem se ligar entre si. Ao engenheirar mudanças precisas nas regiões onde CCM2 e KRIT1 interagem, a equipe demonstrou que esse contato físico é essencial para impedir o aumento de KLF4. Esses experimentos colocam firmemente a parceria KRIT1–CCM2 no centro do sistema de controle desse potente fator de transcrição.
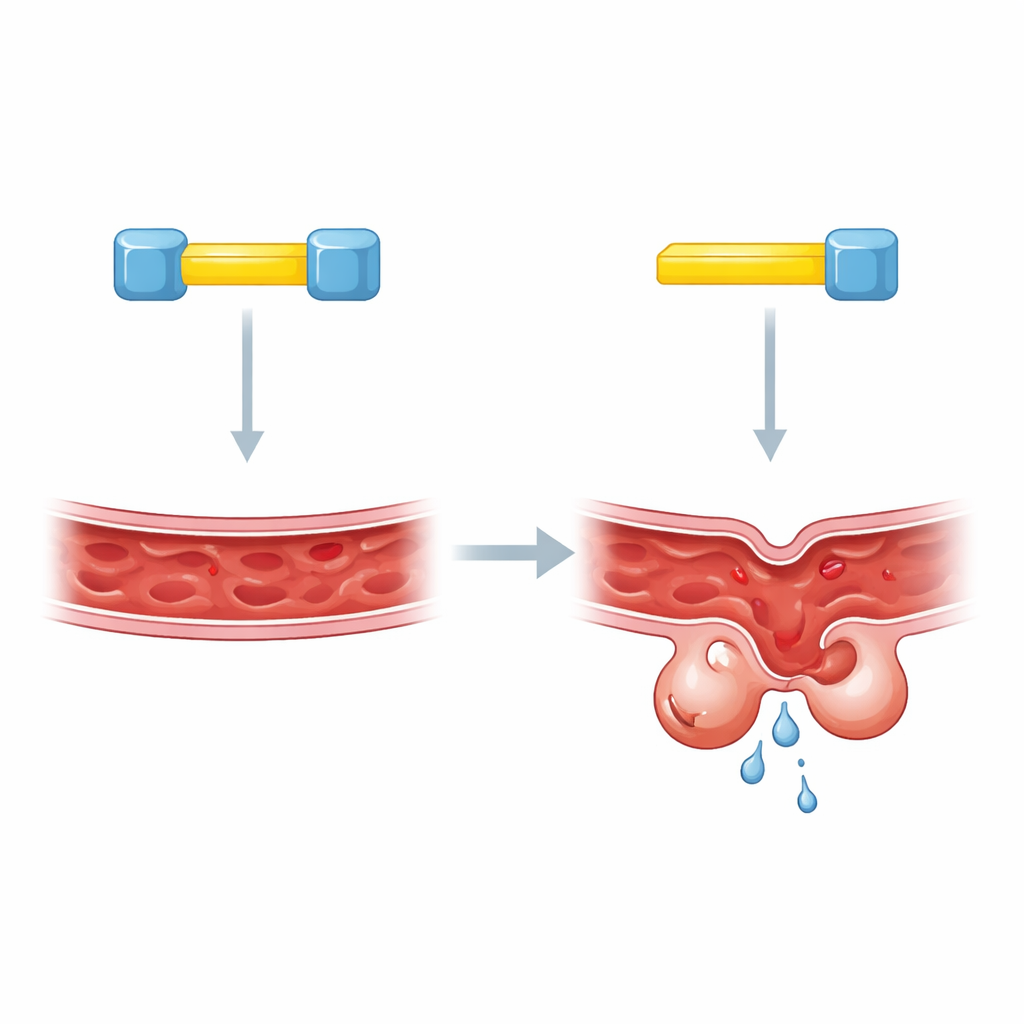
Dois cadeados em uma chave
Para investigar mais a fundo, os autores focalizaram segmentos curtos dentro de KRIT1 que atuam como locais de ancoragem molecular. Trabalhos anteriores sugeriram que CCM2 se liga a KRIT1 em um desses locais, mas métodos diferentes tinham produzido respostas conflitantes sobre qual seria esse local. O novo estudo revela que a confusão surgiu porque o quadro real é mais complexo: KRIT1 carrega dois segmentos de ancoragem próximos, e ambos são necessários. Quando qualquer segmento foi perturbado, os níveis de KLF4 permaneceram anormalmente altos, como se KRIT1 estivesse ausente. Testes bioquímicos em células modificadas mostraram que uma única proteína KRIT1 pode ligar duas moléculas distintas de CCM2 ao mesmo tempo, sugerindo uma montagem inesperada de três partes.
Vendo o grampo molecular em detalhe
A equipe então purificou os trechos relevantes de CCM2 e KRIT1 e examinou como eles se associam em solução e em cristais. Medidas da massa do complexo indicaram que duas cópias de uma região chave de CCM2 se ligam a uma única faixa de KRIT1 que carrega o par de locais de ancoragem. Instantâneos estruturais em alta resolução confirmaram esse arranjo 2:1: um peptídeo estendido de KRIT1 passa entre dois domínios de CCM2, com cada local de ancoragem encaixando-se em um bolso semelhante em uma molécula distinta de CCM2. Um pequeno segmento helicoidal entre os locais de ancoragem ajuda a posicionar os dois domínios de CCM2 lado a lado, criando uma estrutura aconchegante em formato de grampo. Esse tipo de engajamento duplo — dois domínios de ligação aferrando-se a sítios em tandem em um parceiro — não havia sido observado antes para essa família de módulos proteicos.
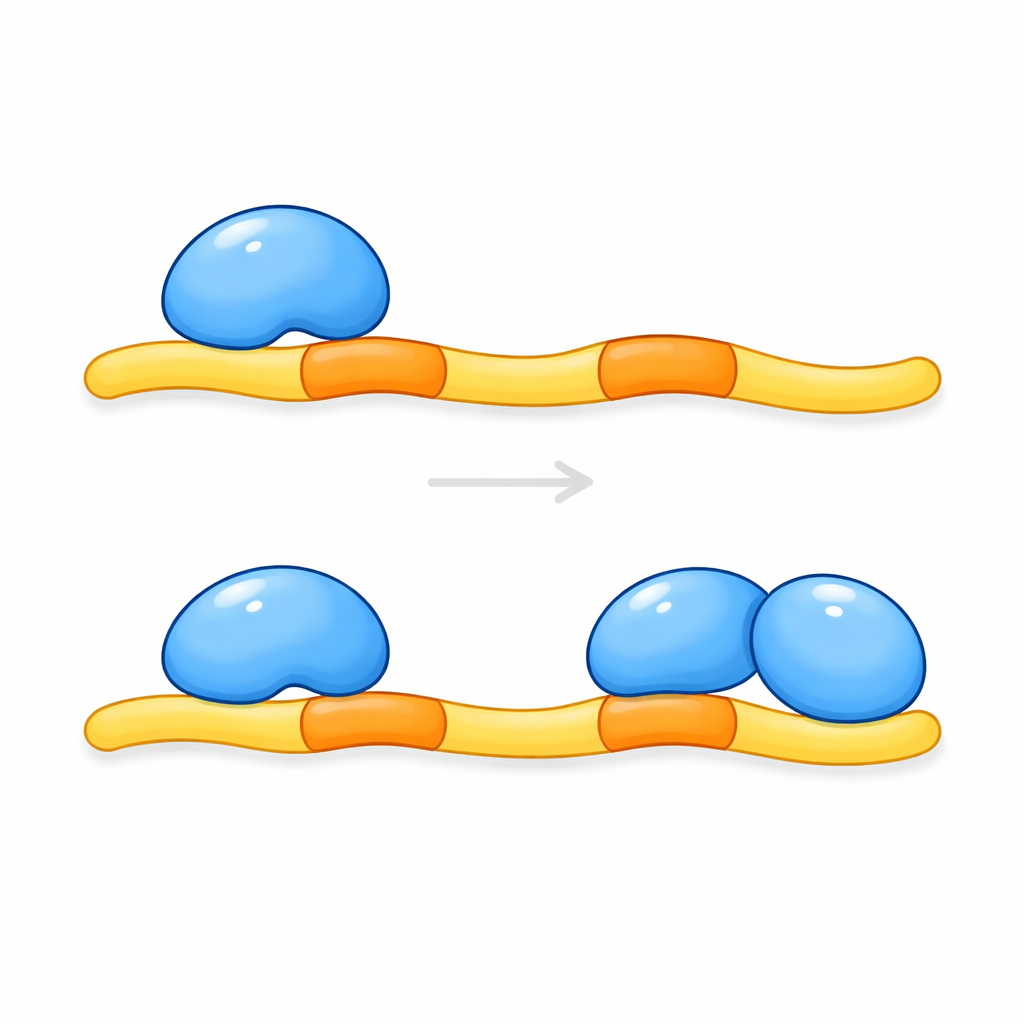
Implicações para doenças cerebrais e além
Essas descobertas mostram que KRIT1 não se limita a ligar uma molécula de CCM2; em vez disso, atua como um andaime que recruta um par de proteínas CCM2. Somente quando ambos os locais de ancoragem em KRIT1 estão ocupados o complexo consegue restringir adequadamente a produção de KLF4 e, por extensão, ajudar a prevenir o crescimento de vasos frágeis. Mutações em KRIT1 que interferem com qualquer um dos locais de ancoragem, portanto, devem enfraquecer esse grampo protetor e podem explicar algumas formas hereditárias de malformações cavernosas cerebrais. Como muitas outras proteínas humanas carregam motivos semelhantes de ancoragem gêmeos, este estudo também sugere um princípio mais amplo: a ligação dupla por pares de domínios relacionados pode ser uma maneira comum de as células ajustarem finamente as redes de sinalização. Entender essa interação tríplice pode, em última instância, orientar estratégias para estabilizar vasos sanguíneos em pessoas com risco de hemorragias cerebrais.
Citação: Huet-Calderwood, C., Fisher, O.S., Das, S. et al. Dual recruitment of two CCM2 molecules to KRIT1 suppresses KLF4 expression. Nat Commun 17, 2719 (2026). https://doi.org/10.1038/s41467-026-69595-7
Palavras-chave: malformações cavernosas cerebrais, células endoteliais, KRIT1, CCM2, KLF4