Clear Sky Science · pt
Identificação do estado da barreira hematoencefálica em gliomas sem contraste via IA generativa de difusão e ressonância magnética sem contraste
Por que isso importa para pacientes com tumor cerebral
Pessoas com tumores cerebrais rotineiramente fazem exames de ressonância magnética, e muitas também recebem um contraste injetável para que os médicos possam avaliar se a barreira protetora do cérebro — a barreira hematoencefálica — foi comprometida. Essa informação orienta cirurgia, radioterapia e prognóstico — mas o contraste pode trazer riscos, aumenta tempo e custo, e nem sempre está disponível. Este estudo apresenta um sistema de inteligência artificial (IA) que lê exames de ressonância magnética de rotina sem contraste e recria virtualmente as imagens de contraste ausentes, permitindo que os médicos inferam o estado da barreira hematoencefálica sem injetar nenhum agente de contraste.
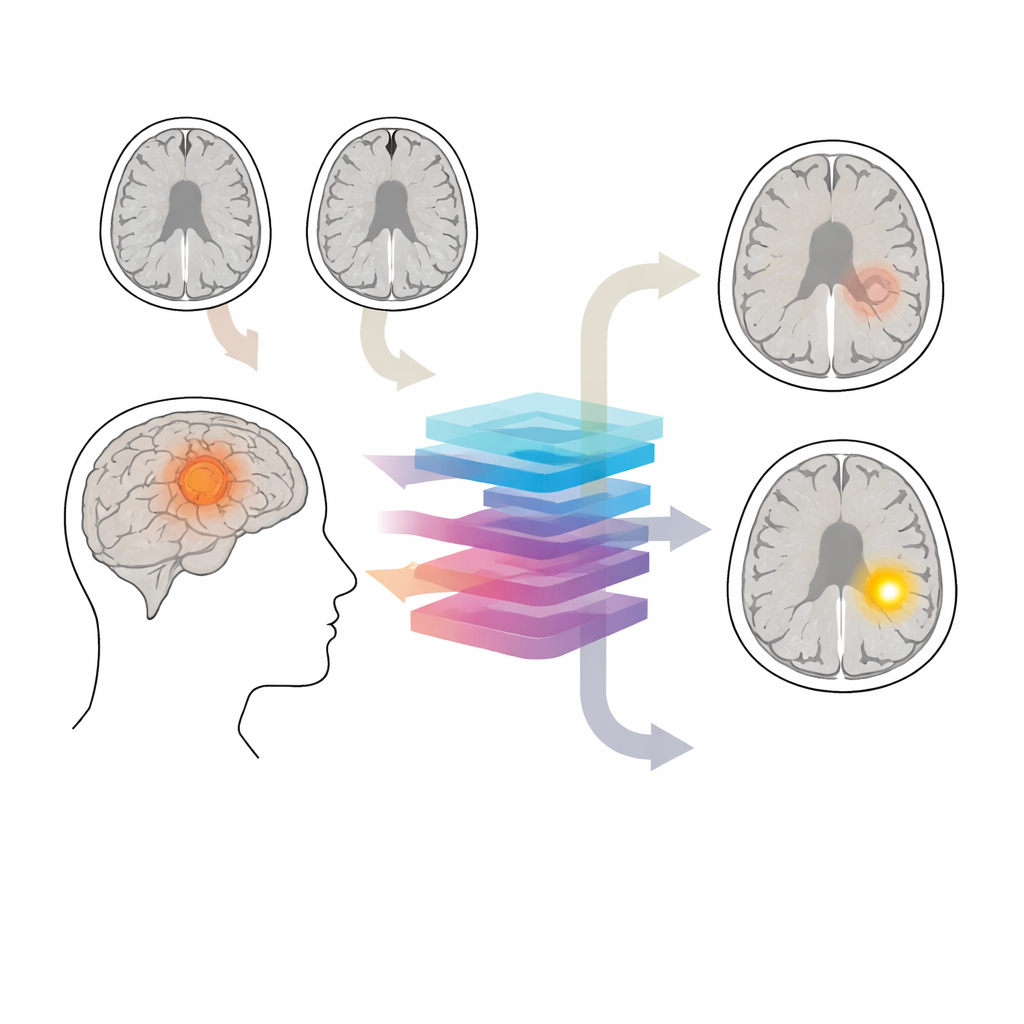
O porteiro protetor do cérebro
A barreira hematoencefálica atua como um filtro microscópico ao redor dos vasos sanguíneos no cérebro, permitindo a passagem apenas de moléculas muito pequenas. Em muitos gliomas essa barreira torna‑se permeável. Na ressonância magnética com contraste padrão, as áreas permeáveis se destacam após a injeção, enquanto as regiões íntegras permanecem escuras. Esses padrões influenciam o grau de agressividade do tratamento e ajudam a definir o que remover cirurgicamente ou visar com radiação. Ainda assim, exames com contraste às vezes são omitidos — por exemplo, em avaliações iniciais ou no acompanhamento de longo prazo de tumores de crescimento lento — e alguns pacientes devem evitar contraste por causa de doença renal, reações alérgicas ou preocupações sobre deposição de gadolínio no cérebro.
Transformando exames comuns em contraste virtual
Os autores perguntaram se exames de ressonância magnética sem contraste, que já são amplamente realizados, contêm informação sutil suficiente para que a IA inferisse o que um exame com contraste teria mostrado. Eles se concentraram em duas sequências comuns: T1 e T2‑FLAIR. Embora essas sequências não mostrem diretamente vazamento da barreira hematoencefálica, elas capturam a estrutura do tumor, o edema circundante e o dano tecidual que frequentemente acompanham a quebra da barreira. A equipe construiu um sistema chamado CBSI que primeiro gera imagens sintéticas com realce de contraste a partir desses exames sem contraste e, em seguida, usa essas imagens, junto com as originais, para decidir se a barreira está íntegra ou rompida em cada glioma.
Como o novo sistema de IA funciona
No coração do CBSI está um modelo de difusão — um tipo de IA que parte de imagens ruidosas e as “desruge” iterativamente até obter imagens realistas. Aqui, ele aprende a transformar a entrada sem contraste em duas imagens virtuais alternativas com contraste: uma assumindo barreira íntegra e outra assumindo barreira permeável. Um mecanismo de orientação informa ao modelo qual padrão de realce almejar, e uma etapa auxiliar de segmentação o ajuda a prestar atenção extra à região do tumor. Em um segundo estágio, uma rede separada compara os dois resultados sintéticos para cada paciente e julga qual deles é mais autoconsistente com os dados originais da ressonância. Essa decisão é então traduzida no estado previsto da barreira hematoencefálica.
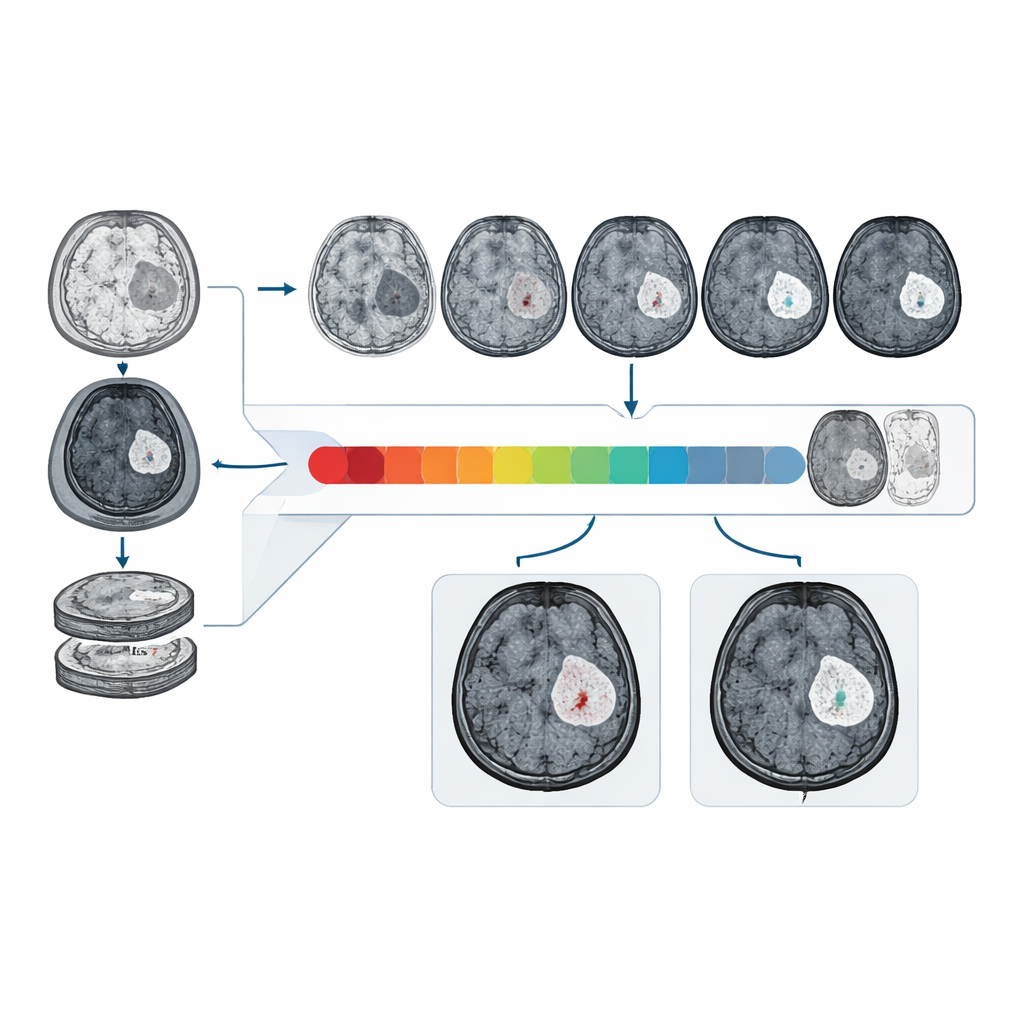
Desempenho em dados reais e diversos
Os pesquisadores treinaram e testaram o CBSI com dados de ressonância magnética de 1.535 pacientes com glioma coletados em vários hospitais e em bases de dados públicas internacionais. Em um conjunto de teste clínico externo, o CBSI distinguiu barreiras íntegras de rompidas com uma área sob a curva de cerca de 81%, claramente melhor do que modelos que dependiam apenas de imagens sem contraste e aproximando‑se do desempenho de modelos que tinham acesso a exames com contraste reais. Radiologistas, quando mostrados misturas aleatórias de imagens de contraste reais e sintéticas do sistema, consideraram mais de 90% das imagens sintéticas de alta qualidade diagnóstica, e sua habilidade de identificar realce de contraste nas imagens sintéticas foi semelhante à observada em exames reais.
Benefícios para planejamento do tratamento e cuidados futuros
Como as imagens sintéticas com contraste produzidas pelo CBSI capturam detalhes do tumor e padrões de realce, elas também melhoraram tarefas subsequentes, como delineamento das margens tumorais e estimativa do grau do tumor — ambas fortemente dependentes do comportamento da barreira hematoencefálica. O método generalizou bem para diferentes aparelhos, protocolos de imagem e populações de pacientes, incluindo dados da África Subsaariana e coortes internacionais maiores. Embora os autores reconheçam que qualquer sistema de aprendizado profundo permanece uma ferramenta estatística, e não uma janela direta para a biologia, seus resultados sugerem que a imagem de contraste virtual poderia reduzir a dependência de agentes injetáveis, especialmente para pacientes vulneráveis ou em contextos onde exames com contraste são difíceis de obter. Em termos práticos, essa abordagem de IA poderia permitir que os médicos extraíssem informações-chave que moldam o tratamento sobre a barreira hematoencefálica a partir dos exames que os pacientes já estão realizando — sem uma picada a mais na agulha.
Citação: Zheng, K., Zhang, Y., Shu, H. et al. Contrast-free identification of glioma blood-brain barrier status via generative diffusion AI and non-contrast MRI. Nat Commun 17, 2162 (2026). https://doi.org/10.1038/s41467-026-69578-8
Palavras-chave: glioma, barreira hematoencefálica, ressonância magnética cerebral, IA em imagem médica, imagens sem contraste