Clear Sky Science · pt
IgG baseada em nanobodies inibe simultaneamente a atividade alergênica e enzimática do principal alérgeno do veneno de abelha
Por que as alergias a picadas de abelha importam
Para a maioria das pessoas, uma picada de abelha é dolorosa, mas de curta duração. Para outras, pode desencadear uma reação sistêmica com risco de vida chamada anafilaxia. O principal tratamento preventivo atual, a imunoterapia com veneno, funciona para muitos pacientes, mas leva anos, envolve injeções frequentes e pode, por si só, provocar efeitos alérgicos. Este estudo investiga uma forma nova e mais direcionada de proteger pessoas com alergia grave ao veneno de abelha, neutralizando um componente-chave do veneno antes que ele cause dano.
O principal causador de problemas no veneno de abelha
O veneno de abelha é um coquetel de diferentes moléculas, mas uma proteína, chamada fosfolipase A2 (ou Api m 1), sobressai. É o alérgeno dominante para pacientes alérgicos ao veneno de abelha e está presente em praticamente todos eles. A Api m 1 tem um duplo papel: danifica membranas celulares, contribuindo para dor e inflamação no local da picada, e é também um alvo principal para anticorpos que causam alergia conhecidos como IgE. Quando a Api m 1 se liga à IgE ancorada em células imunes, como mastócitos e basófilos, pode desencadear uma reação em cadeia que leva à liberação súbita de mediadores inflamatórios e, em casos graves, à anafilaxia.
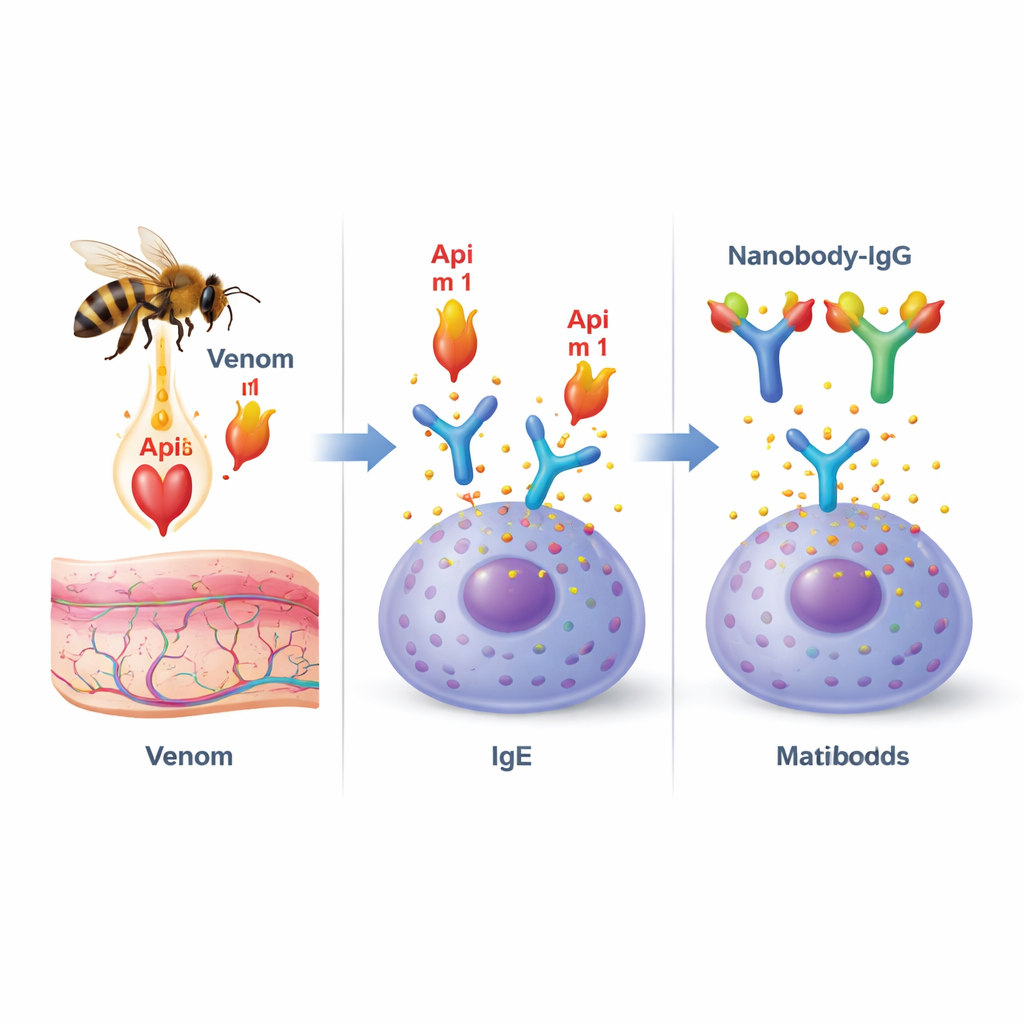
Projetando anticorpos diminutos para bloquear o alérgeno
Os pesquisadores recorreram às “nanobodies”, fragmentos de anticorpos diminutos e estáveis originalmente descobertos em camelídeos. Por serem pequenos e alongados, as nanobodies encaixam-se particularmente bem em sulcos e cavidades das proteínas. A equipe isolou nanobodies específicas para Api m 1 a partir de uma biblioteca imune e selecionou dois candidatos de destaque, denominados AM1‑1 e AM1‑4. Trabalhos estruturais detalhados usando cristalografia de raios X mostraram que essas duas nanobodies se prendem a lados opostos da Api m 1 e não interferem entre si. Uma nanobody, AM1‑1, situa‑se diretamente sobre o centro ativo da enzima, sugerindo que poderia bloquear a função de dano à membrana da Api m 1, enquanto a AM1‑4 se ancora em um bolso separado na superfície da proteína.
Transformando nanobodies em bloqueadores potentes
Para transformar esses pequenos ligantes em fármacos de longa duração, os cientistas fundiram cada nanobody à região Fc da IgG1 humana, criando moléculas maiores, semelhantes a anticorpos, com melhor estabilidade na corrente sanguínea. Eles também projetaram uma versão “biespecífica” que carrega tanto AM1‑1 quanto AM1‑4 em uma única molécula semelhante à IgG. Testes em laboratório mostraram que essas fusões nanobody‑IgG se ligam à Api m 1 com afinidade extremamente alta e, quando presentes, podem reduzir fortemente a ligação de IgE do sangue de pacientes alérgicos a abelhas à Api m 1. Em ensaios celulares, diminuíram a ativação de basófilos, as células imunes que normalmente respondem vigorosamente à Api m 1 em indivíduos alérgicos.
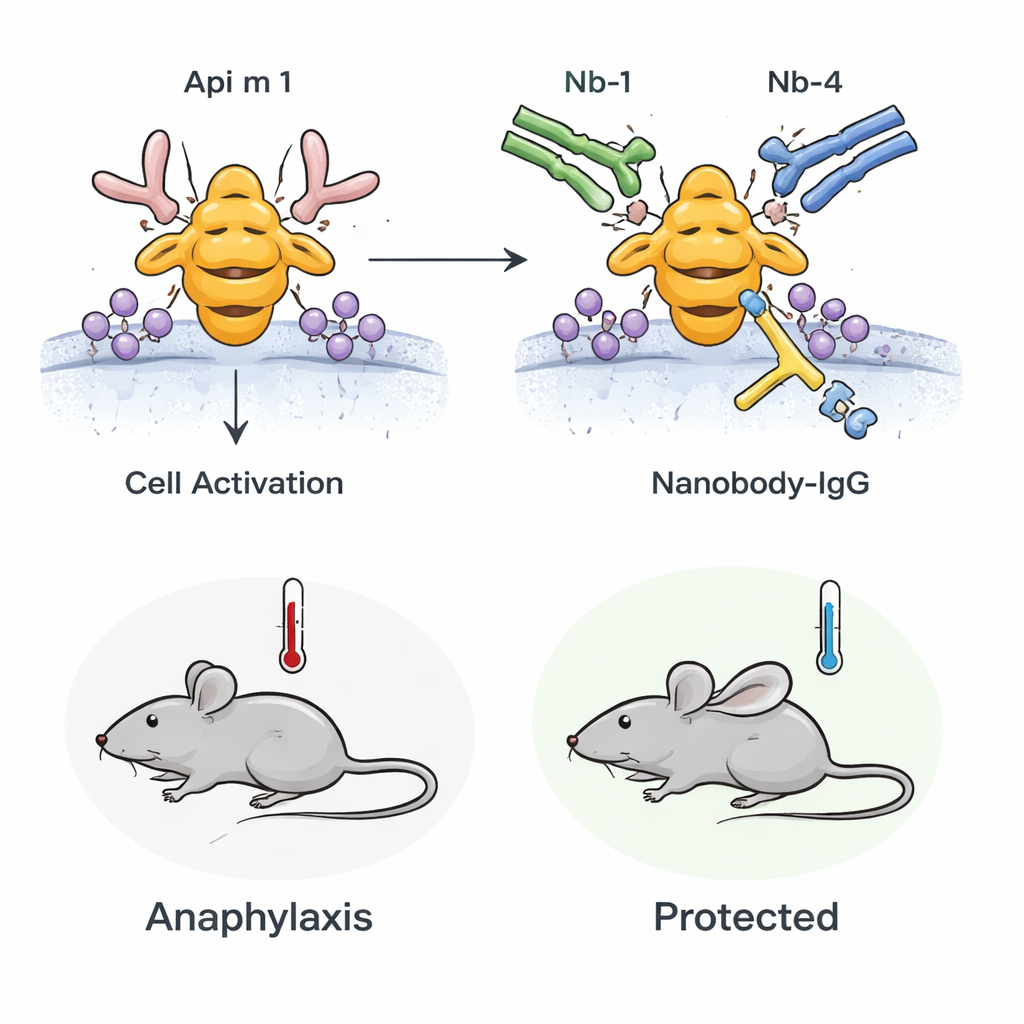
Do tubo de ensaio para animais vivos
A equipe então investigou se esse efeito bloqueador se manteria em um organismo vivo. Eles usaram camundongos sensibilizados ao veneno de abelha para que seus sistemas imunes reagissem à Api m 1 de maneira que imita a alergia humana. Quando esses camundongos foram desafiados com Api m 1, desenvolveram sinais de anafilaxia, incluindo queda na temperatura corporal e marcadores de ativação de mastócitos no sangue. Entretanto, se os animais foram pré‑tratados com a nanobody‑IgG biespecífica, tanto a queda de temperatura quanto a ativação de mastócitos foram significativamente reduzidas. Isso demonstra que anticorpos bloqueadores pré‑existentes e de alta afinidade podem atenuar a reação alérgica sistêmica à Api m 1 in vivo.
O que isso pode significar para pessoas com alergia ao veneno de abelha
Em conjunto, o estudo mostra que moléculas IgG baseadas em nanobodies, cuidadosamente projetadas, podem bloquear simultaneamente as ações alergênicas e enzimáticas da Api m 1, o principal responsável pela alergia ao veneno de abelha. Para os pacientes, isso abre a possibilidade de uma imunização passiva sazonal: algumas injeções dessas proteínas durante os meses em que picadas de abelha são mais prováveis poderiam fornecer proteção temporária contra reações graves, sem o compromisso prolongado e os riscos da imunoterapia tradicional com veneno. Embora mais trabalho seja necessário para ampliar a abordagem a outros componentes do veneno e para testar segurança e eficácia em humanos, essa estratégia baseada em nanobodies oferece uma maneira precisa de proteger indivíduos vulneráveis contra picadas de abelha perigosas.
Citação: Aagaard, J.B., Gandini, R., Ballegaard, AS.R. et al. Nanobody-based IgG simultaneously inhibit the allergenic and enzymatic activity of the dominant honeybee venom allergen. Nat Commun 17, 1814 (2026). https://doi.org/10.1038/s41467-026-69572-0
Palavras-chave: alergia ao veneno de abelha, nanobodies, imunoterapia passiva, fosfolipase A2, prevenção da anafilaxia