Clear Sky Science · pt
Reconhecimento cooperativo do promotor mediado por braçadeira pela RNA polimerase poxviral e seu parceiro semelhante a TBP/TFIIB
Como um vírus reconfigura o controle gênico dentro de nossas células
Os poxvírus, que incluem o vírus historicamente responsável pela varíola, realizam toda a expressão gênica no citoplasma de nossas células, longe do centro de controle do DNA no núcleo. Para conseguir isso, eles trazem sua própria “fábrica genética” em miniatura. Este estudo revela, em detalhe atômico, como um desses vírus, o Vaccinia, liga uma onda específica de seus genes no meio da infecção, usando uma proteína inesperada em forma de braçadeira que funciona em conjunto com a máquina de cópia viral.
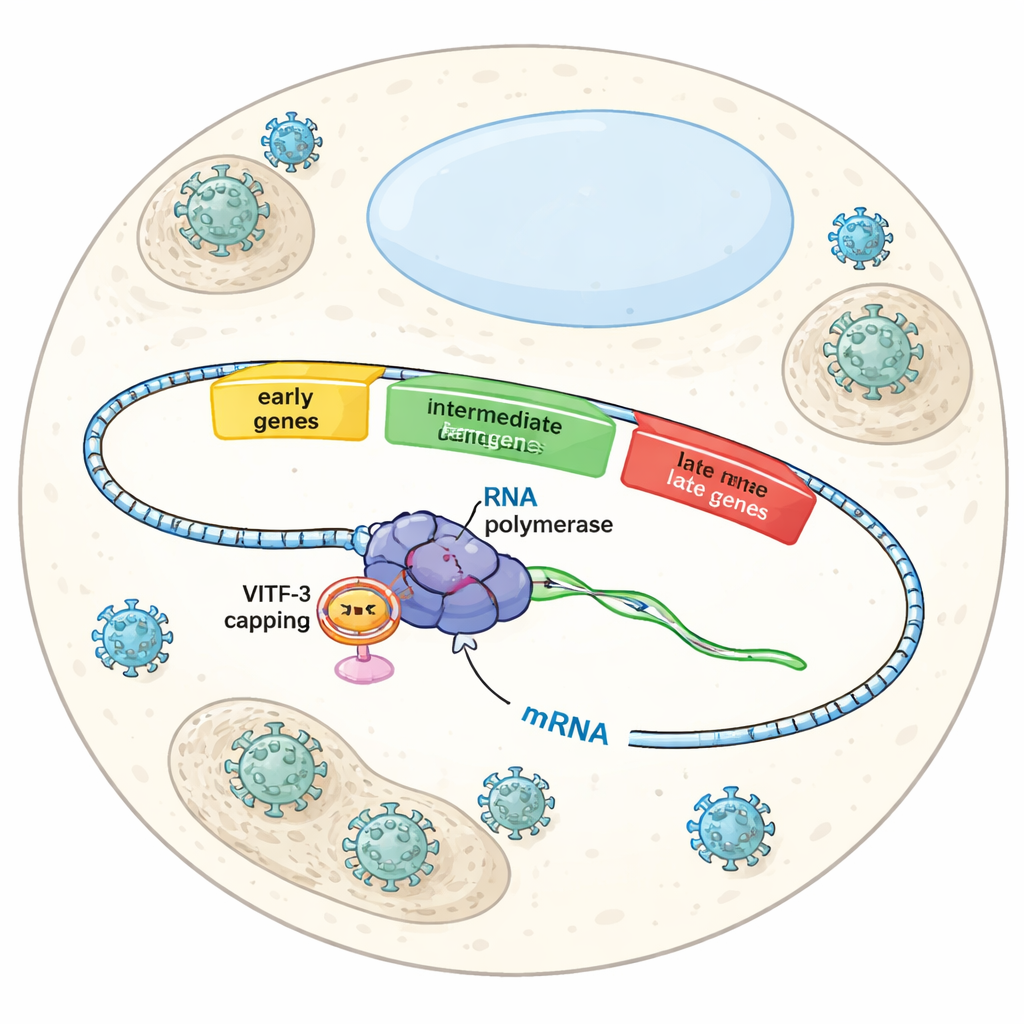
Três ondas em uma tomada viral
Quando o Vaccinia infecta uma célula, ele não ativa todos os seus genes de uma vez. Em vez disso, segue um roteiro cronometrado com genes precoces, intermediários e tardios. Genes precoces preparam o terreno para a replicação viral, genes intermediários ajudam a montar a maquinaria para fazer novas partículas virais, e genes tardios finalizam a montagem e o empacotamento. Cada onda depende da mesma RNA polimerase viral — a enzima que lê DNA para fabricar RNA — mas fatores auxiliares diferentes indicam à polimerase qual grupo de genes ativar em cada etapa. Até agora, os cientistas compreendiam razoavelmente bem o controle dos genes precoces, mas permanecia um mistério como o vírus reconhecia e ativava especificamente os genes intermediários.
Um ajudante em forma de anel que precisa de um parceiro
Os pesquisadores focalizaram uma proteína de duas partes chamada VITF‑3, conhecida por ser necessária para ativar genes intermediários. Muitos organismos, incluindo humanos, usam um par de proteínas chamado TBP e TFIIB para guiar sua RNA polimerase ao ponto correto de início no DNA. A equipe mostrou que VITF‑3 é uma versão altamente modificada desse mesmo par ancestral. Contudo, ao contrário de seus equivalentes celulares, VITF‑3 sozinho não se liga ao DNA. Em vez disso, suas duas subunidades se entrelaçam para formar um anel fechado que é, na prática, inerte em relação ao DNA a menos que a RNA polimerase viral esteja presente. Isso foi inesperado, porque na maioria dos sistemas o componente semelhante a TBP se liga primeiro ao DNA do promotor e então recruta a polimerase; aqui, o vírus parece ter reconfigurado a ordem dos eventos.
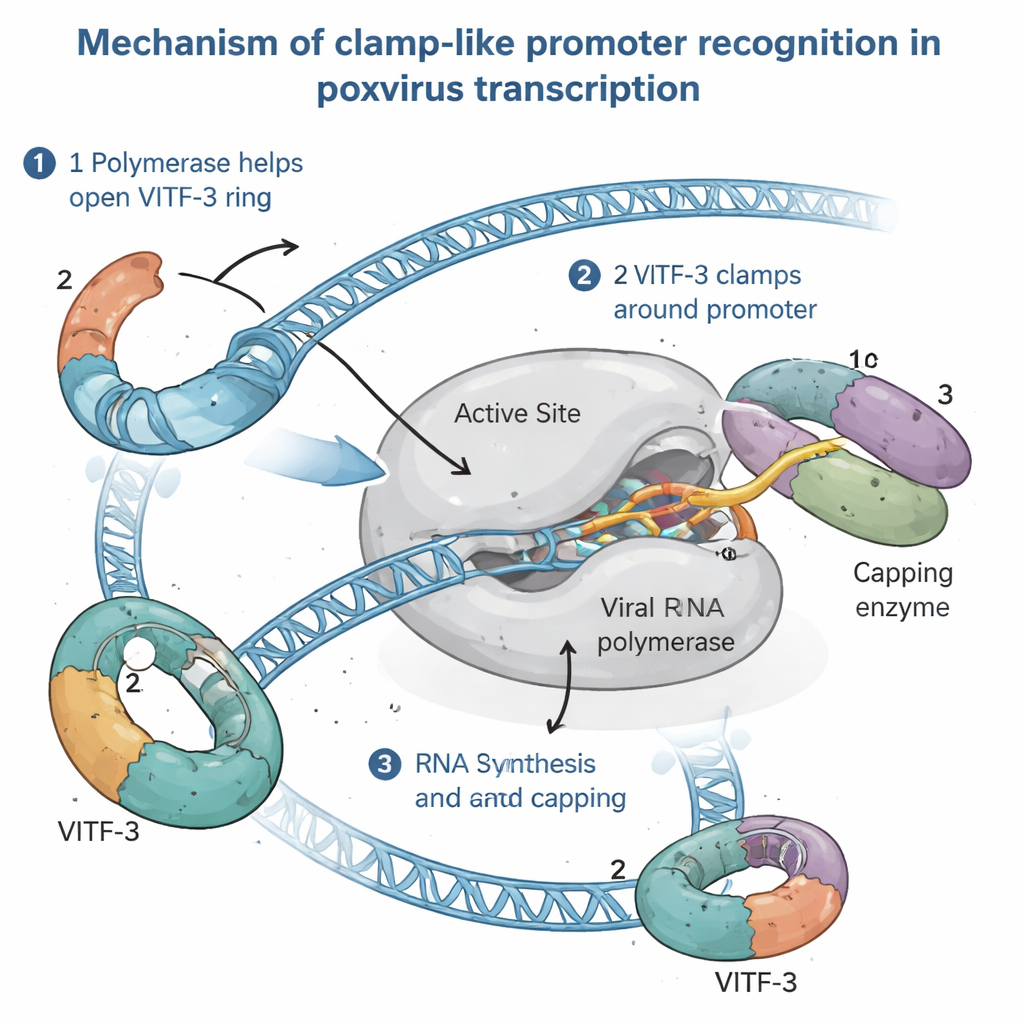
Visualizando a máquina de transcrição intermediária em ação
Para entender como essa montagem incomum funciona, os autores isolaram o complexo pré‑iniciação intermediário completo — o conjunto pronto pouco antes do início da síntese de RNA — de células humanas infectadas. Usando criomicroscopia eletrônica de alta resolução, visualizaram o complexo com detalhes de cerca de 2,4 ångström, nitidez suficiente para ver cadeias laterais de aminoácidos e bases individuais do DNA. As imagens revelaram a RNA polimerase viral agarrando o DNA do promotor, com VITF‑3 formando um anel apertado ao redor de um trecho rico em AT logo a montante do sítio de início. Esse anel dobra o DNA de forma acentuada em aproximadamente 90 graus e o direciona para uma fenda na polimerase. Ao mesmo tempo, uma enzima viral responsável por adicionar o cap protetor à extremidade 5′ do RNA viral está acoplada à polimerase, pronta para modificar os novos transcritos assim que emergirem.
Um mecanismo de carregador de braçadeira emprestado em espírito
Ao combinar imagens estruturais com testes bioquímicos, o estudo propõe que a RNA polimerase viral carrega ativamente o VITF‑3 no DNA, atuando como um “carregador de braçadeira”. Primeiro, a polimerase liga‑se a um promotor intermediário e ajuda a abrir o anel de VITF‑3. Em seguida, junto com a enzima de captação, ela fecha o anel ao redor da região rica em AT, prendendo o complexo no lugar. O DNA é derretido próximo ao sítio de início, e a polimerase lê diretamente um sinal curto de quatro letras (um motivo TAAA) que marca exatamente onde a síntese de RNA deve começar. À medida que o RNA cresce, segue o mesmo caminho ocupado por parte do VITF‑3 no complexo inicial, de modo que o RNA emergente provavelmente empurra o VITF‑3 para fora do caminho, permitindo que a polimerase saia do promotor e continue ao longo do gene, enquanto o VITF‑3 pode ficar para trás para acelerar o reuso do mesmo promotor.
O que isso significa para entender e direcionar poxvírus
Em termos simples, este trabalho mostra que o vírus Vaccinia reaproveitou um módulo universal de controle gênico em uma braçadeira que só se prende ao DNA quando sua própria RNA polimerase o instrui. Essa reviravolta engenhosa permite ao vírus usar uma enzima central para executar três programas de transcrição muito diferentes, simplesmente trocando fatores auxiliares específicos de cada estágio. Como esse tipo de fator é conservado em muitos poxvírus, incluindo patógenos humanos, o mecanismo recém‑revelado de carregamento de braçadeira e o anel único do VITF‑3 oferecem alvos estruturais concretos para estratégias antivirais destinadas a interromper a capacidade do vírus de cronometrar e controlar seus genes durante a infecção.
Citação: Jungwirth, S., Bartuli, J., Lamer, S. et al. Cooperative clamp-mediated promoter recognition by poxviral RNA polymerase and its TBP/TFIIB-like partner. Nat Commun 17, 1648 (2026). https://doi.org/10.1038/s41467-026-69571-1
Palavras-chave: transcrição de poxvírus, Vírus Vaccinia, RNA polimerase, reconhecimento de promotor, fatores de transcrição