Clear Sky Science · pt
Terapia térmica intersticial por laser e pembrolizumabe adjuvante em astrocitoma de alto grau recorrente: um ensaio Fase 1/Fase 2b randomizado
Por que este estudo sobre câncer cerebral é importante
O astrocitoma de alto grau recorrente, incluindo o glioblastoma, está entre os cânceres cerebrais mais letais, e os tratamentos atuais raramente conseguem controlar a doença por muito tempo. Este estudo testa uma estratégia em duas etapas que usa calor de um laser para destruir o tecido tumoral e abrir as defesas do cérebro, seguida por um fármaco imunológico que ajuda os próprios linfócitos T do corpo a atacar qualquer câncer remanescente. Para pacientes e famílias que enfrentam esse diagnóstico, o trabalho investiga se um procedimento minimamente invasivo pode transformar um câncer quase refratário em um que finalmente responde à imunoterapia.
Uma nova forma de enfrentar tumores cerebrais persistentes
Os pacientes deste ensaio apresentavam astrocitomas de alto grau recidivantes após a terapia padrão, que normalmente inclui cirurgia, radioterapia e quimioterapia. Os pesquisadores se concentraram em duas ferramentas. A primeira, terapia térmica intersticial por laser (LITT), é um procedimento por porta de entrada no qual uma sonda fina é guiada por ressonância magnética até o tumor e usada para aquecer e destruir o tecido canceroso, poupando grande parte do cérebro circundante. A segunda ferramenta é o pembrolizumabe, um fármaco de imunoterapia amplamente utilizado que bloqueia o PD-1, um “freio” molecular que frequentemente impede os linfócitos T de atacarem os tumores. Tentativas anteriores de usar esses medicamentos isoladamente nesses cânceres cerebrais foram decepcionantes. A equipe, portanto, questionou se usar primeiro o laser poderia preparar o tumor e o sistema imunológico para responder melhor ao pembrolizumabe. 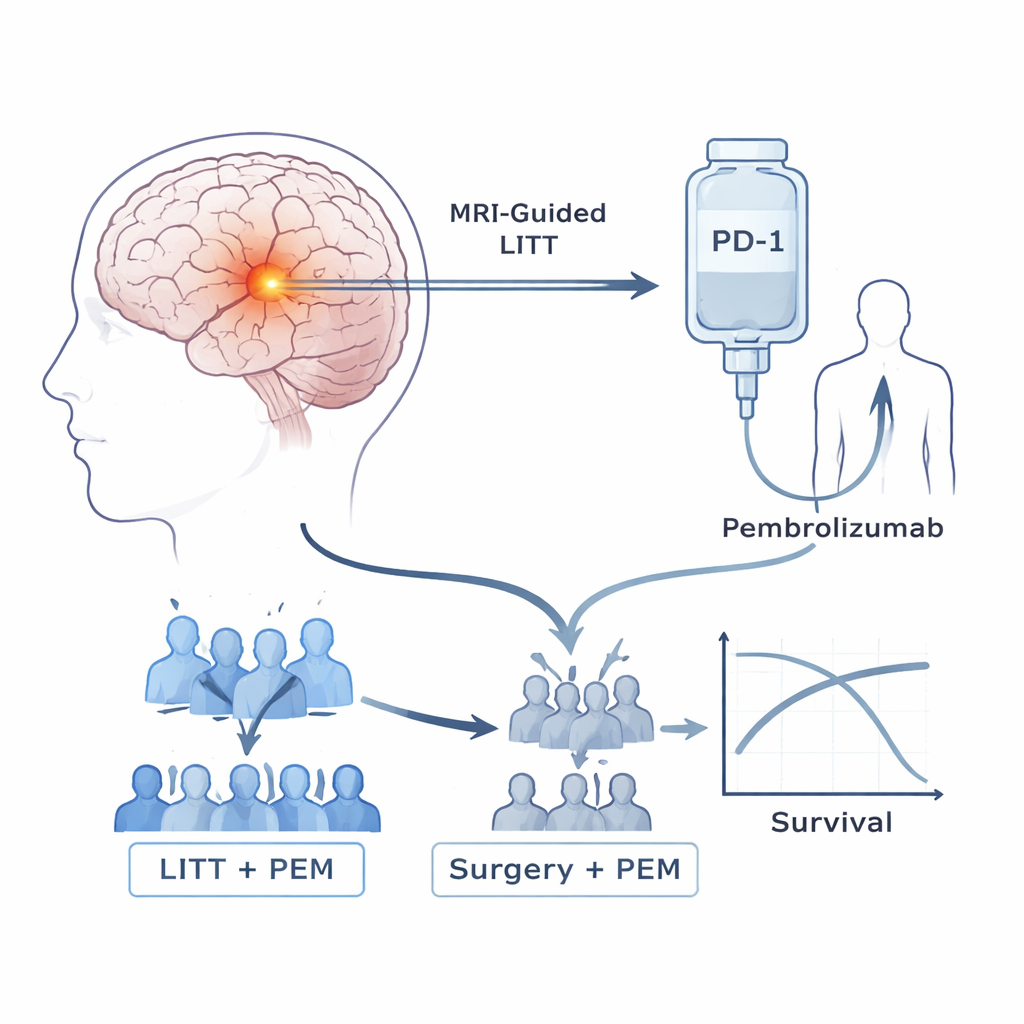
Como o ensaio clínico foi conduzido
O estudo começou com uma pequena fase de segurança, demonstrando que os pacientes podiam receber pembrolizumabe a cada três semanas após LITT com segurança, sem efeitos adversos limitantes de dose. Em seguida, passou para um ensaio de Fase 2b. Inicialmente, os pacientes foram randomizados para um de dois grupos: LITT seguido de pembrolizumabe, ou cirurgia cerebral repetida convencional sem laser, seguida de pembrolizumabe. À medida que evidências externas aumentaram indicando que cirurgia mais imunoterapia oferecia pouco benefício por si só, um comitê independente revisou os resultados iniciais deste ensaio. Ao observar sinais de que o grupo sem laser estava se saindo mal enquanto o grupo LITT parecia viver mais, interromperam a randomização adicional, e todos os pacientes posteriores receberam a combinação laser mais fármaco.
O que aconteceu com a sobrevida e o controle tumoral
Entre 39 pacientes que receberam o tratamento conforme planejado, aqueles tratados com LITT mais pembrolizumabe viveram notavelmente mais do que os que fizeram cirurgia mais pembrolizumabe. A sobrevida global mediana foi de cerca de 11,8 meses com a abordagem combinada LITT, contra 5,2 meses com cirurgia isolada, e nenhum dos pacientes operados estava vivo aos 18 meses, em comparação com 42% daqueles no grupo LITT. O tempo até a progressão tumoral também melhorou, de 1,6 mês no grupo cirúrgico para 4,5 meses com LITT. Cerca de 27% dos pacientes tratados com LITT tiveram redução mensurável dos tumores e 70% alcançaram pelo menos um controle temporário da doença, enquanto todos os pacientes que fizeram cirurgia sem laser seguida de pembrolizumabe apresentaram progressão. Os efeitos adversos da terapia combinada foram em sua maioria leves e manejáveis, com alguns casos de diarreia, fraqueza muscular e elevação de enzimas hepáticas, mas sem mortes relacionadas ao tratamento.
O que o sistema imune estava fazendo
Para entender por que a combinação poderia funcionar, os cientistas examinaram minuciosamente as células sanguíneas ao longo do tempo usando sequenciamento de RNA de célula única e rastreamento do receptor de células T. Após o LITT, observaram um grupo específico de células imunes inatas, chamadas monócitos não clássicos, mudarem para um estado mais ativo ligado à migração, inflamação e interação com linfócitos T — alterações não vistas após a cirurgia padrão. Quando o pembrolizumabe foi então iniciado, pacientes com sobrevida mais longa mostraram fortes ondas de ativação de linfócitos T CD8 e expansão clonal, o que significa que muitos linfócitos T idênticos direcionados aos mesmos antígenos estavam se multiplicando. Esses linfócitos tendiam a migrar para estados de memória e efetores capazes de reconhecer e matar células tumorais, em vez de se tornarem exauridos e ineficazes. Sobreviventes a longo prazo também apresentaram redução de IDO-1, uma molécula associada à supressão imune, sugerindo que a combinação pode aliviar múltiplas camadas de freios imunológicos. 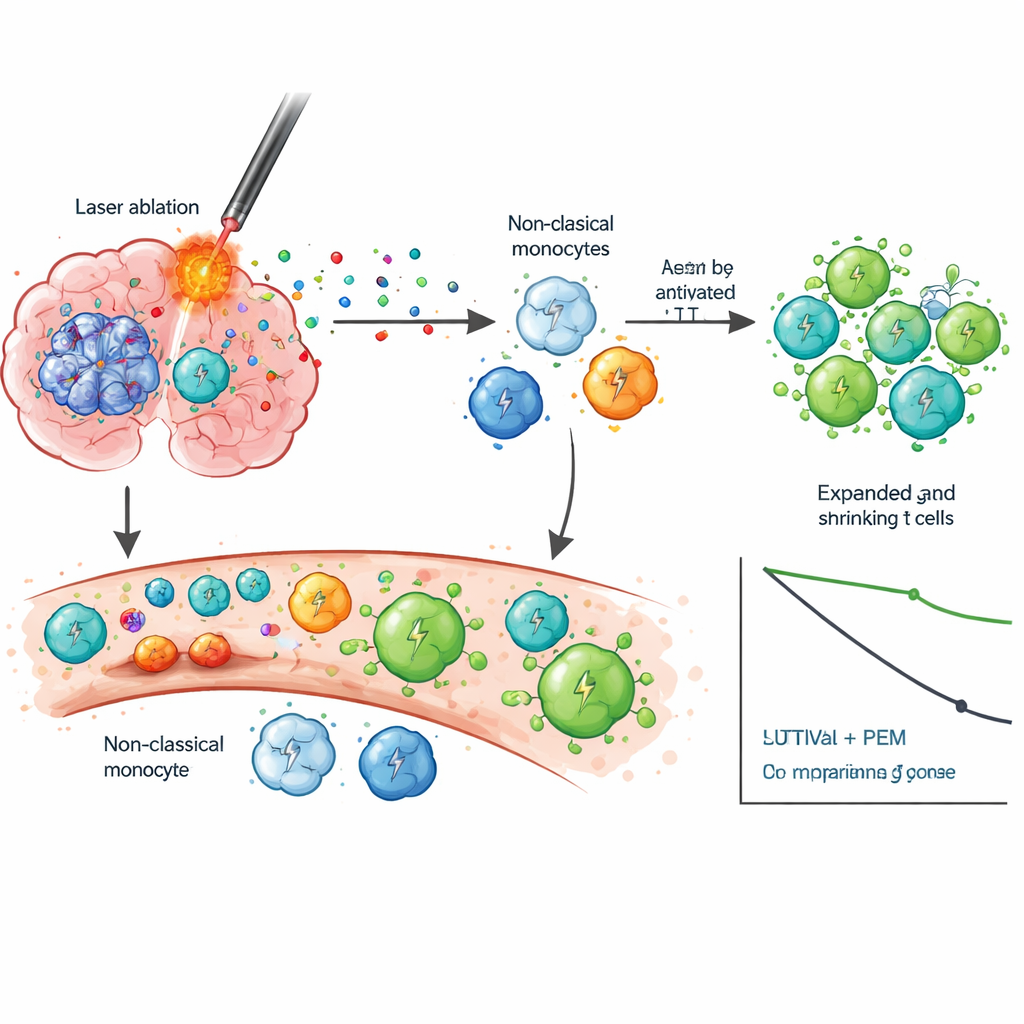
O que isso pode significar para os pacientes
Para pessoas vivendo com astrocitoma de alto grau recorrente, este trabalho sugere que usar ablação a laser guiada por RM para reduzir o volume tumoral, afrouxar temporariamente a barreira hematoencefálica e liberar fragmentos tumorais na circulação pode preparar o terreno para que a imunoterapia funcione onde normalmente falha. Ao acionar um “sinal” para o sistema imune e então remover o freio PD-1 com pembrolizumabe, a combinação parece gerar respostas de linfócitos T mais duradouras e estender a sobrevida em um câncer com poucas opções. Como o estudo foi relativamente pequeno e a randomização terminou precocemente, os autores enfatizam que são necessários ensaios maiores e totalmente controlados. Ainda assim, os resultados apontam para uma estratégia promissora: parear destruição física precisa do tumor com fármacos imunes para transformar um tumor cerebral frio e resistente em um que o corpo finalmente consiga reconhecer e combater.
Citação: Campian, J.L., Le, S.B., Ghiaseddin, A. et al. Laser interstitial thermal therapy and adjuvant pembrolizumab in recurrent high-grade astrocytoma: a Phase 1/randomized Phase 2b trial. Nat Commun 17, 1763 (2026). https://doi.org/10.1038/s41467-026-69522-w
Palavras-chave: glioblastoma, ablação a laser, pembrolizumabe, imunoterapia, tumor cerebral