Clear Sky Science · pt
Sinalização excessiva de FGFR3 na acondroplasia prejudica a renovação de condrócitos da zona de repouso via sinalização CREB
Por que este estudo sobre crescimento ósseo é importante
A acondroplasia é a causa genética mais comum de nanismo com membros curtos. Ela afeta não só a altura, mas também a saúde da coluna, a mobilidade e a qualidade de vida. Tratamentos atuais ajudam, mas não restauram completamente o crescimento ósseo. Este estudo usa um modelo murino sofisticado para revelar uma zona problemática anteriormente negligenciada em ossos em crescimento e aponta para um novo interruptor de sinalização, chamado CREB, como um alvo promissor para terapias futuras.
Como ossos saudáveis crescem em comprimento
Ossos longos, como o fêmur na coxa, alongam-se nas placas de crescimento próximas às suas extremidades. Essas placas estão organizadas em três camadas principais de células cartilaginosas. No topo fica a zona de repouso, onde as células se comportam como um reservatório de células-tronco, dividindo-se lentamente e enviando células filhas para baixo. Abaixo dela, a zona proliferativa contém células que se dividem rapidamente, empilhadas em colunas ordenadas que impulsionam o alongamento. Mais adiante, a zona hipertrofia abriga células maduras e aumentadas que ajudam a orientar a formação do novo osso. O equilíbrio entre essas zonas mantém o crescimento ósseo na taxa e forma corretos.
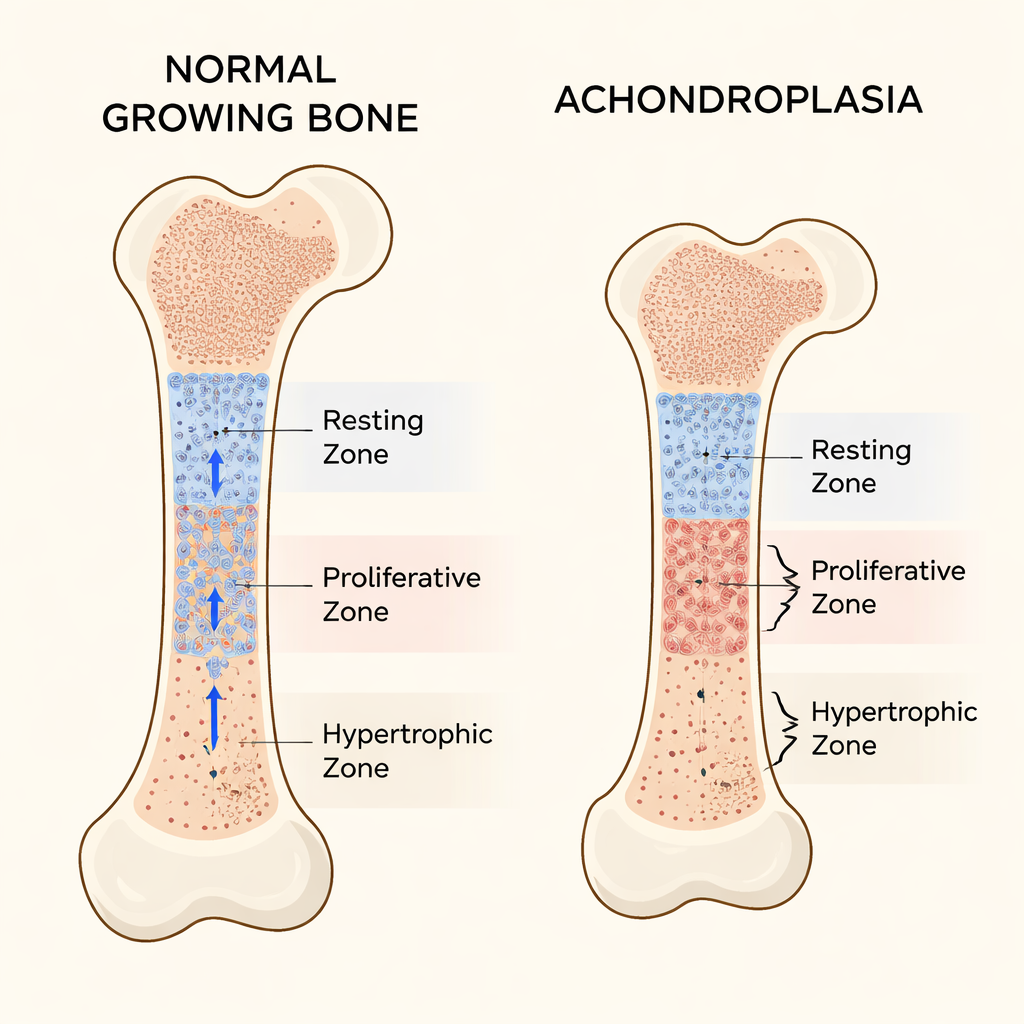
O que dá errado na acondroplasia
Na maioria das pessoas com acondroplasia, uma única mutação no gene FGFR3 torna seu receptor hiperativo, freando o crescimento ósseo. Trabalhos anteriores mostraram que essa sinalização desacelera a divisão celular na zona proliferativa e bloqueia a ampliação final das células na zona hipertrofia. Usando camundongos geneticamente modificados para carregar a mutação humana de acondroplasia, os autores confirmaram membros severamente curtos e placas de crescimento encurtadas. Mas medições cuidadosas revelaram algo que vinha sendo em grande parte negligenciado: a própria zona de repouso tornou-se anormalmente espessa. Em vez de atuar como um reservatório estável e bem comportado de células-tronco, essa região expandiu-se e continha células pobres na matriz cartilaginosa normal.
As células da zona de repouso perdem seu comportamento "semelhante a tronco"
Para entender essa expansão, a equipe rastreou como as células da placa de crescimento se dividiam e se moviam ao longo do tempo. Em camundongos normais, as células da zona de repouso dividiam-se raramente, e suas descendentes migravam para baixo em colunas retas para repor a zona proliferativa. Nos camundongos mutantes, muitas mais células na zona de repouso dividiram-se lentamente e permaneceram no lugar, acumulando uma camada congestionada que não alimentava adequadamente as zonas inferiores. Rastreamento de linhagem com marcadores genéticos multicoloridos mostrou que as colunas clonais eram curtas e desorganizadas, com células filhas vagando em direções aleatórias em vez de formar pilhas ordenadas. Marcadores de identidade semelhante a células-tronco, como a proteína CD73, foram perdidos na zona de repouso expandida, sugerindo que o FGFR3 hiperativo havia corrompido o nicho normal de células-tronco.
Um novo culpado na sinalização: CREB
Em seguida, os pesquisadores usaram RNA-seq de célula única para perfilar milhares de células individuais da placa de crescimento. Identificaram um aglomerado distinto que correspondia à zona de repouso expandida e era rico em um gene chamado Spon1, entre outros. A análise de vias destacou a ativação de CREB, uma proteína que ativa genes quando é fosforilada. Microscopia mostrou que células da zona de repouso nos camundongos mutantes expressavam fortemente CREB ativado e seu coativador CBP, junto com altos níveis de FGFR3 e moléculas a jusante como STAT5. Em cultura celular, estimular a via FGFR3 aumentou a atividade de CREB e elevou SPONDIN1 (a proteína SPON1), enquanto bloquear FGFR3 ou CREB reduziu esses sinais. Isso posicionou o CREB como um elo-chave entre o receptor hiperativo na superfície celular e o comportamento defeituoso das células da zona de repouso.
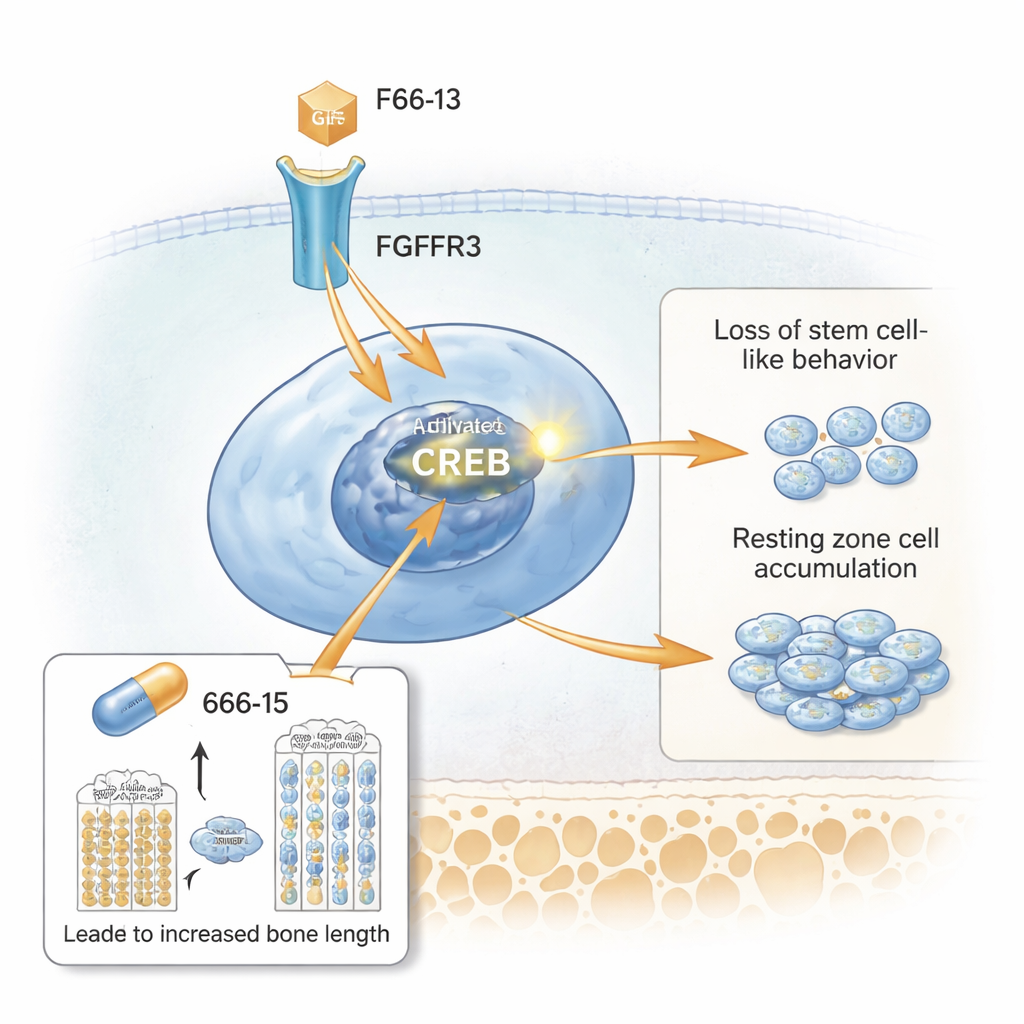
Testando um fármaco que reduz o CREB
Por fim, a equipe perguntou se reduzir o CREB poderia aliviar os problemas de crescimento. Eles trataram camundongos modelo de acondroplasia com um inibidor de CREB de pequena molécula, chamado 666-15, durante o período de rápido crescimento após o nascimento. Em comparação com camundongos mutantes não tratados, os animais que receberam 666-15 tinham maior peso corporal e fêmures mais longos. Suas placas de crescimento pareciam mais normais: a zona de repouso afinou, as zonas proliferativa e hipertrofia recuperaram altura e proteínas da matriz cartilaginosa reapareceram. Marcadores de sinalização CREB hiperativa, incluindo fosfo-CREB, SPONDIN1 e STAT5, diminuíram na zona de repouso, enquanto o marcador semelhante a célula-tronco CD73 retornou. Importante, o mesmo fármaco teve pouco efeito em camundongos controles saudáveis na dose testada, sugerindo que age principalmente quando o CREB está anormalmente elevado.
O que isso significa para tratamentos futuros
O estudo mostra que, na acondroplasia, o FGFR3 hiperativo faz mais do que desacelerar células que se dividem e se ampliam; ele também desvia a zona de repouso, silenciosa e semelhante a célula-tronco, ativando o CREB. Essa disrupção priva as camadas inferiores da placa de crescimento de novas células e contribui para ossos curtos. Drogas existentes como o vosorotide atuam principalmente em outras vias nas zonas proliferativa e hipertrofia e restauram apenas parcialmente o comprimento ósseo. Ao adicionar o CREB à lista de alvos — especialmente na zona de repouso — terapias combinadas futuras podem normalizar mais plenamente o crescimento em crianças com acondroplasia.
Citação: Horike, N., Oura, S., Koyamatsu, S. et al. Excess FGFR3 signaling in achondroplasia disrupts turnover of resting zone chondrocytes via CREB signaling. Nat Commun 17, 1856 (2026). https://doi.org/10.1038/s41467-026-69507-9
Palavras-chave: acondroplasia, FGFR3, placa de crescimento, células-tronco da cartilagem, sinalização CREB