Clear Sky Science · pt
Densidade de carga do metal hidratado como um descritor universal que explica variações mecanísticas na ativação do periodato para degradação de poluentes
Limpeza da água com química inteligente
Muitos medicamentos e produtos químicos industriais escapam às estações convencionais de tratamento de água e acabam em rios e na água potável. Este estudo explora uma via promissora para degradar esses poluentes persistentes usando um agente oxidante comum, o periodato, e mostra que uma propriedade simples dos íons metálicos em água pode prever quão bem — e quão seguramente — essa química funcionará. Compreender essa regra pode ajudar engenheiros a projetar sistemas de tratamento mais limpos e eficientes para águas diversas do mundo real.
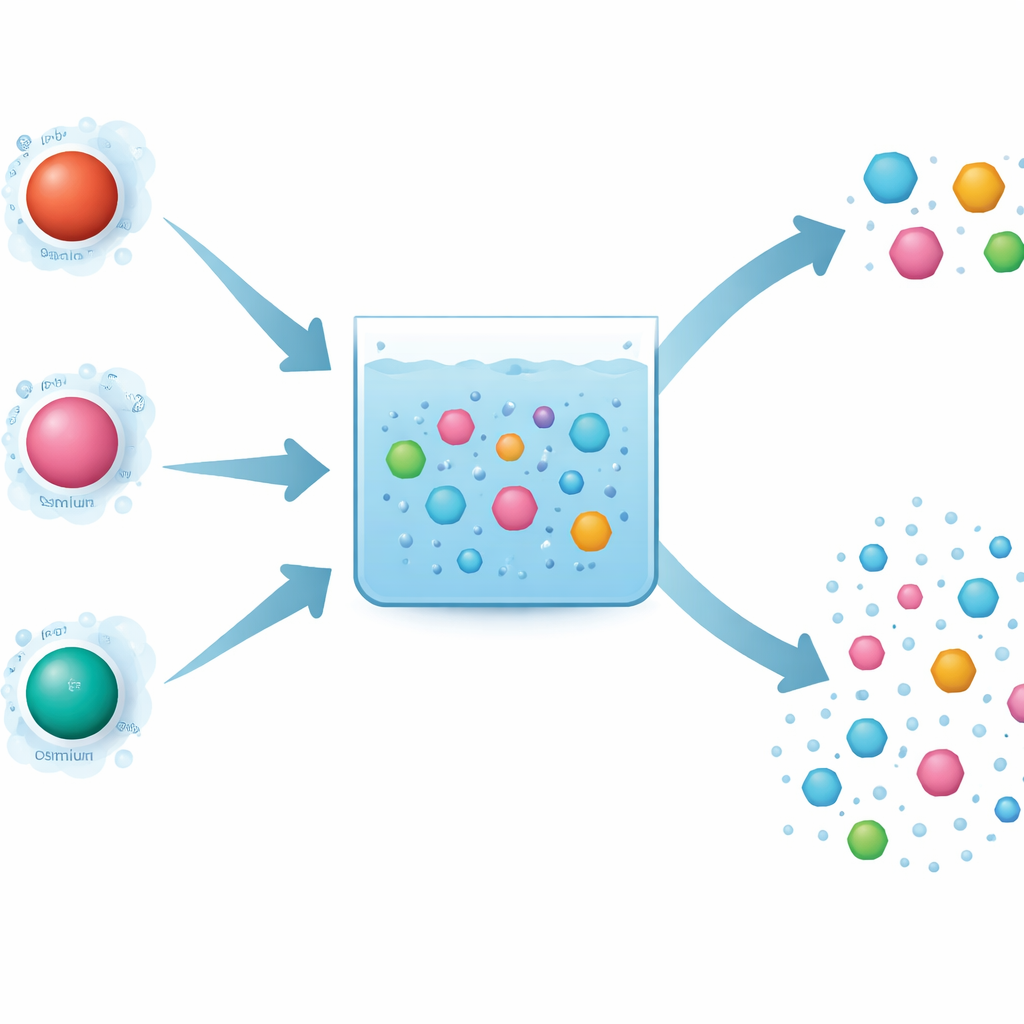
Por que a escolha do metal importa para a degradação de poluentes
Processos avançados de oxidação usam espécies reativas poderosas para fragmentar moléculas orgânicas. O periodato é um desses oxidantes e pode ser “ativado” por íons metálicos dissolvidos. Os autores compararam três metais intimamente relacionados — ferro, rutênio e ósmio — que pertencem à mesma coluna da tabela periódica e que poderiam ser esperados comportar‑se de maneira semelhante. Todos os três podem ativar o periodato e ajudar a destruir um poluente‑teste farmacêutico, a carbamazepina. Ainda assim, os experimentos mostraram diferenças marcantes: o rutênio foi extremamente rápido, o ferro foi mais lento e o ósmio ficou entre os dois. Mais intrigante, o ósmio removeu uma ampla variedade de poluentes com pouca preferência, enquanto o ferro e o rutênio foram seletivos, atacando algumas substâncias muito mais prontamente do que outras.
Dois caminhos químicos muito diferentes
Para descobrir o que estava por trás dessas diferenças, a equipe acompanhou quais espécies oxidantes de vida curta apareceram em cada sistema metal–periodato. Com ferro e rutênio, os protagonistas dominantes foram unidades “metal–oxigênio” que atuam como ferramentas de precisão, transferindo diretamente um átomo de oxigênio para sítios específicos de um poluente. Esses caminhos tenderam a formar produtos epóxi — estruturas em anel que adicionam um único átomo de oxigênio — indicando que a reação é bastante seletiva. No sistema com ósmio, entretanto, os agentes principais foram radicais hidroxila, fragmentos extremamente reativos que atacam quase qualquer molécula orgânica próxima, levando a produtos hidroxilados e pequenos fragmentos com anéis abertos. Testes com sondas químicas e espectroscopia de armadilhamento de spin confirmaram que radicais hidroxila e espécies reativas de oxigênio relacionadas, e não unidades oxigênio–ósmio de alto estado de oxidação, conduzem a maior parte da destruição de poluentes quando o ósmio está presente.
Como as condições da água moldam as reações
A equipe também examinou como o pH e os componentes naturais da água influenciam esses processos. Para o ósmio, a remoção de poluentes tornou‑se mais intensa à medida que a água se tornava mais alcalina, quando a coordenação de ânions hidróxido extras em torno do metal facilita o movimento de elétrons e a formação de radicais. Em doses altas de metal ou oxidante, no entanto, o sistema com ósmio se “auto‑extinguiu”, pois os radicais recém‑formados foram consumidos por excesso de reagentes em vez de pelos poluentes. A matéria orgânica natural, que geralmente interfere em reações de oxidação, teve surpreendentemente pouco impacto na degradação promovida pelo ósmio, sugerindo que a via radicalar permanece robusta em águas realistas. Em contraste, ferro e rutênio funcionaram melhor em condições ácidas, e a matéria orgânica natural suprimiu fortemente sua atividade ao sequestrar os importantes oxidantes metal–oxigênio.
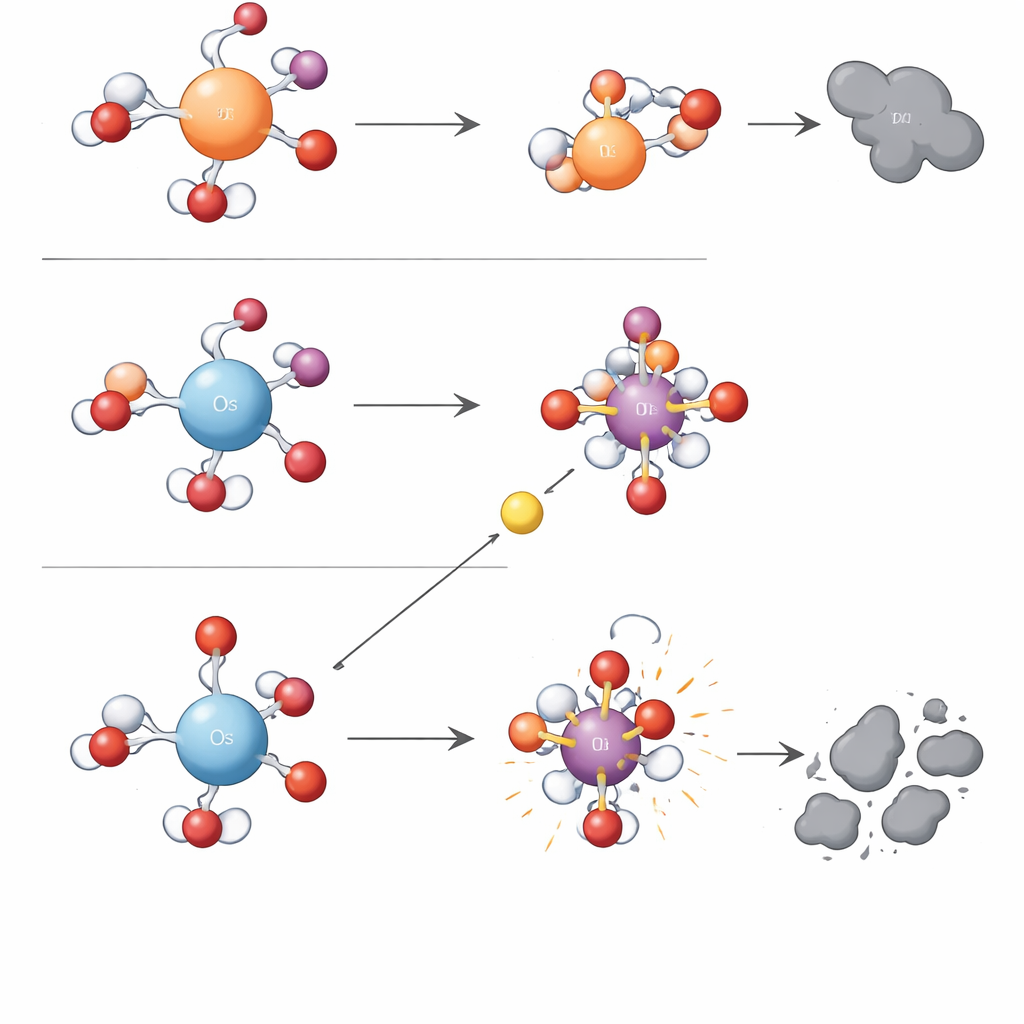
Uma regra simples de carga por trás de uma química complexa
Para ir além do método tentativa‑e‑erro, os pesquisadores recorreram a cálculos quântico‑químicos. Eles descobriram que uma única característica eletrônica — a densidade de carga positiva no centro metálico hidratado — podia explicar a divisão entre os dois tipos de reação. O ósmio em água carrega uma carga positiva mais concentrada do que o ferro ou o rutênio. Esse centro positivamente intenso prende firmemente seu átomo de oxigênio ligado, tornando sua unidade metal–oxigênio estável, porém lenta para transferência direta de oxigênio. Ao mesmo tempo, a forte atração sobre a água e íons vizinhos reduz a barreira energética para etapas de um elétron que, em última análise, rompem uma ligação de oxigênio no periodato e liberam radicais hidroxila. Metais com densidade de carga mais baixa, como ferro e rutênio, mantêm os elétrons de forma diferente, favorecendo a formação e o uso de oxidantes seletivos metal–oxigênio em vez de radicais livres. Os autores chamam essa ideia organizadora de “Mecanismo de Controle por Densidade de Carga” e mostram que ela também racionaliza tendências relatadas para outros metais, como o manganês.
Projetando tratamento de água melhor a partir de um único ajuste
Ao ligar um conjunto complexo de observações a um descritor simples — a densidade de carga de um metal cercado por água — este trabalho oferece um roteiro para ajustar processos avançados de oxidação. Metais de alta densidade de carga devem favorecer a degradação ampla baseada em radicais de misturas complexas de poluentes, especialmente em águas alcalinas ou ricas em matéria orgânica. Metais de menor densidade de carga são mais adequados quando se deseja oxidação seletiva e mais suave, por exemplo para transformar contaminantes específicos sem reagir excessivamente com todo o resto presente. Em termos práticos, isso significa que químicos e engenheiros podem selecionar ou projetar catalisadores para purificação de água ajustando o quão firmemente os centros metálicos retêm carga em seu ambiente aquoso, em vez de otimizar cada sistema apenas por tentativa.
Citação: Qian, Y., Sun, Y., Xu, J. et al. Hydrated metal charge density as a universal descriptor explaining mechanistic variations in periodate activation toward pollutant degradation. Nat Commun 17, 2683 (2026). https://doi.org/10.1038/s41467-026-69496-9
Palavras-chave: processos avançados de oxidação, ativação do periodato, tratamento de água, catálise por metais de transição, radicais hidroxila