Clear Sky Science · pt
Fluxo de trabalho de proteômica química de alto rendimento para mapear a dinâmica da citrulinização de proteínas
Por que alterar os blocos de construção das proteínas importa
Nossas células ajustam constantemente o comportamento das proteínas ao adicionar pequenas modificações químicas depois de serem sintetizadas. Uma dessas alterações, chamada citrulinização, muda sutilmente a carga de um aminoácido comum e pode remodelar o dobramento das proteínas, a interação com o DNA ou a ligação com outras moléculas. Essas pequenas edições estão cada vez mais associadas a doenças autoimunes, infecções, câncer e função cerebral — mas são notoriamente difíceis de detectar. Este estudo apresenta um fluxo de trabalho laboratorial de alto rendimento que finalmente torna possível mapear a citrulinização em milhares de proteínas, revelando quando e onde ela aparece em tecidos e células imunes.
Um interruptor oculto nas proteínas
A citrulinização ocorre quando enzimas chamadas PADs modificam quimicamente o aminoácido arginina, removendo sua carga positiva. Essa mudança aparentemente pequena pode afrouxar o empacotamento do DNA, alterar a rigidez de proteínas estruturais ou modificar a forma como o sistema imune reconhece nossos próprios tecidos. A citrulinização anômala tem sido implicada em artrite reumatoide, distúrbios neurodegenerativos, infecções virais e câncer. No entanto, proteínas citrulinizadas são raras e facilmente confundidas com outras modificações mais comuns, por isso métodos padrão de espectrometria de massas frequentemente as deixam passar. O resultado é que os pesquisadores tiveram apenas uma visão fragmentada do “citrulinoma” do corpo — o conjunto completo de proteínas citrulinizadas.
Uma estratégia de marcar e capturar em dois passos
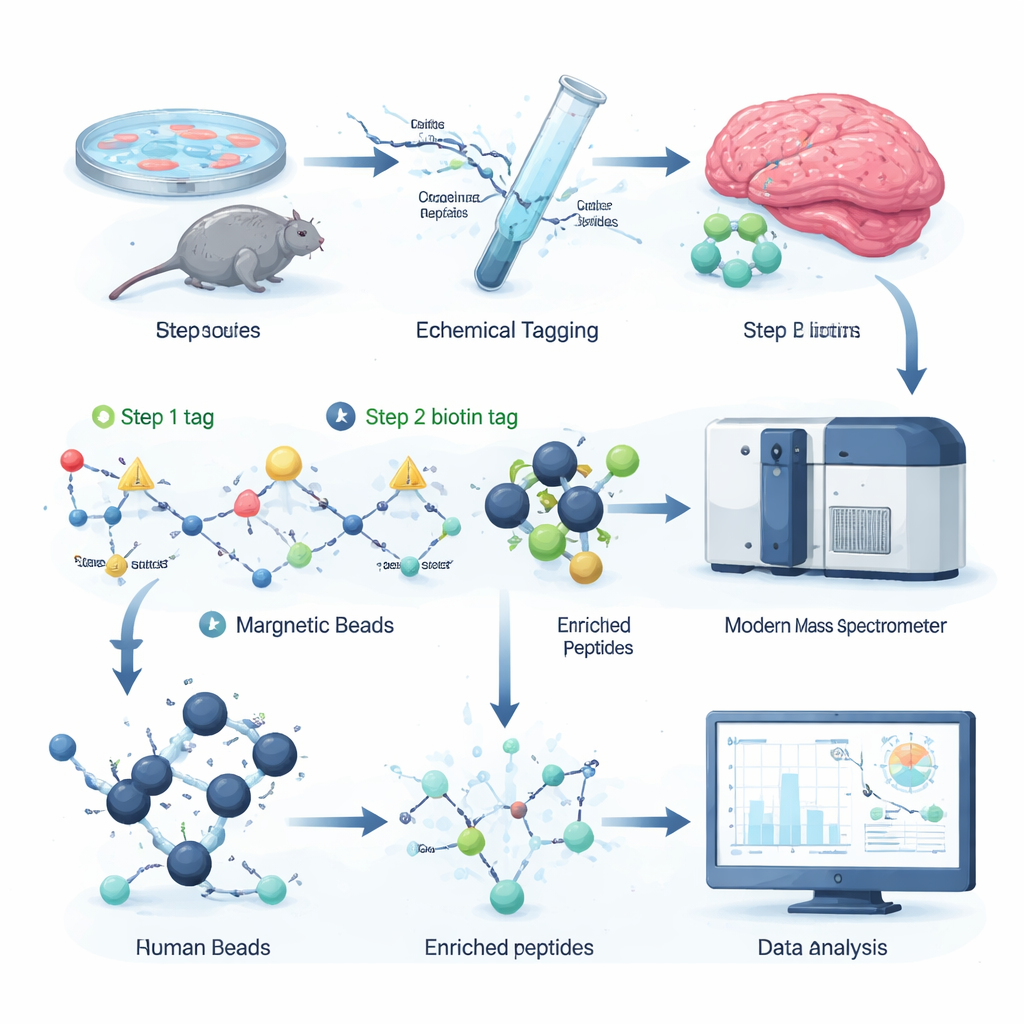
Os autores desenvolveram uma estratégia de rotulagem química que liga seletivamente uma “alça” removível aos sítios citrulinizados em peptídeos, os fragmentos de proteínas analisados por espectrometria de massas. No primeiro passo, uma pequena molécula reativa reconhece a citrulina e instala uma etiqueta diminuta. No segundo, uma etiqueta maior com biotina é acoplada por um clique, permitindo que os peptídeos rotulados sejam capturados de uma mistura complexa com esferas de estreptavidina, uma ferramenta bioquímica comum. Um tratamento químico suave então remove a parte volumosa da etiqueta, deixando um pequeno deslocamento de massa bem definido que o espectrômetro de massas detecta facilmente. Como todos os reagentes são comercialmente disponíveis e todo o protocolo cabe em placas de 96 poços, o fluxo de trabalho é rápido, escalável e compatível com plataformas de proteômica existentes.
Vendo mais do citrulinoma
Ao adicionar peptídeos citrulinizados conhecidos a extratos celulares e diluí‑los sistematicamente, a equipe demonstrou que sua estratégia de enriquecimento aumenta o sinal de peptídeos citrulinizados mais de dez vezes, mesmo quando representam menos de uma em mil moléculas. Em amostras complexas, o número de sítios citrulinizados detectados e suas intensidades medidas aumentaram dramaticamente após o enriquecimento. A aplicação do método a tecido cerebral de camundongo revelou duas a três vezes mais sítios distintos de citrulinização do que uma abordagem de última geração anterior, incluindo muitos na proteína basica da mielina, que isola fibras nervosas, e em proteínas envolvidas na comunicação sináptica. Isso sugere que a citrulinização pode influenciar tanto a sinalização entre neurônios quanto a manutenção da arquitetura cerebral.
Células imunes lançando teias proteicas pegajosas
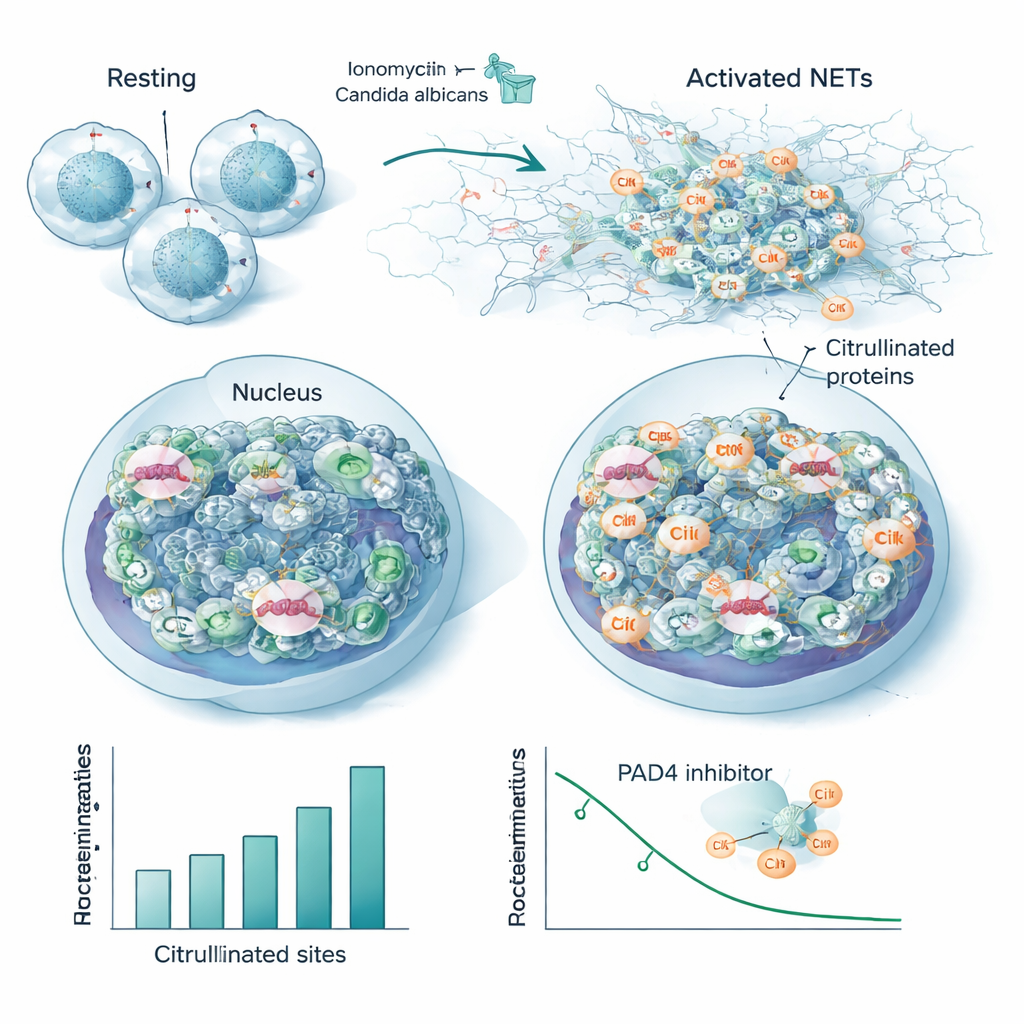
Neutrófilos, um tipo de célula branca de linha de frente, podem combater invasores liberando teias pegajosas de DNA e proteínas chamadas armadilhas extracelulares de neutrófilos, ou NETs. A formação de NETs depende de PAD4, uma enzima citrulinizante que afrouxa a cromatina para que o DNA possa ser liberado. Usando seu novo fluxo de trabalho, os pesquisadores acompanharam como a citrulinização mudava em neutrófilos humanos expostos a doses crescentes de um ativador químico. Eles detectaram até 1.700 fragmentos peptídicos citrulinizados em 580 proteínas, com centenas de sítios aumentando ou diminuindo de maneira dependente da dose, enquanto os níveis gerais de proteína permaneciam constantes. As histonas — as proteínas que empacotam o DNA — mostraram citrulinização disseminada, não apenas em alguns sítios clássicos, e variantes da histona de ligação H1 foram especialmente modificadas. Proteínas estruturais como reguladores da actina e a laminina B, que molda o envelope nuclear, também ficaram fortemente citrulinizadas, apontando para um amolecimento coordenado tanto da cromatina quanto dos andaimes celulares durante a liberação de NETs.
Uma assinatura central de citrulinização na infecção
Para imitar uma infecção real, a equipe estimulou neutrófilos com Candida albicans morta pelo calor, um patógeno fúngico comum. Embora isso tenha produzido menos sítios modificados no total do que o forte ativador químico, a grande maioria das proteínas e posições citrulinizadas se sobrepôs entre os dois estímulos. Essa sobreposição define um “citrulinoma” central conservado associado à formação de NETs, incluindo muitas proteínas nucleares e do citoesqueleto e vários autoantígenos conhecidos — os próprios alvos de anticorpos em doenças autoimunes. Quando os pesquisadores adicionaram um fármaco bloqueador de PAD4, muitos desses mesmos sítios perderam sua citrulinização de forma dependente da dose, vinculando‑os diretamente à atividade da enzima e sugerindo que podem servir como marcadores sensíveis da inibição de PAD4.
O que isso significa para a saúde e a doença
Ao transformar uma modificação elusiva em um sinal mensurável, esse fluxo de trabalho torna possível mapear onde e quando a citrulinização ocorre em tecidos, respostas imunes e modelos de doença. Para não especialistas, a mensagem chave é que a citrulinização atua como um dimmer molecular sutil nas proteínas, e poder ver seus padrões em alto detalhe pode ajudar a explicar como as doenças autoimunes começam, como infecções remodelam células imunes e como proteínas cerebrais mudam ao longo do tempo. A escalabilidade do método e sua dependência de equipamentos laboratoriais padrão significam que ele pode ser amplamente adotado, abrindo caminho para descobrir novos alvos terapêuticos, diagnósticos de precisão e uma compreensão mais profunda de como pequenas edições químicas podem ter grandes consequências biológicas.
Citação: Meelker González, R., Laposchan, S., Riedel, E. et al. High-throughput chemical proteomics workflow for profiling protein citrullination dynamics. Nat Commun 17, 1982 (2026). https://doi.org/10.1038/s41467-026-69490-1
Palavras-chave: citrulinização, doença autoimune, armadilhas extracelulares de neutrófilos, espectrometria de massas, modificação pós‑translacional