Clear Sky Science · pt
Significado fisiopatológico da acetilação da histona H3K14 dependente de KAT7 comprometida durante a deficiência de zinco
Por que nutrientes minúsculos importam para nossa saúde
O zinco é um metal-traço de que nossos corpos precisam em quantidades muito pequenas, mas que apoia discretamente centenas de proteínas que mantém as células funcionando. Quando o zinco falta — por dieta, doença ou envelhecimento — isso tem sido associado a problemas que vão do crescimento prejudicado à imunidade enfraquecida e à doença hepática gordurosa. Este estudo faz uma pergunta mais profunda: como as células realmente detectam que o zinco está em falta, e como essa escassez pode ser traduzida em mudanças duradouras na atividade gênica e na saúde dos órgãos?
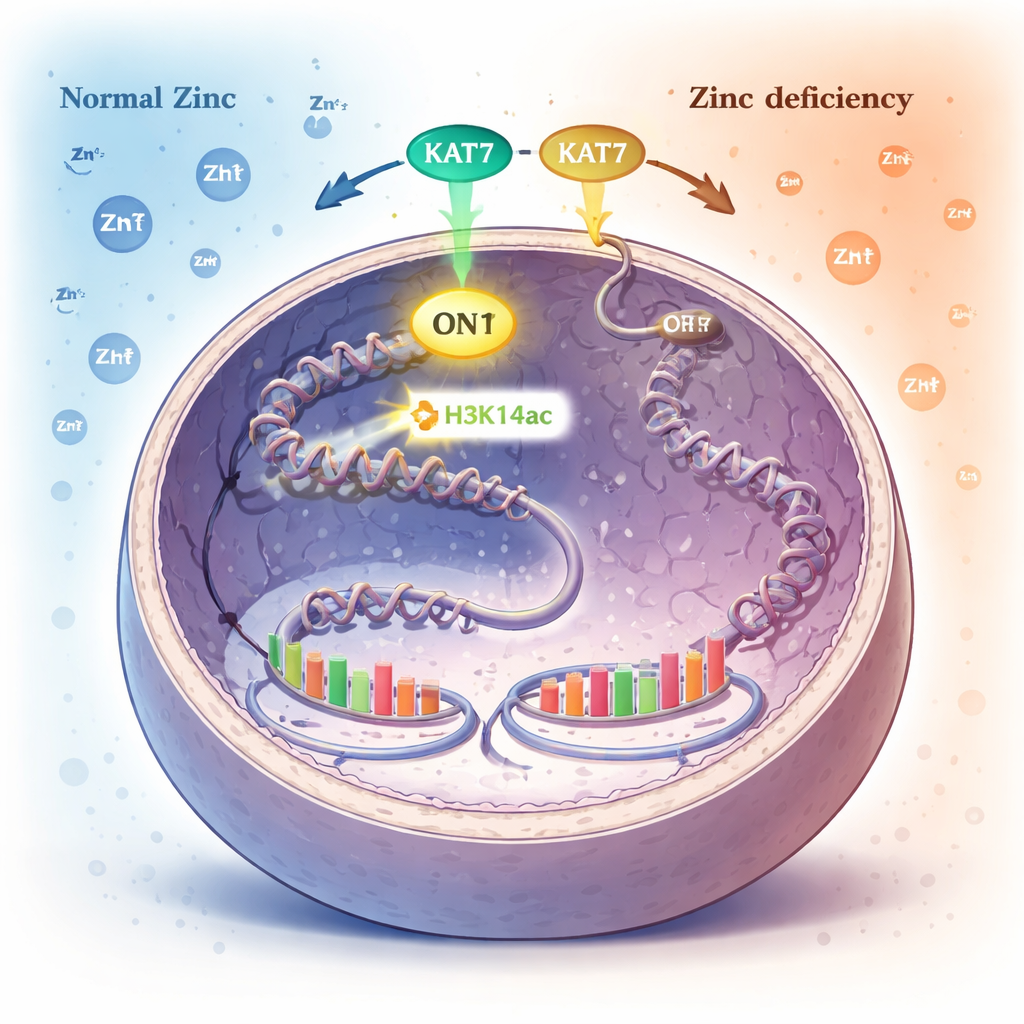
Uma marca química na embalagem do DNA como alarme interno de zinco
Dentro do núcleo, o DNA é enrolado em torno de bobinas proteicas chamadas histonas. As células controlam quais genes estão ativos adicionando ou removendo pequenas marcas químicas nessas histonas. Uma dessas marcas, chamada acetilação em um ponto específico da histona H3 (H3K14ac), é adicionada por uma enzima chamada KAT7. Os autores descobriram que, quando o zinco se torna escasso, os níveis dessa marca H3K14ac caem dramaticamente, enquanto muitas outras marcas histônicas comuns permanecem inalteradas. Isso apontou H3K14ac, e a enzima KAT7 que a gera, como um sensor-chave do estado do zinco.
Como o zinco mantém uma enzima-chave ativada
Ao desativar sistematicamente diferentes enzimas, os pesquisadores mostraram que a KAT7 é a principal fonte de H3K14ac em células humanas. A KAT7 contém uma pequena estrutura que liga zinco dentro de seu centro ativo. Quando as células foram levadas à deficiência de zinco, a capacidade da KAT7 de colocar a marca H3K14ac diminuiu, mesmo que a proteína em si permanecesse no núcleo e continuasse associada a seus parceiros auxiliares. Testes detalhados com fragmentos purificados de KAT7 revelaram que o zinco corretamente ligado nessa região é essencial para sua atividade; perturbar a ligação ao zinco inativou a enzima, e a reposição cuidadosa de zinco restaurou a função. Em essência, a KAT7 se comporta como um interruptor dependente de zinco que controla uma marca histônica específica.
Convertendo perda de zinco em mudanças gênicas que resgatam os níveis de zinco
O que a perda dessa marca histônica realmente faz? Usando mapeamento em todo o genoma, a equipe mostrou que H3K14ac é especialmente enriquecida em regiões potenciadoras — trechos regulatórios de DNA que afinam genes vizinhos. Em condições de deficiência de zinco, H3K14ac foi removida de muitos potenciadores, e quanto maior a perda, mais forte a mudança na atividade dos genes próximos. Um gene de destaque foi ZIP10, que codifica uma proteína na superfície celular que importa zinco. Quando H3K14ac caiu no potenciador de ZIP10, os níveis de ZIP10 na membrana aumentaram, permitindo que mais zinco entrasse na célula. Bloquear a KAT7 ou impedir a perda de H3K14ac interferiu nessa resposta e reduziu a captação de zinco, mesmo após a reposição do metal. Isso mostra que as células convertam a escassez de zinco em um sinal epigenético que reforça o maquinário de importação de zinco para restaurar o equilíbrio.
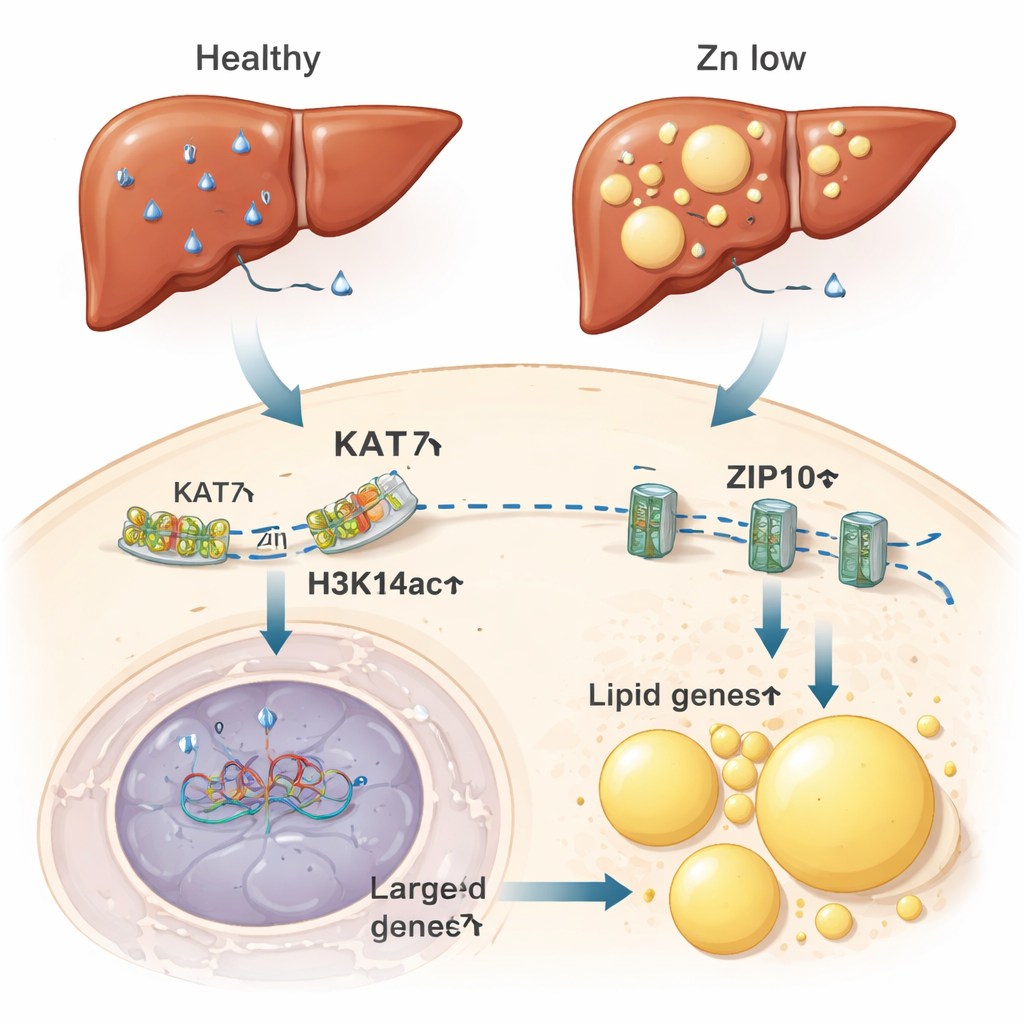
De células privadas de zinco a fígados gordurosos
Os autores seguiram perguntando se esse interruptor sensível ao zinco teria consequências em animais inteiros. Em camundongos alimentados com dieta deficiente em zinco, o fígado — um centro chave do metabolismo do zinco e das gorduras — mostrou níveis reduzidos de zinco, menor H3K14ac e atividade enfraquecida da KAT7. Essas mudanças coincidiram com maior expressão de genes que impulsionam o armazenamento de gordura e a formação de gotículas lipídicas, os minúsculos pacotes de gordura dentro das células. Os fígados dos camundongos com deficiência de zinco acumularam gordura em grau comparável ao observado em animais submetidos a dieta rica em gordura. Notavelmente, simplesmente reduzir a atividade da KAT7 com um medicamento, mesmo sem alterar o zinco dietético, foi suficiente para promover o acúmulo de gordura nas células hepáticas. Por outro lado, fornecer zinco extra diminuiu o acúmulo de gordura causado pela dieta rica em gordura.
O que isso significa para o risco de doenças humanas
Colocando suas descobertas em um contexto clínico, os pesquisadores revisaram estudos humanos que mediram níveis de zinco em tecido hepático. Em diversos relatórios, pessoas com fígado gorduroso e distúrbios relacionados apresentaram significativamente menos zinco em seus fígados do que controles saudáveis. Juntando-se aos experimentos em camundongos, isso sugere que a deficiência crônica de zinco pode promover a doença hepática gordurosa ao silenciar a KAT7, apagar a marca H3K14ac e aumentar persistentemente genes que favorecem o armazenamento de gordura. Em termos simples, o trabalho revela um circuito interno “zinco-para-epigenética”: quando o zinco cai, uma enzima dependente de zinco perde potência, alterando a embalagem do DNA de formas que primeiro ajudam as células a captar mais zinco, mas que, ao longo do tempo, também podem empurrar o fígado para um acúmulo de gordura prejudicial à saúde.
Citação: Fujisawa, T., Takenaka, S., Maekawa, L. et al. Pathophysiological significance of impaired KAT7-dependent histone H3K14 acetylation during zinc deficiency. Nat Commun 17, 1710 (2026). https://doi.org/10.1038/s41467-026-69476-z
Palavras-chave: deficiência de zinco, epigenética, gordura no fígado, acetilação de histonas, transportadores de zinco