Clear Sky Science · pt
Insights mecanicistas sobre a termodinâmica fora de equilíbrio da fixação de nitrogênio via cavitação acústica
Transformando o ar em fertilizante útil com som
O nitrogênio do ar é essencial para fertilizantes e produção de alimentos, mas converter esse gás resistente em formas úteis costuma exigir fábricas enormes, calor extremo e alta pressão. Este estudo explora uma abordagem muito diferente: usar ondas sonoras intensas para criar pequenas bolhas explosivas na água que podem "fixar" o nitrogênio em condições muito distantes do equilíbrio. Ao observar e modelar o que acontece dentro desses pontos quentes efêmeros, os pesquisadores mostram como bolhas acionadas por som podem oferecer uma nova rota para produzir químicos à base de nitrogênio sem catalisadores tradicionais ou reatores gigantes.
Por que fixar o nitrogênio é tão difícil
Nossa atmosfera é majoritariamente gás nitrogênio, mas seus átomos estão presos por uma das ligações químicas mais fortes da natureza. Quebrar essa ligação de forma eficiente é o motivo pelo qual o processo Haber–Bosch depende de equipamentos potentes e consome grandes quantidades de energia em todo o mundo. Métodos convencionais precisam atingir um equilíbrio desconfortável: temperaturas altas o suficiente para ativar o nitrogênio, mas não tão altas que os produtos desejados se decomponham ou que o equilíbrio favoreça a reação inversa. Este artigo argumenta que, em vez de manter uma temperatura constante, pode ser mais eficaz ultrapassar brevemente esse patamar — usando rajadas ultrarrápidas de calor — e então resfriar tão rapidamente que os produtos úteis fiquem aprisionados antes de se decompor.
Usando ultrassom para criar minúsculas câmaras de reação
Quando ultrassom poderoso atravessa a água, ele forma bolhas microscópicas de gás que crescem e depois colapsam violentamente, um fenômeno conhecido como cavitação acústica. Cada bolha em colapso comporta-se como um reator em miniatura e de curta duração. Em bilionésimos de segundo, o gás interno é comprimido a temperaturas acima de 5.000 kelvin e então resfriado novamente em taxas próximas a 1012 kelvin por segundo. Nessas condições, moléculas de nitrogênio na bolha podem se dividir em fragmentos reativos, que então se combinam com fragmentos derivados de oxigênio, hidrogênio ou água para formar nitrito, nitrato ou amônio. Os novos produtos são então lançados no líquido circundante, onde se acumulam ao longo do tempo enquanto a próxima geração de bolhas se forma e colapsa. 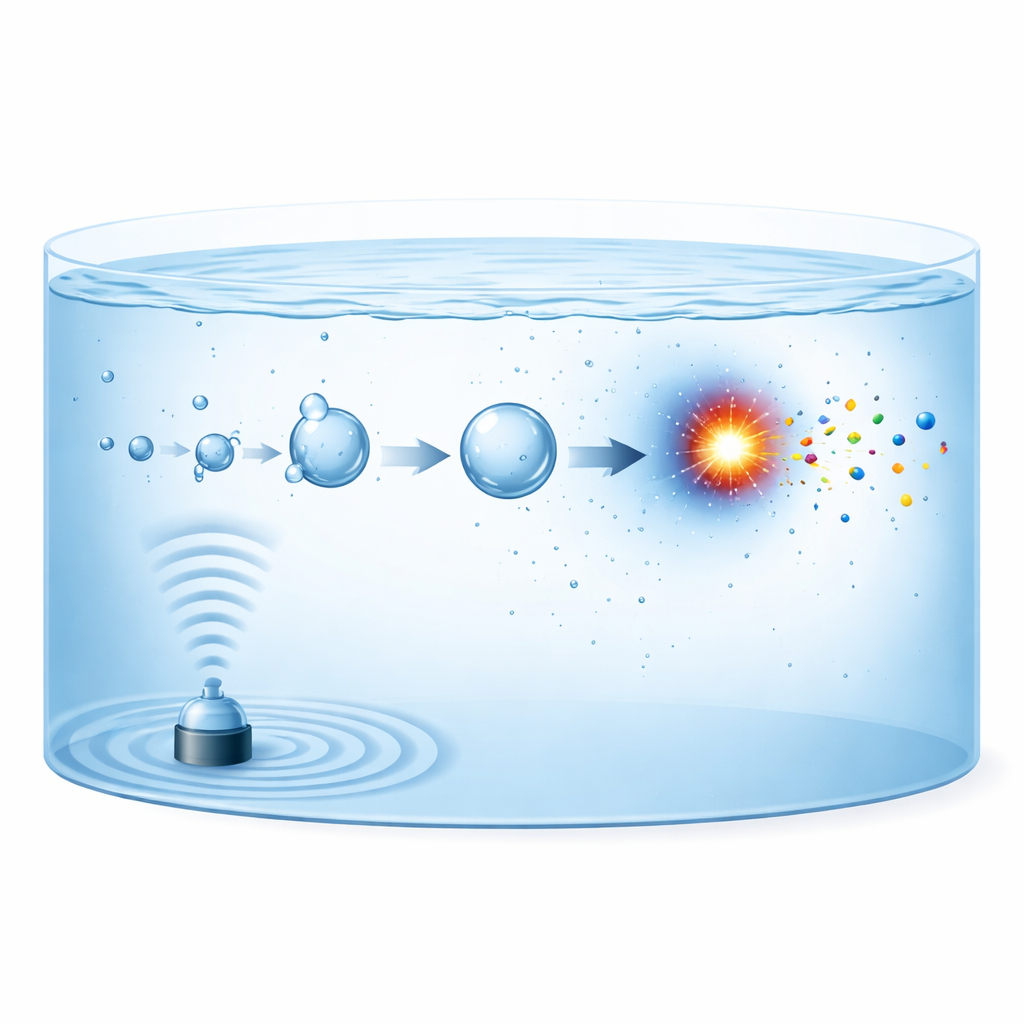
Ajustando bolhas para escolher entre diferentes produtos
A equipe variou sistematicamente os gases que alimentavam as bolhas (nitrogênio mais oxigênio ou hidrogênio), a intensidade e a frequência do ultrassom, e a presença de partículas sólidas que facilitam a formação de bolhas. Com misturas nitrogênio–oxigênio, o sistema produziu principalmente produtos oxidados, como nitrito e nitrato; com misturas nitrogênio–hidrogênio, favoreceu-se a formação de amônio. Pequenas quantidades de partículas de talco atuaram como "sementes" de bolha, reduzindo o limiar para cavitação e tornando as reações mais reprodutíveis. Ao ajustar a pressão sonora e o tempo de reação, os pesquisadores puderam deslocar o equilíbrio entre nitrito e nitrato, mostrando que parte da química ocorre dentro da bolha em colapso e parte continua na água circundante enquanto fragmentos reativos convertem lentamente o nitrito em nitrato mais oxidado.
Perscrutando o pulso térmico em nanoescala
Para entender por que condições tão extremas e fugazes ainda produzem compostos estáveis, os autores combinaram medições com simulações detalhadas e cálculos quântico-químicos. Estes mostram que, em temperaturas muito altas, o nitrogênio pode se decompor diretamente na fase gasosa, abrindo vias que normalmente são inacessíveis. Mas os mesmos cálculos também revelam que manter o gás quente tornaria os produtos finais instáveis. A chave é o resfriamento rápido: o pico de temperatura da bolha ativa o nitrogênio, então o resfriamento quase instantâneo estabiliza fragmentos intermediários e moléculas finalizadas como amônia e ácido nitroso antes que possam se decompor ou reverter a nitrogênio. Modelar bolhas individuais, especialmente quando dopadas com argônio que eleva as temperaturas de colapso, confirmou que picos de temperatura mais altos deslocam a mistura de produtos e aumentam as taxas gerais de fixação. 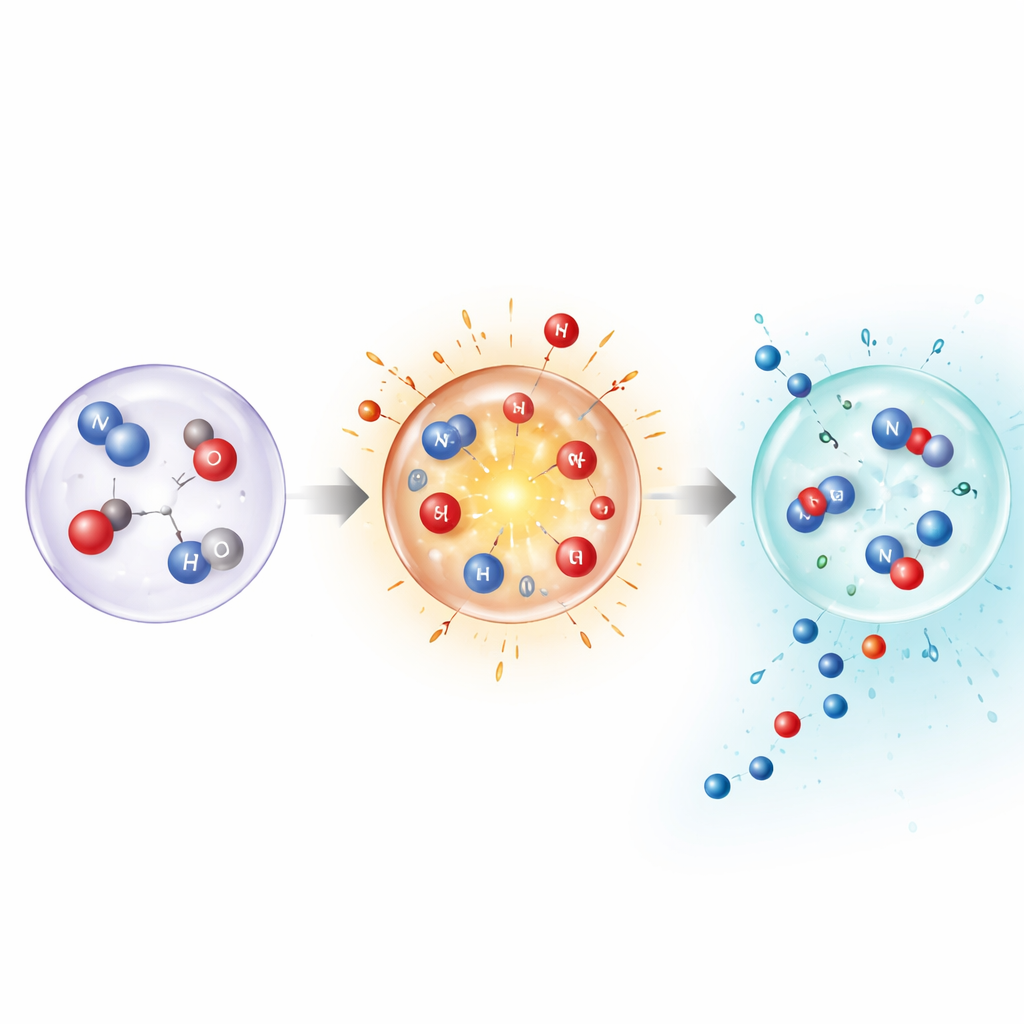
Uso de energia e possibilidades futuras
Embora este método acionado por som ainda não seja tão eficiente em termos energéticos quanto os melhores processos industriais, seu desempenho já rivaliza com abordagens históricas por arco elétrico e alguns sistemas de plasma modernos, operando tudo isso em condições ambientais e sem catalisadores sólidos. É importante que os mesmos eventos de cavitação também dividam a água, liberando hidrogênio, oxigênio e peróxido de hidrogênio — subprodutos ricos em energia que podem ser aproveitados junto com o nitrogênio fixado. Os autores enfatizam que seu arranjo foi projetado para revelar mecanismos, em vez de maximizar a produção, mas o trabalho estabelece a cavitação acústica como uma via distinta para fixar nitrogênio ao explorar ciclos térmicos extremamente rápidos em bolhas microscópicas. Para não especialistas, a conclusão é que som cuidadosamente controlado pode transformar água e ar comuns em ingredientes de fertilizante por meio de uma sequência de pequenas explosões invisíveis, sugerindo rotas mais verdes e flexíveis para produzir no futuro químicos vitais à base de nitrogênio.
Citação: Pan, X., Preso, D.B., Liu, Q. et al. Mechanistic insights into the non-equilibrium thermodynamics of nitrogen fixation via acoustic cavitation. Nat Commun 17, 2682 (2026). https://doi.org/10.1038/s41467-026-69466-1
Palavras-chave: fixação de nitrogênio, cavitação acústica, sonquímica, produção de fertilizantes, química por ultrassom