Clear Sky Science · pt
Tripla atuação em STING, TGF-β e PD-L1 potencializa o sinal CXCL16–CXCR6 para forte resposta antitumoral
Tornando tumores frios em quentes
A imunoterapia contra o câncer transformou o tratamento de alguns pacientes, mas muitos tumores ainda resistem a essas drogas poderosas. Este estudo investiga por que certos cânceres escapam aos modernos medicamentos “inibidores de checkpoint” e propõe um ataque mais inteligente em três frentes que desperta as defesas do corpo, atrai células T assassinas de elite e as mantém ativas dentro do tumor.
Por que os medicamentos imunológicos atuais não são suficientes
Grande parte das imunoterapias aprovadas mira um único freio nas células imunes, como a via PD-1/PD-L1. Uma classe mais recente de drogas tenta avançar ao bloquear também o TGF-β, uma molécula que suprime fortemente a imunidade em cânceres avançados. Um desses medicamentos, YM101, combina bloqueio de TGF-β e PD-L1 em um único anticorpo e mostrou resultados promissores em camundongos. Mas mesmo em animais geneticamente idênticos, alguns tumores praticamente não reduziram. Ao comparar tumores responsivos e resistentes, os pesquisadores descobriram que o sucesso do tratamento andava lado a lado com forte ativação imune “inata”, especialmente sinalização pela via chamada STING, que detecta DNA anômalo e dispara sinais semelhantes a alarme antiviral.
Adicionando uma terceira alavanca: a via STING
Suspeitando que a fraca ativação inata fosse a peça que faltava, a equipe combinou YM101 com um agonista de STING em forma de comprimido chamado MSA-2 em vários modelos de tumor em camundongos, incluindo tumores tipicamente difíceis de tratar, os chamados “frios”. A abordagem tripla—ativação de STING mais bloqueio de TGF-β e PD-L1—reduziu os tumores de forma mais eficaz, prolongou a sobrevida e frequentemente protegeu os camundongos contra o retorno do tumor após novo desafio, indicando memória imune duradoura. Isso superou a combinação mais convencional de um agonista de STING com bloqueio de PD-L1 sozinho, e até melhorou a terapia com agonista de STING quando apenas TGF-β era bloqueado, revelando que o próprio TGF-β atua como um freio importante sobre a imunidade mediada por STING. 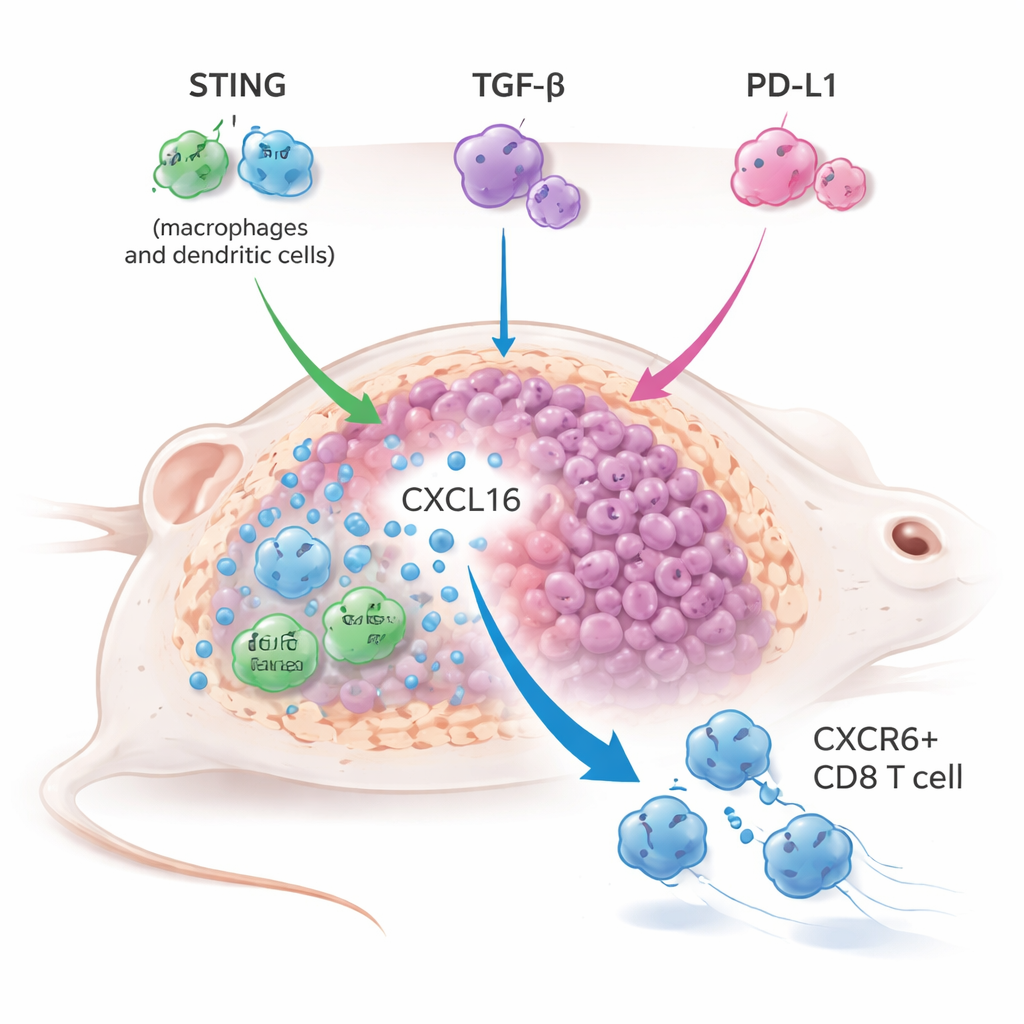
Recrutando uma força assassina especializada
Para entender como essa estratégia tripla funcionou, os pesquisadores usaram sequenciamento de RNA em célula única e perfilagem imune detalhada de tumores tratados. Eles descobriram uma expansão marcante de um subconjunto de células T citotóxicas marcadas pelo receptor CXCR6. Essas células CD8+ CXCR6+ estavam altamente armadas, expressando altos níveis de granzimas, perforina e moléculas inflamatórias, e mostravam fortes sinais de ativação e proliferação. Ao mesmo tempo, macrófagos associados ao tumor e células dendríticas aumentaram a produção de uma quimiocina chamada CXCL16, que se liga a CXCR6 e ajuda a reter essas células T no tumor. Quando a ligação CXCL16–CXCR6 foi interrompida—seja bloqueando CXCL16 ou deletando geneticamente CXCR6 nas células T—o tratamento combinado perdeu em grande parte seu poder antitumoral, comprovando que esse eixo é central para o sucesso da terapia.
Como a cascata de sinal é acionada
Aprofundando, a equipe perguntou como a ativação de STING e o bloqueio de TGF-β aumentam conjuntamente o CXCL16. Em células imunes humanas e de camundongo, agonistas de STING aumentaram fortemente CXCL16 e a citocina antiviral IFN‑β, enquanto TGF-β adicional reduziu ambos de forma acentuada. Os pesquisadores mostraram que STING desencadeia sinalização IFN‑I, que ativa o fator de transcrição STAT1; o STAT1 então se liga diretamente à região de controle do gene CXCL16, ligando sua expressão. O TGF-β interrompe essa cadeia ao interferir em uma etapa chave da sinalização de STING, provavelmente via uma proteína chamada HDAC4 e espécies reativas de oxigênio, atenuando a ativação de IRF3 e a produção downstream de IFN‑β e CXCL16. Bloquear TGF-β remove esse freio, permitindo que agonistas de STING acendam totalmente a via STAT1–CXCL16 em células mieloides e, assim, forneçam aos linfócitos CXCR6+ os sinais necessários para permanecerem e combater no tumor.
Construindo um único fármaco de precisão
Para tornar esse regime complexo mais prático e direcionado ao tumor, os pesquisadores projetaram um único “conjugado anticorpo-estimulador imune” chamado Y101S. Essa molécula combina o anticorpo duplo bloqueador de TGF-β/PD-L1 com um agonista de STING ligado por um conector clivável. Y101S é direcionado a células mieloides PD-L1–positivas no tumor, é internalizado e então libera a droga de STING dentro dessas células. Em vários modelos de câncer em camundongos, Y101S igualou ou superou a eficácia de administrar YM101 mais um agonista de STING livre em alta dose, apesar de carregar apenas uma fração minúscula daquela dose de STING. Ele aumentou macrófagos e células dendríticas CXCL16+, expandiu células CD8+ CXCR6+, induziu memória imune durável e concentrou sinais inflamatórios nos tumores enquanto poupava órgãos saudáveis, com um perfil de segurança favorável em camundongos. 
O que isso significa para o tratamento futuro do câncer
Para não especialistas, a mensagem-chave é que atacar o câncer com apenas um ou dois interruptores imunes pode não ser suficiente—especialmente quando tumores silenciam ativamente os primeiros sistemas de alarme. Este trabalho mostra que combinar ativação de STING com bloqueio de TGF-β e PD-L1 pode reconfigurar o microambiente tumoral, atrair e sustentar de forma potente um grupo especializado de células T citotóxicas e alcançar respostas mais profundas e duradouras em modelos pré-clínicos. O anticorpo-droga alvo Y101S encarna essa estratégia em um único medicamento direcionado e oferece um roteiro para imunoterapias de próxima geração destinadas a tumores que hoje resistem aos inibidores de checkpoint padrão.
Citação: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
Palavras-chave: imunoterapia contra o câncer, via STING, bloqueio de TGF-beta, anticorpo anti–PD-L1, CXCL16 CXCR6 células T