Clear Sky Science · pt
Cooperatividade positiva entre domínios de ligação a RAS e domínios ricos em cisteína regula a cinética de ligação de RAF à membrana via re-ligação lateral
Por que essa pequena dança molecular importa
Dentro de nossas células, decisões de vida ou morte sobre crescimento, divisão e sobrevivência muitas vezes são tomadas na superfície da membrana celular. Um ator-chave nessas decisões é uma proteína chamada RAF, que ajuda a transmitir sinais de crescimento e frequentemente está desregulada no câncer. Este estudo revela, com detalhes cinéticos sem precedentes, como o RAF se prende às membranas celulares, quanto tempo permanece nelas e por que regiões densas de outra proteína, RAS, podem manter o RAF ativo por mais tempo do que se esperava.
Sinais se encontrando na superfície celular
O RAF atua em uma via de sinalização importante conhecida como via MAPK, que conecta sinais externos, como fatores de crescimento, a alterações na atividade gênica. Em sua forma inativa, o RAF flutua no interior da célula em uma configuração dobrada e auto-inibida. Ele só é ativado quando encontra o RAS, um pequeno interruptor molecular ancorado na face interna da membrana celular. O RAS precisa estar em seu estado “ligado” e inserido no tipo certo de lipídios para que o RAF seja recrutado e ativado. Como as moléculas de RAF são relativamente escassas em comparação com muitos outros componentes de sinalização, a forma exata como elas se ligam à membrana e evitam a liberação prematura influencia fortemente se uma célula responderá de forma fraca ou intensa a um sinal de crescimento.
Duas mãos para agarrar a membrana
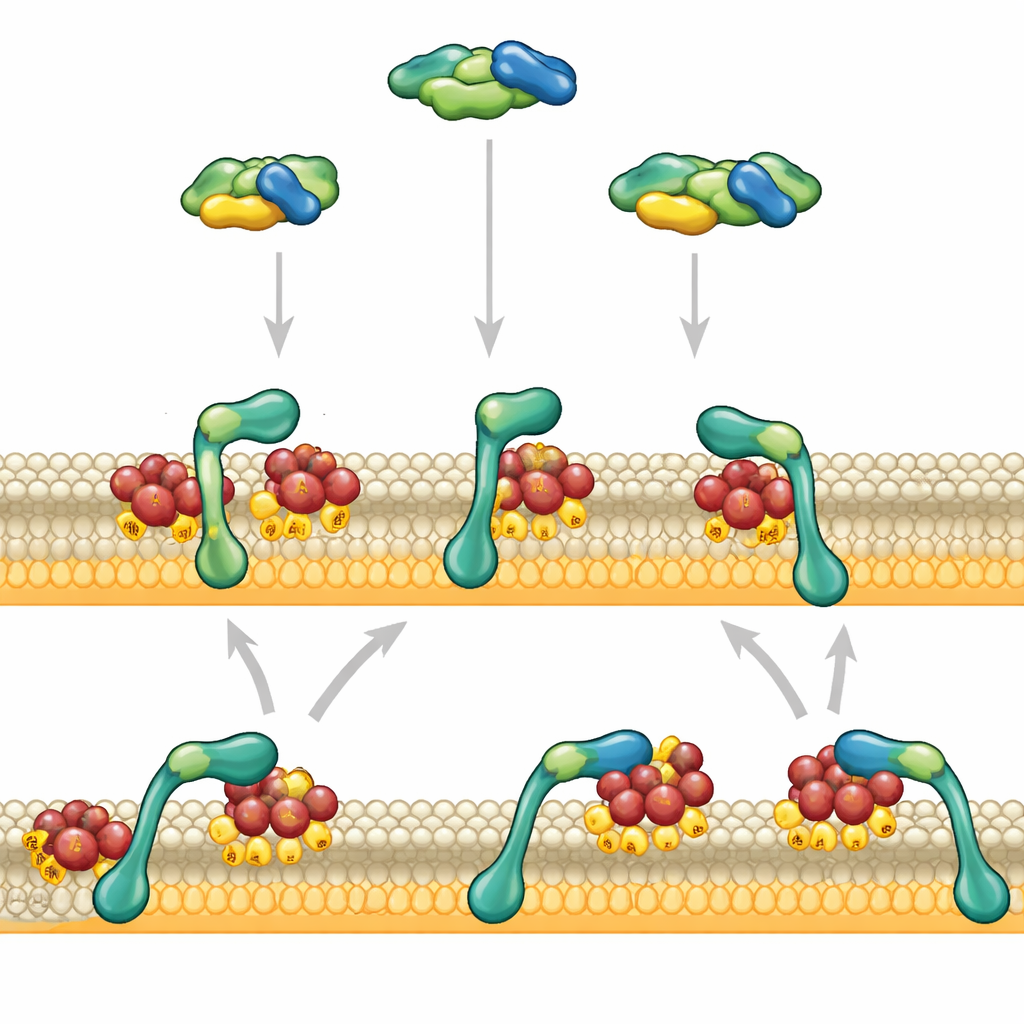
Os autores focaram em duas regiões na extremidade anterior do RAF: uma que prende o RAS e outra que prefere lipídios de membrana carregados negativamente. Usando membranas artificiais e proteínas purificadas, observaram fragmentos individuais de RAF ligando-se a superfícies decoradas com RAS por meio de microscopia avançada. Quando a região de ligação a RAS atuava sozinha, tocava a membrana brevemente e se soltava em cerca de um segundo. A região que prefere lipídios, por si só, quase não aderiu. Mas quando essas duas regiões foram conectadas, o comportamento mudou drasticamente: o RAF passou a se ligar fortemente e a permanecer na membrana por dezenas de segundos, especialmente quando a membrana continha muitos lipídios carregados negativamente semelhantes aos de células reais.
Cooperação que retarda a saída
Essa mudança dramática não ocorreu porque o RAF encontrava a membrana mais rapidamente, mas porque saía mais lentamente. Primeiro, o segmento de ligação a RAS do RAF reconhece o RAS ativado e ancora o RAF na membrana. Só depois desse primeiro aperto de mão a região de ligação a lipídios passa a interagir plenamente com os lipídios circundantes, reduzindo o movimento lateral do RAF e ancorando-o com mais firmeza. Esse segundo contato, por sua vez, estabiliza a interação original RAS–RAF, criando um ciclo de feedback positivo entre contatos proteína–proteína e proteína–lipídio. Experimentos que alteraram o curto conector (linker) que une as duas regiões mostraram que a coordenação espacial estreita entre elas é crucial: tornar o conector mais flexível ou mais longo enfraqueceu a capacidade do RAF de permanecer na membrana.
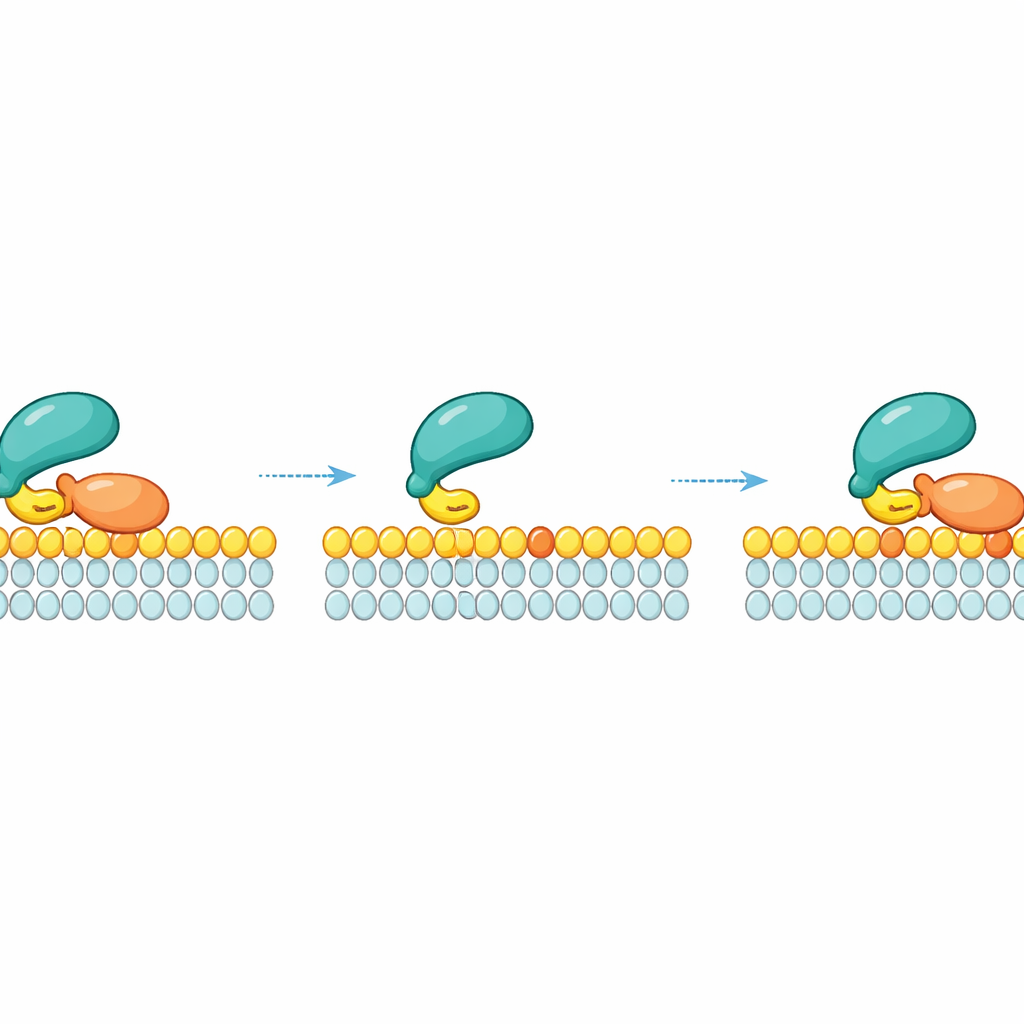
Re-ligação lateral: deslizar em vez de cair
Uma ideia central do trabalho é que o RAF não se solta simplesmente para o fluido circundante quando perde a ligação com uma molécula específica de RAS. Em vez disso, após o RAS se desligar, o RAF pode permanecer brevemente preso à membrana por meio de seu fraco contato com lipídios e deslizar lateralmente. Enquanto está nesse estado transitório, pode "reagarrar" uma molécula vizinha de RAS no mesmo fragmento de membrana. Essa re-ligação lateral cria uma rede de segurança cinética: em alta densidade local de RAS — por exemplo em nanoclusters onde moléculas de RAS se empacotam densamente — o RAF tem muitas chances de se reconectar ao RAS antes de se afastar. Medições e simulações mostraram que quanto maior a densidade de RAS ativo na membrana, mais tempo o RAF permanece ligado à membrana devido a essas reanexações locais repetidas.
De visitas prolongadas a ativação confiável
O tempo estendido que o RAF passa na membrana tem consequências importantes. A ativação do RAF não é um evento único, mas uma sequência multietapa que inclui mudanças conformacionais, remoção de marcas inibitórias e o pareamento de duas moléculas de RAF em um dímero ativo. O estudo sugere que apenas moléculas de RAF que permanecem tempo suficiente na membrana conseguem completar essa sequência, uma forma de "prova cinética" que ajuda as células a evitar ativações acidentais causadas por sinais fugazes e fracos. Ao revelar como a interação entre ligação a RAS, engajamento lipídico e re-ligação lateral determina a residência do RAF na membrana, o trabalho descreve uma estratégia geral pela qual as células podem usar muitas interações pequenas e fracas nas membranas para ajustar com precisão vias de sinalização poderosas.
Citação: Jimenez Salinas, A., Tevdorashvili, K., Grim, J. et al. Positive cooperativity between RAS-binding and cysteine-rich domains regulates RAF membrane binding kinetics via lateral rebinding. Nat Commun 17, 2593 (2026). https://doi.org/10.1038/s41467-026-69437-6
Palavras-chave: RAS, quinase RAF, sinalização na membrana celular, re-ligação lateral, prova cinética