Clear Sky Science · pt
Sal de sulfato de guanidínio dinâmica para adsorção seletiva de dióxido de carbono com inflexão de pressão negativa
Um sal inteligente que retira dióxido de carbono do gás
Reduzir o dióxido de carbono (CO2) de chaminés industriais e do ar é central para desacelerar as mudanças climáticas, mas a maioria dos métodos de captura atuais consome muita energia e é complexa. Este estudo apresenta um material surpreendentemente simples — um sal de aparência comum chamado sulfato de guanidínio — que se comporta de forma extraordinária quando entra em contato com CO2. Ele não apenas absorve grandes quantidades do gás, como o faz por meio de um efeito de “auto‑bombeamento” incorporado que pode, de fato, reduzir a pressão do gás dentro de um espaço fechado, abrindo novas possibilidades para dispositivos compactos de captura de CO2 e controle de pressão.
Por que este sal importa para um ar mais limpo
O sulfato de guanidínio (SG) é feito a partir de ingredientes baratos e abundantes e é mantido por ligações de hidrogênio, as mesmas atrações suaves que definem a água e o DNA. Como essas ligações são flexíveis, a estrutura cristalina do sal pode se rearranjar quando submetida a calor ou pressão de gás. Os autores descobriram que o SG pode existir em pelo menos três formas sólidas, chamadas fases α, β e γ, que diferem tanto em estabilidade quanto em quanto espaço vazio contêm. Sob condições moderadas, essas formas podem hospedar seletivamente CO2 enquanto ignoram o nitrogênio, sugerindo que este sal modesto pode competir com materiais porosos de ponta usados para separação de gases.
Como o material muda de forma para capturar mais gás
Em medições cuidadosas da quantidade de CO2 que o sal absorve em diferentes pressões, a equipe constatou que a forma β do SG faz algo raro. A princípio, quase nenhum CO2 penetra; as pequenas cavidades internas estão efetivamente fechadas até que a pressão do gás ultrapasse um “portão” limiar. Uma vez alcançado esse ponto, o CO2 começa a infiltrar‑se em bolsões isoladas dentro do cristal. À medida que a pressão aumenta, a quantidade de CO2 absorvida cresce de forma constante — até uma pressão crítica, quando o material sofre uma transformação súbita e mais profunda para uma forma γ mais aberta, com poros maiores que podem acomodar muito mais moléculas de CO2.
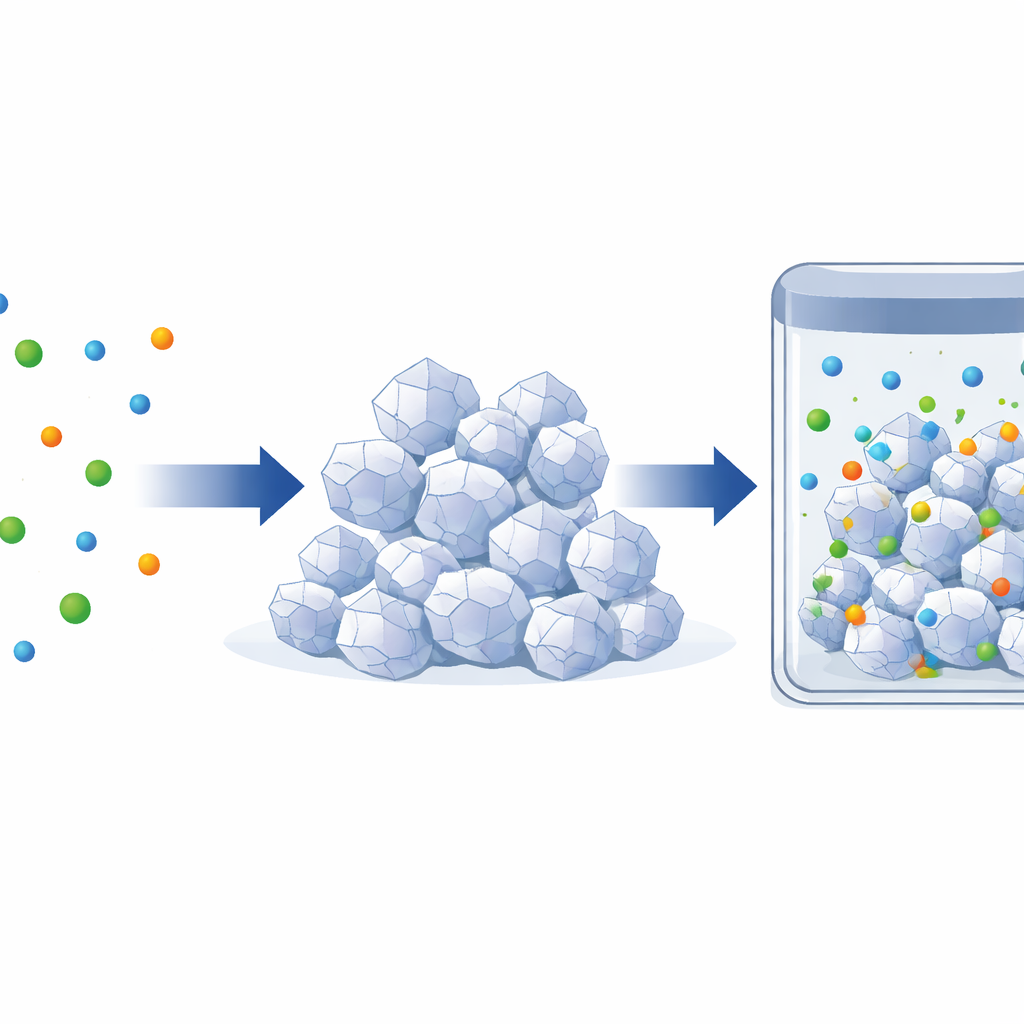
Uma estranha queda de pressão com explicação simples
Em uma célula de teste fechada, essa capacidade extra repentina leva a um efeito contra‑intuitivo que os autores chamam de inflexão de pressão negativa. Em vez de a pressão na célula aumentar à medida que mais CO2 é introduzido, ela cai brevemente. A razão é que o reestruturamento interno do cristal age como a abertura de salas de armazenamento ocultas: o sal absorve tanto CO2 adicional tão rapidamente que as moléculas de CO2 desaparecem da fase gasosa livre mais depressa do que são fornecidas, reduzindo temporariamente a pressão total. Isso é o oposto de um fenômeno anterior conhecido como adsorção negativa de gás, em que uma estrutura expulsa gás e aumenta a pressão. Aqui, o material efetivamente “engole” o gás e alivia a pressão.
Observando o funcionamento interno do cristal
Para entender esses saltos estranhos no comportamento, os pesquisadores combinaram medidas por raios X com simulações por computador que mapeiam o panorama energético dos empacotamentos cristalinos possíveis. Confirmaram que α‑SG é a forma mais estável em repouso, β‑SG tem energia ligeiramente maior, e γ‑SG é a mais aberta, mas também a menos estável a não ser na presença de CO2. Cálculos mostraram que, à medida que mais CO2 preenche os poros, γ‑SG torna‑se energeticamente favorecida, impulsionando a transição de β para γ. As simulações também revelaram breves movimentos de “respiração” na estrutura β, onde pequenos canais conectam momentaneamente cavidades isoladas, permitindo que o CO2 difunda e desencadeie o rearranjo total.
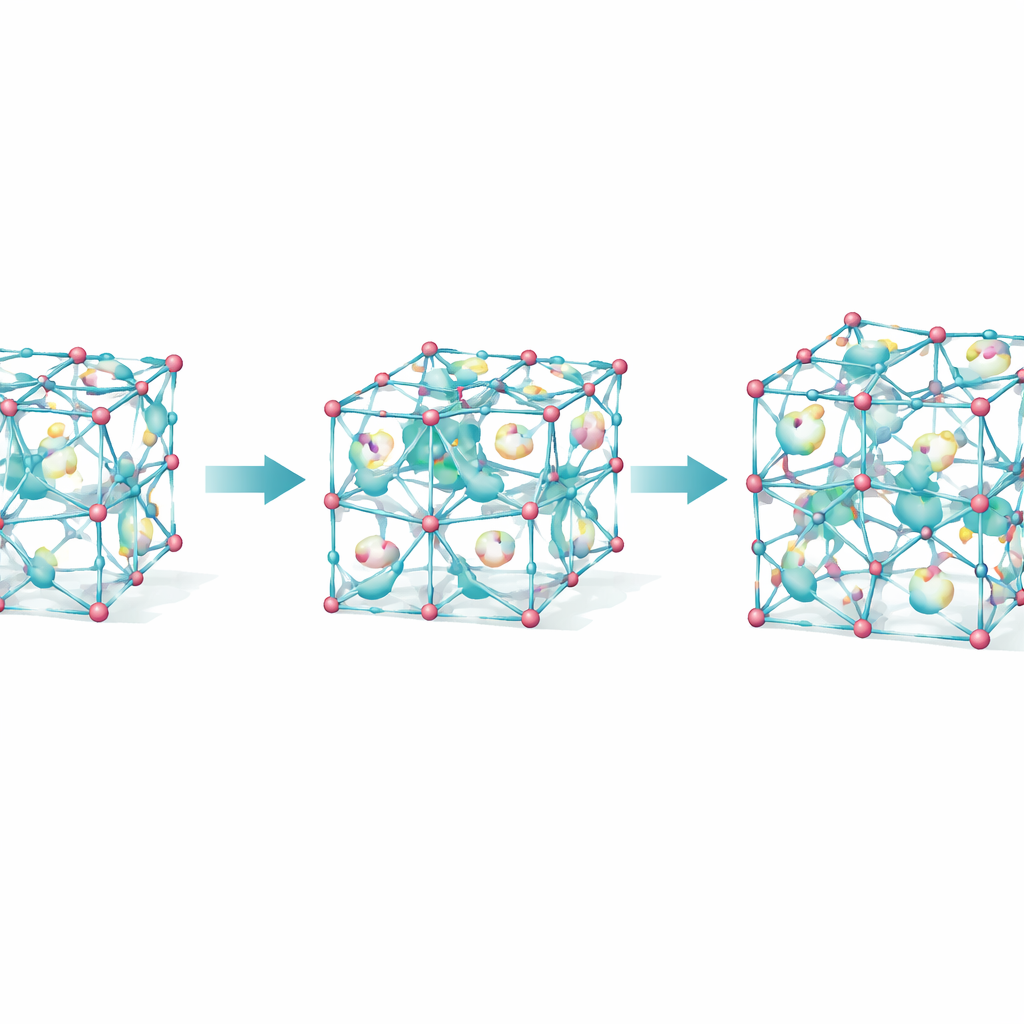
De curiosidade de laboratório a esponja prática para CO2
O trabalho vai além de uma curiosidade na física gás‑sólido. A forma γ carregada com CO2 retém cerca de 17 por cento de seu peso em gás (por volta de 4,2 milimoles por grama em temperaturas próximas de zero e pressões do dia a dia) e o libera de forma limpa quando aquecida suavemente, sem o alto custo energético de ferver água em soluções padrão de aminas. O sal permanece estável por muitos ciclos de captura e liberação e prefere fortemente CO2 em relação ao nitrogênio em gases mistos, um requisito essencial para o tratamento de gases de combustão no mundo real. Em termos simples, este sal dinâmico comporta‑se como uma esponja adaptativa que se abre, se remodela e até reduz brevemente a pressão para atrair CO2, oferecendo uma rota promissora rumo a sistemas mais simples e eficientes para capturar, armazenar e transportar este gás que aquece o clima.
Citação: Zhao, L., Zhao, C., Liu, C. et al. Dynamic guanidinium sulfate salt for selective carbon dioxide adsorption with negative pressure inflexion. Nat Commun 17, 2628 (2026). https://doi.org/10.1038/s41467-026-69433-w
Palavras-chave: captura de dióxido de carbono, sais porosos, adsorção de gases, estruturas ligadas por ligações de hidrogênio, transições de fase