Clear Sky Science · pt
Falta de MDA5 atrasa o envelhecimento hematopoiético ao modular inflammaging e proteostase em camundongos
Por que manter o sangue jovem importa conforme envelhecemos
À medida que envelhecemos, o sistema que produz nossas células sanguíneas vai se degradando lentamente. As células-tronco na medula óssea que normalmente reabastecem glóbulos vermelhos, células do sistema imune e plaquetas tornam-se mais propensas à inflamação e mais inclinadas a produzir certos tipos celulares em detrimento de outros. Essa mudança contribui para anemia, imunidade enfraquecida e maior risco de câncer na idade avançada. O estudo resumido aqui explora um interveniente surpreendente nesse processo: um sensor antiviral chamado MDA5. Ao desativar essa única molécula em camundongos, os pesquisadores descobriram que conseguiram manter as células-tronco formadoras de sangue funcionalmente mais jovens por mais tempo.
Um sensor feito para combater vírus que se volta contra o organismo com a idade
MDA5 é um sensor da imunidade inata que detecta RNA de dupla fita, um padrão molecular comum em vírus mas também gerado a partir dos nossos próprios genomas, especialmente por elementos genéticos móveis cuja atividade aumenta com a idade. Quando MDA5 detecta esse RNA, ele desencadeia uma cascata de sinais inflamatórios e respostas antivirais. A equipe investigou se essa ativação de baixo nível constante em animais mais velhos poderia impulsionar o “inflammaging” — a inflamação persistente e branda que acompanha o envelhecimento — na medula óssea. Comparando camundongos normais com camundongos sem MDA5, mediram muitas moléculas de sinalização imune no fluido da medula. Camundongos idosos sem MDA5 apresentaram níveis marcadamente menores de citocinas inflamatórias-chave, incluindo interferon-β e interleucina-1, e mostraram redução na ativação de regiões inflamatórias do DNA em células-tronco, indicando um ambiente mais calmo e menos inflamado.
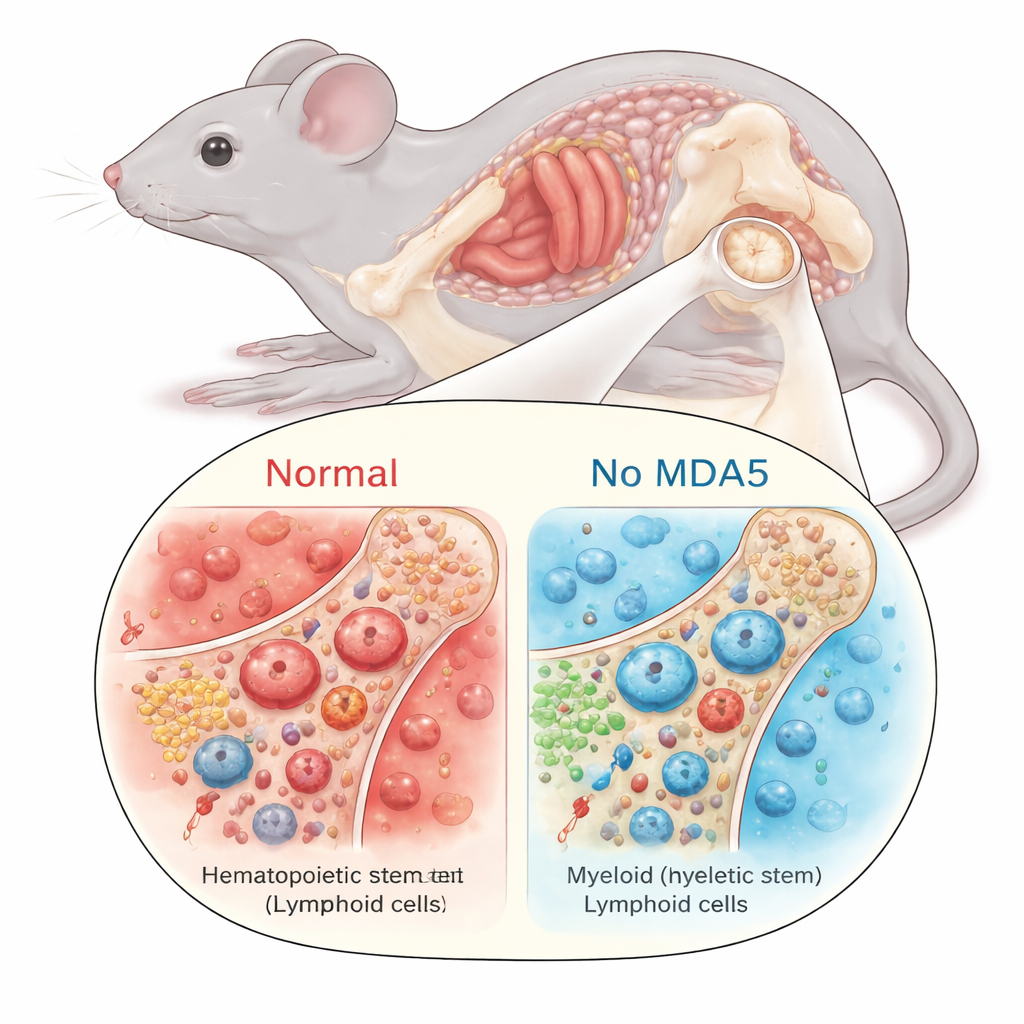
Comportamento mais jovem das células-tronco sanguíneas envelhecidas
Com menos inflamação na medula, as células-tronco formadoras de sangue se comportaram de forma diferente. No envelhecimento normal, essas células-tronco hematopoiéticas (HSCs) tendem a se acumular em número, mas a perder qualidade: dividem-se com mais frequência, perdem sua capacidade regenerativa de longo prazo e desenvolvem um viés para produzir células mieloides (como certos leucócitos) em vez de células linfoides que sustentam a imunidade adaptativa. Em camundongos idosos desprovidos de MDA5, esse padrão típico foi atenuado. Suas HSCs expandiram-se menos, mostraram um viés mieloide reduzido e permaneceram mais quiescentes — passando mais tempo em estado de repouso em vez de proliferar. Quando os pesquisadores transplantaram números iguais de células-tronco em camundongos receptores irradiados, as HSCs idosas sem MDA5 foram melhores em reconstruir o sistema sanguíneo em condições não competitivas, indicando reservas funcionais superiores em comparação com HSCs normais da mesma idade.
Metabolismo e controle da qualidade proteica permanecem mais juvenis
Além da contagem e do comportamento celular, os pesquisadores examinaram o funcionamento interno dessas células-tronco. Usando uma combinação de expressão gênica, acessibilidade de cromatina, perfilagem de metabólitos e análises de célula única, eles descobriram que a perda de MDA5 preservou um perfil metabólico e de manutenção proteica mais jovem. HSCs idosas sem MDA5 apresentaram marcadores redox mais saudáveis, como níveis menores de glutationa oxidada e níveis mais elevados de NAD e NADP, moléculas associadas à resiliência celular. Dentro dessas células, proteínas mal dobradas e desnaturadas — uma marca do envelhecimento e do estresse — foram reduzidas, enquanto marcadores de autofagia, o processo pelo qual as células reciclam componentes danificados, aumentaram. A síntese proteica foi diminuída, e aminoácidos se acumularam, consistente com uma mudança para um controle de qualidade proteica mais cuidadoso em vez de produção rápida e sujeita a erros.
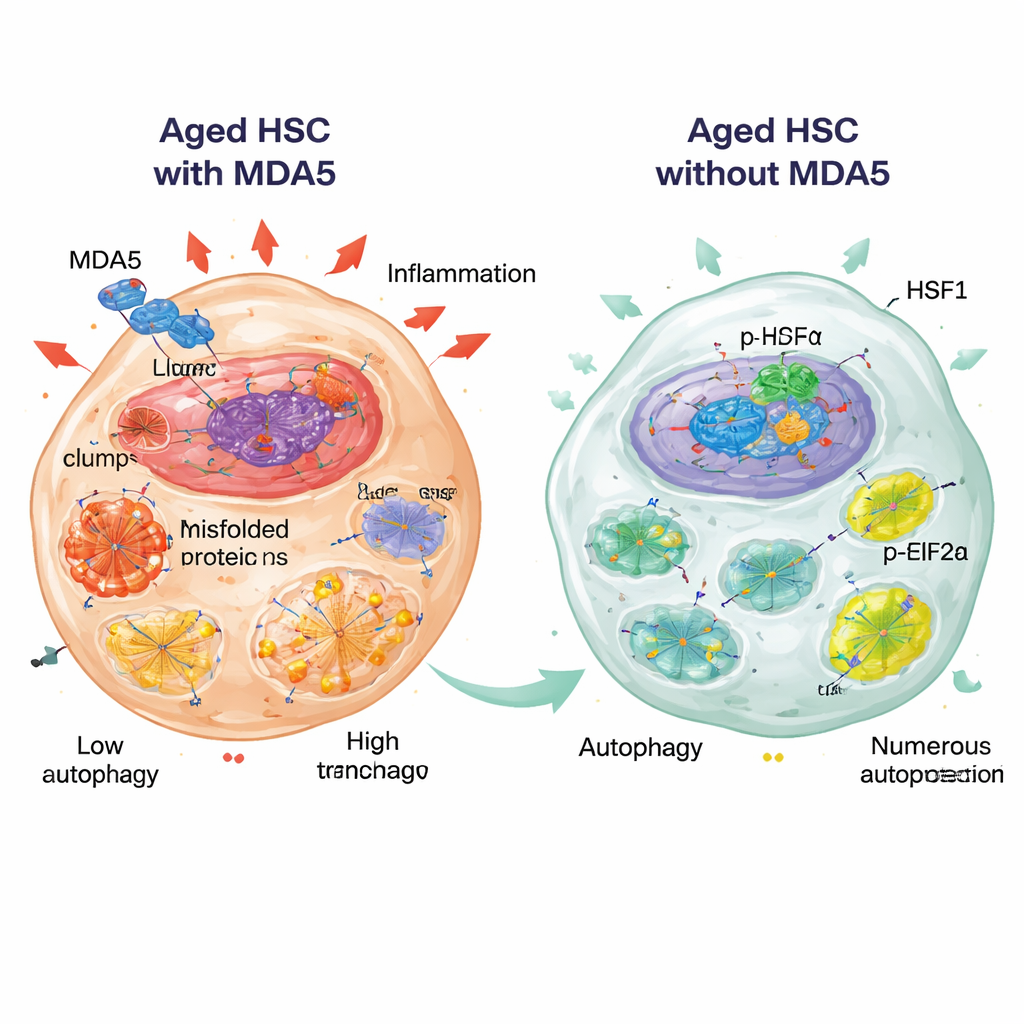
HSF1 e eIF2α: guardiões da proteostase
Dois reguladores moleculares emergiram como centrais para esse estado protetor: HSF1, um fator de transcrição mestre que aumenta a produção de chaperonas e outros fatores protetores de proteínas, e eIF2α, um fator de tradução cuja forma fosforilada (p-eIF2α) desacelera a síntese proteica durante o estresse. Em HSCs idosas sem MDA5, os níveis de proteína HSF1 e sua localização nuclear estavam elevados, e p-eIF2α também estava aumentado, consistente com um programa ativo de proteção contra estresse. Os autores descobriram que MDA5 pode se aproximar de HSF1 e, quando superexpresso, pode reter HSF1 no citoplasma, sugerindo que MDA5 ativo pode limitar as funções nucleares benéficas de HSF1. Importante, quando ativaram farmacologicamente HSF1 em HSCs idosas normais usando uma pequena molécula, essas células ficaram mais quiescentes e melhor mantiveram sua capacidade de formar colônias ao longo de rodadas repetidas em cultura, imitando parcialmente as características juvenis observadas na ausência de MDA5.
O que isso significa para o envelhecimento saudável do sangue
Em conjunto, esses achados descrevem um quadro no qual a ativação crônica de um sensor antiviral, MDA5, gradualmente empurra as células-tronco formadoras de sangue para um estado de inflamação, estresse metabólico e dano proteico. Remover MDA5 em camundongos interrompe esse ciclo: os sinais inflamatórios na medula são atenuados, as HSCs permanecem mais descansadas e menos tendenciosas, e seus sistemas internos de controle da qualidade proteica se mantêm robustos. Embora desativar diretamente MDA5 em pessoas seria arriscado devido ao seu papel no combate a infecções, este trabalho destaca o princípio amplo de que direcionar a inflamação relacionada à idade e reforçar a proteostase pode ajudar a preservar a função das células-tronco sanguíneas em idades avançadas. A longo prazo, formas mais seguras de modular as vias relacionadas a MDA5 ou de impulsionar as respostas ao estresse mediadas por HSF1 e eIF2α podem oferecer estratégias para estender a janela de saúde do nosso sangue e dos sistemas imunológicos.
Citação: Bergo, V., Bousounis, P., To Vu, G. et al. Lack of MDA5 delays hematopoietic aging by modulating inflammaging and proteostasis in mice. Nat Commun 17, 1645 (2026). https://doi.org/10.1038/s41467-026-69424-x
Palavras-chave: células-tronco hematopoiéticas, inflammaging, MDA5, proteostase, sangue envelhecido