Clear Sky Science · pt
Base estrutural e molecular para a regulação alostérica e o acoplamento catalítico da fosforibosilformilglicinamida amida sintase humana
Por que esta enzima importa para a saúde
Cada célula do seu corpo depende de purinas, pequenas moléculas que impulsionam reações, armazenam energia e carregam informação genética. Células cancerosas, que se dividem rapidamente, têm uma demanda especialmente alta por purinas e frequentemente reprogramam a forma como elas são produzidas. Este estudo foca numa enzima humana chamada FGAMS, um elemento central na construção de purinas a partir do zero. Ao revelar a estrutura tridimensional da FGAMS e como suas partes se movem e se comunicam, os autores desvendam como a enzima é ativada e inativada e como ela pode ser alvo para desacelerar o crescimento tumoral.
Tijolos da vida sob controle
As células sintetizam purinas por meio de uma linha de montagem exigente conhecida como via de novo, que consome energia e várias enzimas para montar um anel complexo. A FGAMS realiza a quarta etapa dessa sequência e ocupa um lugar central em um aglomerado enzimático maior chamado purinosoma, que ajuda a canalizar os ingredientes de forma eficiente. Como células de crescimento rápido frequentemente amplificam essa via, enzimas como a FGAMS são alvos atrativos para drogas: bloqueá‑las pode privar tumores dos nucleotídeos de que precisam, enquanto células saudáveis recorrem a vias de reciclagem.
Uma máquina molecular que muda de forma
A FGAMS é composta por três partes conectadas, ou domínios, que desempenham cada um uma função diferente e precisam cooperar em uma ordem precisa. Um domínio libera amônia do aminoácido glutamina, outro usa essa amônia para modificar uma pequena molécula à base de açúcar, e um terceiro atua como um centro regulador. Usando microscopia crioeletrônica de alta resolução, os pesquisadores capturaram a FGAMS em três estados de trabalho distintos: com uma molécula transportadora de energia ligada, com um intermediário reacional de vida curta aprisionado e com múltiplos substratos e intermediários presentes simultaneamente. Comparar esses estados revelou que alças flexíveis e um “braço” N‑terminal movem‑se dramaticamente, reconfigurando a enzima conforme a química avança.
Túnel oculto e portas moleculares
Um enigma chave tem sido como a amônia liberada em um domínio viaja com segurança até o sítio distante onde é utilizada, sem difundir‑se e causar danos. As novas estruturas expõem um túnel interno até então invisível que conecta os dois sítios, juntamente com uma série de “portas” formadas por aminoácidos específicos. Quando os substratos apropriados se ligam e o intermediário se forma, uma alça central prende‑se em uma posição ordenada, puxando o domínio N‑terminal e rearranjando alças próximas no domínio catalítico. Essa coreografia abre duas portas de entrada para que a glutamina possa ser processada e remodela brevemente uma região que estabiliza o intermediário de alta energia necessário para a quebra de ligações.
Acoplando a química por meio do movimento
À medida que a reação progride, a enzima não fica simplesmente esperando; ela usa cada etapa química como um sinal. Uma vez que um intermediário tioéster covalente se forma no domínio gerador de amônia, os movimentos anteriores são parcialmente revertidos. Isso relaxa a alça central e reposiciona as portas para fechar rotas de escape, enquanto duas portas adicionais em cada extremidade do túnel se abrem. Mudanças sutis em um punhado de resíduos que atuam como “estreitos” alargam a passagem interna, permitindo que uma molécula de amônia percorra o túnel diretamente até o segundo sítio ativo, onde reage com o intermediário aprisionado para produzir o produto final. Mutar os resíduos das portas causa vazamento de amônia ou desacoplamento das duas metades da reação, confirmando que esse sistema de portas e canal é essencial para uma catálise eficiente.
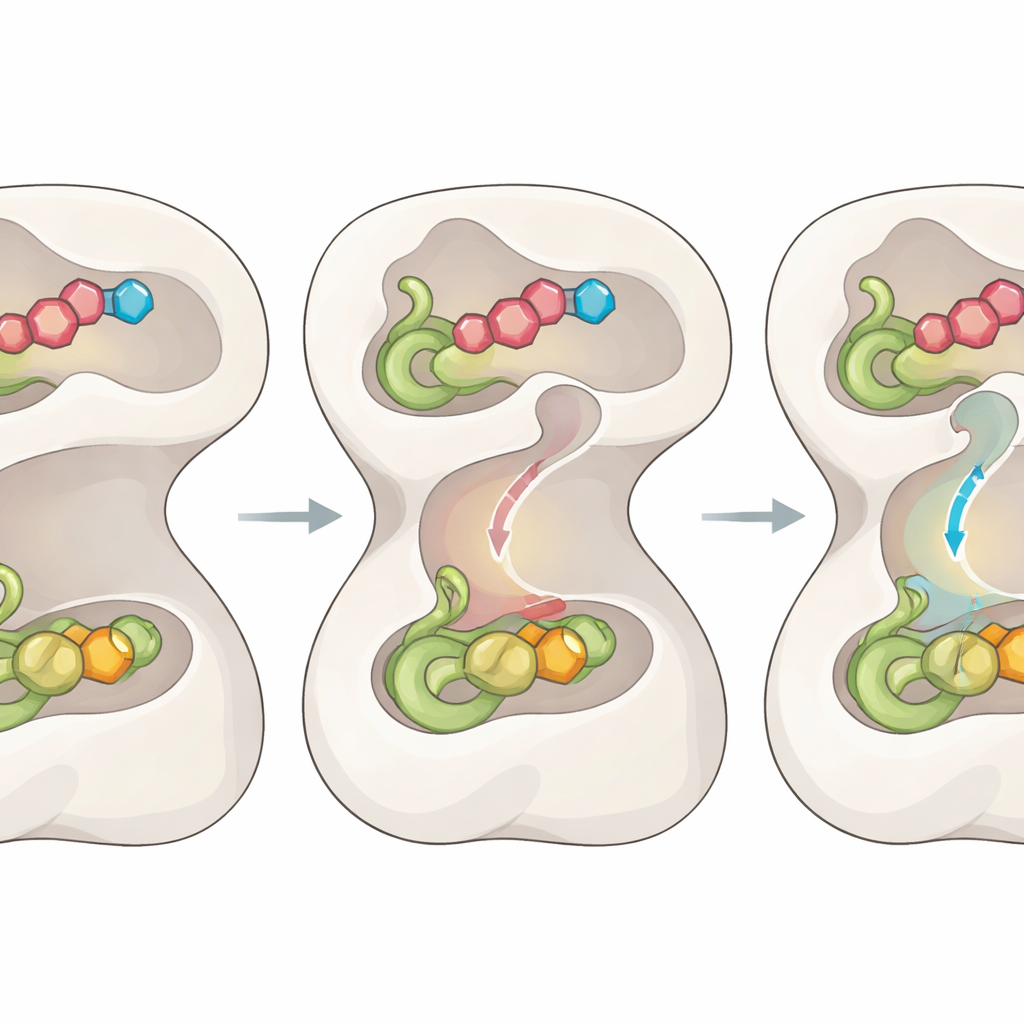
Da visão estrutural a vias terapêuticas
Ao acompanhar a FGAMS ao longo de seu ciclo catalítico, o estudo apresenta um quadro detalhado de como movimentos de domínios, alças flexíveis, portas internas e um túnel transitório estão todos interligados para coordenar a química. Para um público leigo, a conclusão é que a enzima funciona como uma pequena fábrica programável: ela só abre suas portas e a esteira interna quando todas as peças certas estão no lugar, garantindo rapidez e segurança. Como a FGAMS sustenta a produção de purinas em células cancerosas e está ligada a pior prognóstico em tumores hepáticos, os projetos estruturais e os pontos de controle recém‑identificados oferecem várias alavancas para desenhar fármacos que entupam o túnel, congelem as portas ou aprisionem intermediários-chave, potencialmente originando uma nova classe de terapias anticâncer direcionadas.
Citação: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
Palavras-chave: biossíntese de purinas, regulação alostérica, canalização de amônia, metabolismo do câncer, estrutura por crio‑ME