Clear Sky Science · pt
Regulação por realimentação negativa do sinal de STING por golgifagia dirigida por TAX1BP1
Como as células evitam uma reação imune exagerada
Nosso sistema imunológico precisa caminhar em uma corda bamba: deve reconhecer vírus invasores e DNA danificado rapidamente, mas também precisa desligar esse alarme antes que a inflamação descontrolada prejudique tecidos saudáveis. Este estudo revela como um ajudante celular pouco conhecido, TAX1BP1, atua como um freio embutido numa via de alarme potente chamada cGAS–STING. Ao explicar como as células desmontam esse alarme uma vez que ele cumpriu seu papel, o trabalho esclarece aspectos de doenças autoimunes, defesa antiviral e possíveis terapias contra o câncer.
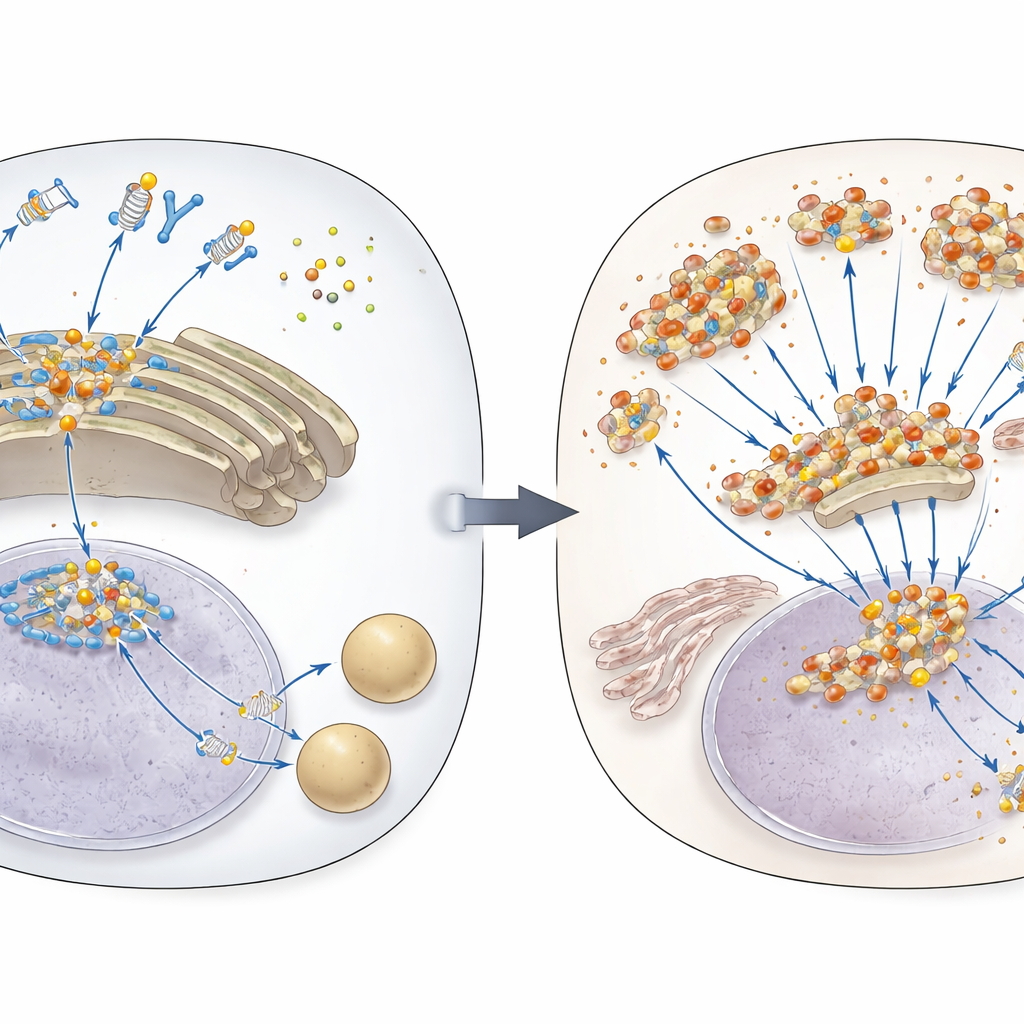
O sistema de alarme de DNA da célula
Quando DNA estranho ou fora do lugar aparece no fluido dentro das células, uma proteína sensora chamada cGAS o detecta e produz uma pequena molécula mensageira. Essa mensageira ativa STING, uma proteína tipo interruptor que vive em membranas internas. STING então viaja para um centro de distribuição celular chamado Golgi, onde se reúne em agregados e desencadeia a produção de moléculas antivirais conhecidas como interferons tipo I, juntamente com outros sinais inflamatórios. Como essa resposta é muito potente, as células normalmente degradam o STING após um curto período de atividade, direcionando-o para centros de reciclagem celular chamados lisossomos. Até agora, como o STING era marcado para essa etapa de desligamento havia sido compreendido apenas em parte.
Um freio celular com muitas funções
TAX1BP1 era conhecido anteriormente como um multitarefas que ajuda o sistema de descarte celular, a autofagia, a reconhecer material indesejado. Ele pode ligar-se tanto a cargas marcadas para remoção quanto aos sacos em formação que englobarão essas cargas. Os autores investigaram se o TAX1BP1 também poderia ajudar a conter o alarme cGAS–STING. Usando células do tipo imune humanas e macrófagos de camundongos sem TAX1BP1, eles descobriram que ativar cGAS ou STING produzia muito mais interferon e citocinas inflamatórias do que em células normais. Essas células deficientes em TAX1BP1 também eram mais resistentes à infecção pelo vírus herpes simplex, compatível com seu sinal antiviral hiperativado.
Limpeza do STING e de um Golgi estressado
Ao aprofundar, os pesquisadores mostraram que, sem TAX1BP1, o STING permanecia ativo por mais tempo e era degradado mais lentamente. Microscopia e testes bioquímicos revelaram que o STING ativo forma grandes agregados e que esses aglomerados se acumulam quando o TAX1BP1 está ausente. Ao mesmo tempo, a estrutura do Golgi incha e se fragmenta em pedaços. A equipe descobriu que o TAX1BP1, junto com outro auxiliar de reciclagem chamado p62, direciona esses fragmentos de Golgi danificados e os aglomerados de STING sobre eles para destruição em lisossomos — uma forma especializada de limpeza que os autores chamam de “golfifagia”. Esse processo é distinto da forma clássica e maciça de autofagia e, em vez disso, usa vias mais seletivas para capturar os pedaços sobrecarregados do Golgi.
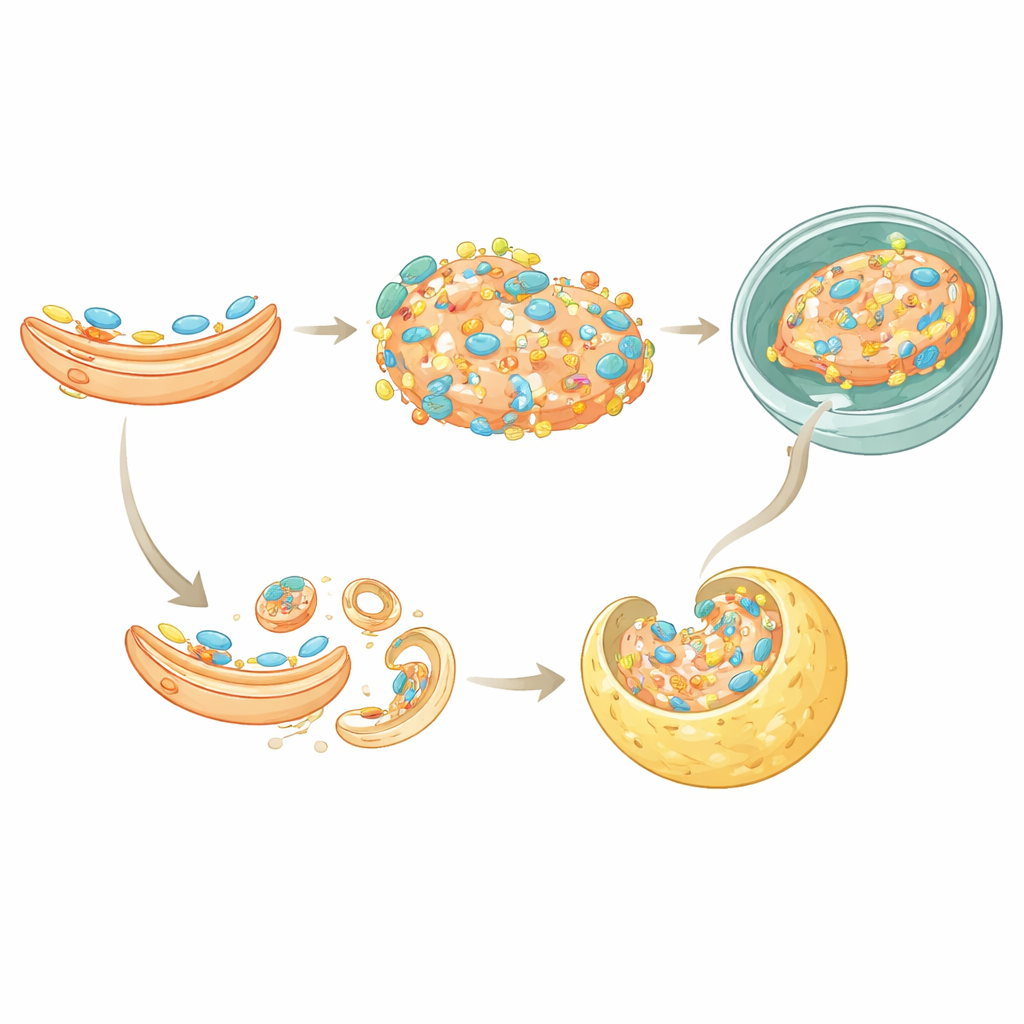
DuAS rotas para desligar o alarme
O estudo também revelou uma segunda maneira pela qual o TAX1BP1 ajuda a silenciar o STING. Normalmente, uma vez que o STING sinalizou no Golgi, ele é embalado em pequenas vesículas que se destacam e são reconhecidas por um sistema de triagem de proteínas chamado ESCRT, que então entrega o STING aos lisossomos. TAX1BP1 liga-se diretamente ao STING e ajuda sua interação com um componente chave do ESCRT, HGS. Quando o TAX1BP1 foi removido, a transferência do STING para essa maquinaria de triagem foi menos eficiente e sua degradação ficou mais lenta. Entretanto, alguma degradação ainda ocorreu, indicando que o TAX1BP1 atua ao lado do p62 nessa rota de microautofagia, dando às células modos parcialmente redundantes de garantir que o STING não permaneça ativo por tempo excessivo.
Por que isso importa para saúde e doença
Para testar a importância desse freio em animais vivos, os pesquisadores criaram camundongos sem TAX1BP1 especificamente em certas células imunes. Quando estimulados com uma droga ativadora de STING, esses camundongos apresentaram níveis mais altos de interferon e citocinas inflamatórias no sangue do que camundongos normais. Quando infectados com um poxvírus, apresentaram menor carga viral, mostrando resistência aumentada. Em conjunto, essas descobertas sugerem que TAX1BP1 conecta o momento de ativação do STING no Golgi a um desligamento temporizado por meio da destruição direcionada tanto do STING quanto das membranas do Golgi danificadas. Para um público leigo, a conclusão é que as células não apenas soam um alarme quando detectam DNA perigoso, mas também desmontam ativamente partes de sua própria fiação interna para garantir que o alarme seja desligado. Entender e, possivelmente, ajustar esse freio interno pode ajudar a projetar tratamentos para doenças inflamatórias crônicas, melhorar defesas antivirais ou modular respostas imunes no câncer.
Citação: Suklabaidya, S., Mohanty, S., Reider, I.E. et al. Negative feedback regulation of STING signaling by TAX1BP1-directed Golgiphagy. Nat Commun 17, 2762 (2026). https://doi.org/10.1038/s41467-026-69422-z
Palavras-chave: imunidade inata, via STING, autofagia, aparelho de Golgi, resposta antiviral