Clear Sky Science · pt
Mecanismo molecular de ação da pequena molécula SMT-738 no transportador de lipoproteínas bacteriano LolCDE
Por que este novo antibiótico é importante
À medida que mais infecções hospitalares resistem aos nossos melhores antibióticos, os médicos precisam com urgência de fármacos que eliminem bactérias perigosas sem destruir os microrganismos benéficos que convivem conosco. Este estudo desvenda como um composto experimental promissor, chamado SMT-738, bloqueia uma máquina de transporte crucial na camada externa de certas bactérias de difícil tratamento. Ao revelar exatamente onde e como esse fármaco emperra o maquinário, o trabalho aponta caminhos para antibióticos mais inteligentes que atinjam superbactérias ao mesmo tempo que preservem grande parte do microbioma intestinal.
A armadura externa das bactérias nocivas
Muitos dos patógenos mais preocupantes adquiridos em hospitais pertencem a um grupo conhecido como bactérias Gram-negativas. Elas são difíceis de matar porque se envolvem em uma armadura externa com dupla camada. Essa camada externa é construída e mantida por várias máquinas moleculares que movem blocos de construção essenciais da membrana interna, onde são fabricados, para a superfície. Um conjunto importante de cargas são as lipoproteínas, que ajudam a manter a integridade da camada externa e sustentam processos como captação de nutrientes e resistência a antibióticos. Um sistema de transporte chamado via Lol, e em particular uma bomba chamada LolCDE, extrai lipoproteínas da membrana interna e as entrega a chaperonas que as levam até a superfície externa. Como essas etapas são essenciais, elas constituem alvos atraentes para novos antibióticos.
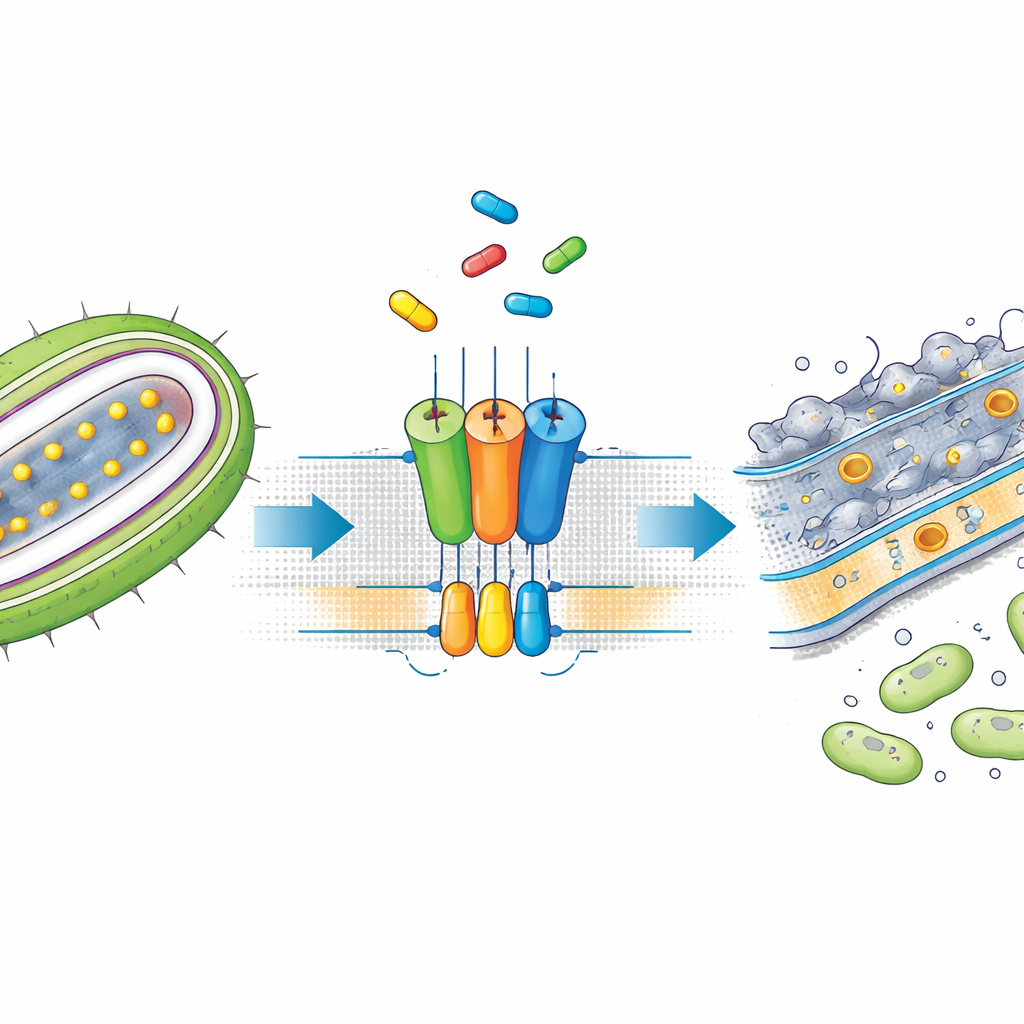
Uma pequena molécula que para a esteira
SMT-738 surgiu em triagens anteriores como um bloqueador potente de patógenos Gram-negativos da família Enterobacteriaceae, incluindo cepas multirresistentes de Escherichia coli e Klebsiella pneumoniae. Ainda assim, seu modo de ação preciso era incerto. Os autores primeiro mostraram que SMT-738 impede que uma lipoproteína de teste seja liberada pela LolCDE em bactérias engenheiradas, confirmando que o fármaco realmente paralisa a etapa de transporte. Importante, quando as bactérias carregavam certas mutações nos genes do complexo LolCDE, tornaram-se resistentes ao SMT-738, sugerindo que o composto atua ligando-se diretamente a essa bomba. Essas observações prepararam o terreno para um mergulho estrutural em como o composto interage com o transportador.
Travando a bomba por dentro
Usando microscopia eletrônica crio (cryo-EM) de alta resolução, os pesquisadores capturaram uma imagem tridimensional do LolCDE com SMT-738 travado no local. A estrutura mostra o fármaco encaixado em um bolso na extremidade periplásmica — o lado voltado para o espaço entre as membranas interna e externa — entre duas subunidades centrais, LolC e LolE. Esse sítio se sobrepõe à área de encaixe normal da carga de lipoproteína. Quando SMT-738 ocupa esse bolso, aminoácidos vizinhos em LolC e LolE mudam de posição em até cerca de um nanômetro. Esses movimentos criam colisões estéricas com onde a lipoproteína e suas caudas gordurosas normalmente se acomodariam, bloqueando efetivamente a entrada da carga na bomba. A mutação de muitos desses resíduos que revestem o bolso ou enfraqueceu a ligação ao fármaco ou conferiu resistência às bactérias, correspondendo perfeitamente ao retrato estrutural.
Desencadeando uma quebra unilateral
A história não termina no sítio de ligação. LolCDE é impulsionado por duas cópias de uma subunidade motora chamada LolD, que se situam do lado citoplasmático e gastam ATP para alimentar o transporte. Notavelmente, na estrutura com SMT-738 ligado, apenas uma LolD permanece associada; a parceira LolD dissociou-se. Géis bioquímicos e ensaios de ATPase confirmaram que a ligação de SMT-738 causa a perda de uma LolD e reduz fortemente a atividade de conversão de energia da bomba. Simulações computacionais do transportador em uma membrana reforçaram essa visão: à medida que SMT-738 se acomodava em seu bolso, mudanças conformacionais se propagavam para baixo, empurrando os helices de acoplamento que conectam LolC e LolE a LolD. Esses deslocamentos forçaram a LolD ligada a LolC para um choque desfavorável, fazendo com que ela se desprendesse, enquanto a LolD ligada a LolE permaneceu. O resultado é uma máquina assimétrica e «travada» que não pode mais movimentar lipoproteínas.
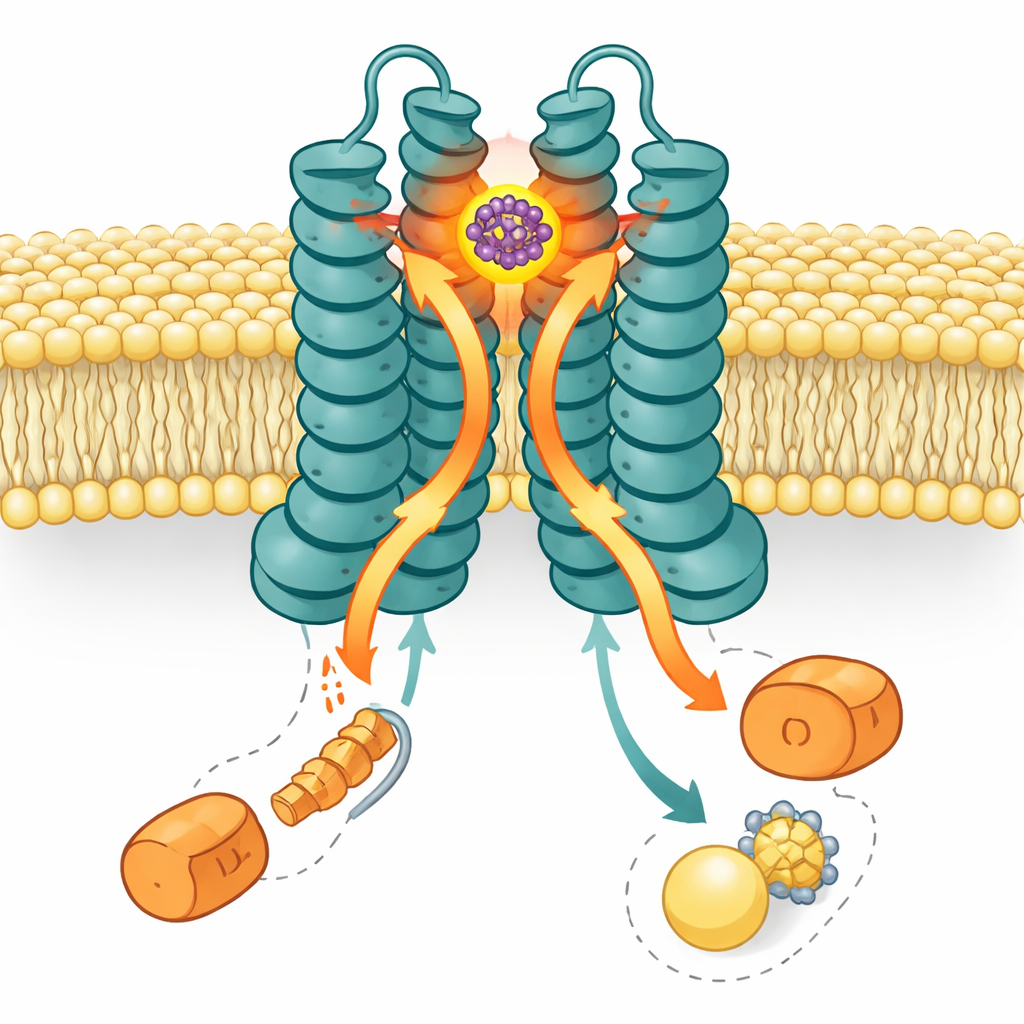
Por que algumas bactérias são atingidas e outras são poupadas
SMT-738 tem uma característica desejável: ataca fortemente Enterobacteriaceae resistentes a medicamentos, mas deixa muitas outras espécies Gram-negativas do intestino em grande parte intactas. Para entender essa seletividade, a equipe comparou sequências de LolE de bactérias suscetíveis e resistentes e concentrou-se em posições que fazem contato com SMT-738. Dois resíduos em LolE, especialmente um correspondente à posição D264 em E. coli, destacaram-se. Em patógenos sensíveis, essas posições coincidiam com a versão que contata o fármaco em E. coli, enquanto em muitos comensais resistentes do intestino foram substituídas por outros aminoácidos. Quando os pesquisadores engenheiraram E. coli para carregar tais substituições, as bactérias tornaram-se altamente resistentes ao SMT-738 enquanto ainda expressavam LolCDE. Simulações sugeriram que essas mudanças alteram a flexibilidade local ao redor do bolso, reduzindo a capacidade do SMT-738 de se ligar. Curiosamente, outro inibidor de LolCDE, a lolamicina, dependia de pontos de contato apenas parcialmente sobrepostos e mostrou um padrão de resistência diferente, indicando maneiras distintas de atingir a mesma bomba.
Novos projetos para futuros antibióticos
Ao combinar imagens estruturais, varreduras por mutação, testes bioquímicos e simulações computacionais, este trabalho mostra que SMT-738 não é apenas uma tampão em um canal. Em vez disso, ele se prende ao lado periplásmico da bomba LolCDE, bloqueia o sítio de entrada da lipoproteína e então desencadeia mudanças de longo alcance que derrubam uma das duas unidades motoras, congelando o transportador em um estado inativo. Esse mecanismo de «travamento alostérico» representa uma nova forma de desativar uma máquina bacteriana e ajuda a explicar por que o SMT-738 pode mirar em patógenos perigosos enquanto poupa grande parte do microbioma. O mapa detalhado do bolso de ligação e o resíduo chave de seletividade em LolE agora oferecem um roteiro racional para projetar a próxima geração de antibióticos que explorem a mesma vulnerabilidade com ainda maior potência e precisão.
Citação: Li, H., Zhu, X., Zhang, D. et al. Molecular mechanism of action of small molecule SMT-738 on bacterial lipoprotein transporter LolCDE. Nat Commun 17, 2540 (2026). https://doi.org/10.1038/s41467-026-69411-2
Palavras-chave: resistência a antibióticos, bactérias Gram-negativas, transporte de lipoproteínas, inibidor de LolCDE, estrutura por crio-ME