Clear Sky Science · pt
O fotoliase/criptocromo de Aspergillus nidulans detecta estresse oxidativo e se desloca do núcleo para as mitocôndrias
Como os fungos percebem luz e estresse
A luz solar mantém plantas e fungos vivos, mas também traz perigos como danos ao DNA e compostos oxigenados nocivos. Este estudo investiga como um fungo comum, Aspergillus nidulans, usa uma única proteína, chamada CryA, para perceber tanto a luz quanto o estresse oxidativo e para se proteger. Compreender esse “sensor duplo” não apenas aprofunda nosso conhecimento sobre como microrganismos lidam com ambientes adversos, como também pode esclarecer como células, em geral, coordenam sinais entre o núcleo e as mitocôndrias produtoras de energia.
Uma enzima de reparo dependente de luz azul com papel oculto
CryA pertence a uma família de proteínas conhecidas por reparar danos no DNA causados pela luz ultravioleta. Essas proteínas, chamadas fotoliases e criptocromos, usam uma molécula absorvedora de luz (um flavina) para captar luz azul e consertar bases de DNA danificadas. Os pesquisadores confirmaram que CryA tem a arquitetura clássica de uma enzima de reparo de DNA, liga os cofatores usuais de captação de luz e se agrupa com fotoliases conhecidas em árvores evolutivas. Somente por isso, CryA pareceria uma ferramenta de reparo rotineira. No entanto, trabalhos anteriores sugeriam que ela também influencia o desenvolvimento do fungo, comportando-se mais como um interruptor regulado pela luz do que como um mero componente mecânico.
Um regulador mestre para genes sensíveis à luz
Para desvendar o lado regulatório de CryA, a equipe rastreou sua localização celular e como alterar sua quantidade modifica o crescimento fúngico. Descobriram que, em condições normais, CryA se acumula no núcleo, onde o DNA está armazenado. Quando o gene cryA foi removido, o fungo produziu mais estruturas sexuais; quando CryA foi superexpresso, quase bloqueou totalmente a formação das usuais esporas assexuadas, deixando colônias pálidas e felpudas. Testes de expressão gênica mostraram que muitos genes ativados pela luz e relacionados ao desenvolvimento eram excessivamente ativados sem CryA e insuficientemente ativados quando CryA estava em excesso. Juntos, esses resultados revelam CryA como um elemento de retroalimentação negativa: a luz eleva os níveis de cryA, CryA então migra para o núcleo e freia genes induzidos pela luz e pelo desenvolvimento, impedindo que a resposta fuja ao controle. 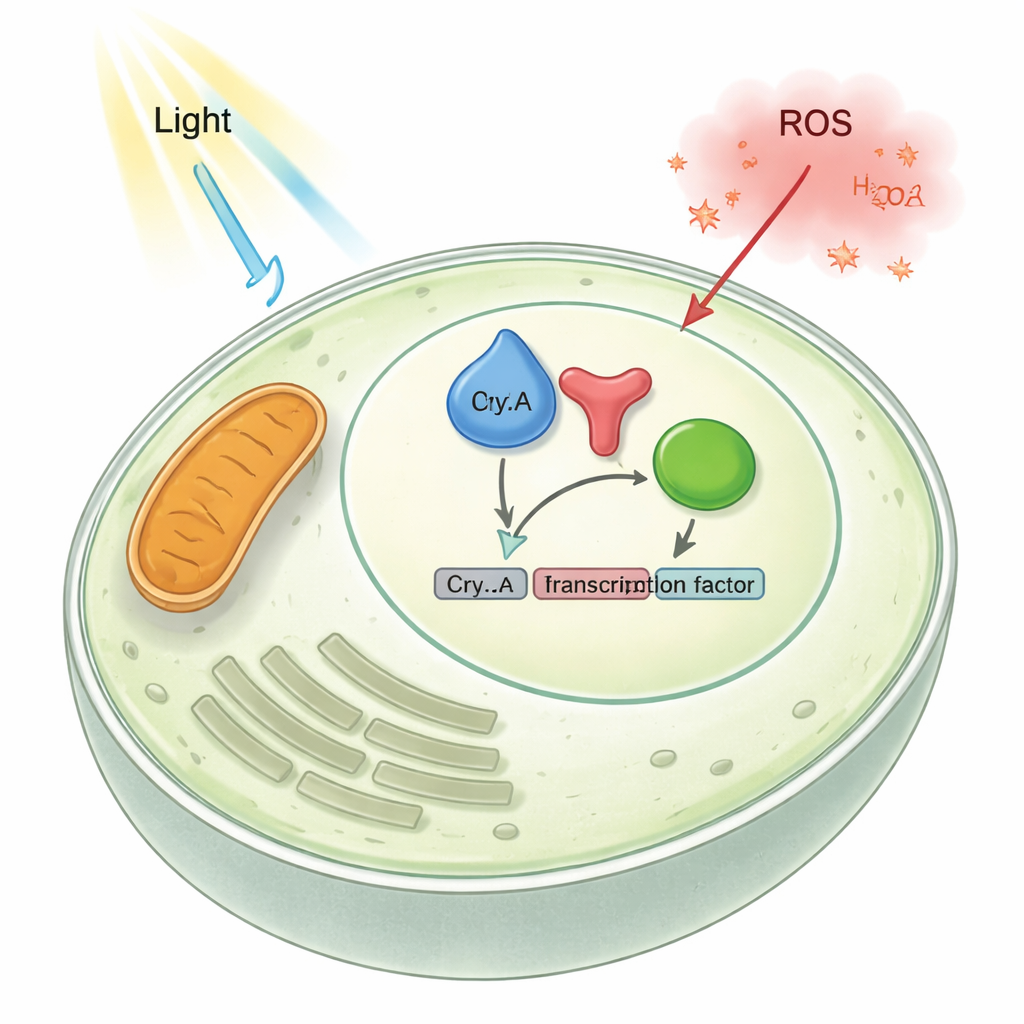
Crosstalk com as principais vias de luz e estresse
O fungo já depende de outro fotoreceptor, um sensor de luz vermelha chamado fitocromo (FphA), e de uma via de estresse que termina em um fator de transcrição chamado AtfA. Usando testes de interação proteína–proteína em células vivas e com proteínas purificadas, os pesquisadores mostraram que CryA se liga fisicamente tanto a FphA quanto a AtfA no núcleo. Quando cryA foi deletado, genes normalmente ativados pela luz vermelha via fitocromo foram expressos mais fortemente; quando cryA foi superexpresso, tornaram-se mais difíceis de ativar. Experimentos com cromatina indicaram que, na ausência de CryA, um gene chave responsivo à luz apresenta mais marcas de histona associadas à ativação, sugerindo que CryA normalmente atenua a atividade de abertura da cromatina dirigida pelo fitocromo. Em efeito, CryA reprime tanto o sensor de luz quanto o fator de transcrição a jusante, atuando como um freio compartilhado para os sinais de luz e estresse.
Um sensor rápido de estresse que salta para as mitocôndrias
O estresse oxidativo — um excesso de espécies reativas de oxigênio como o peróxido de hidrogênio — representa uma ameaça constante às células. Os autores descobriram que esse estresse, assim como a luz, aumenta a expressão de cryA. Notavelmente, quando peróxido de hidrogênio foi adicionado, CryA mudou do núcleo para as mitocôndrias em menos de um minuto. Essa translocação exigia uma extensão curta e flexível na extremidade N-terminal da proteína e, em particular, uma única cisteína dentro dela. Quando essa cisteína foi substituída por outro resíduo, CryA não conseguiu mais sair do núcleo sob estresse. Truncar a cauda N-terminal forçou CryA a residir permanentemente nas mitocôndrias. Essas linhagens modificadas responderam de modo diferente aos oxidantes: versões de CryA restritas ao núcleo ou às mitocôndrias alteraram a resistência do fungo ao peróxido de hidrogênio e à menadiona e remodelaram a expressão de genes antioxidantes. As descobertas sugerem que CryA faz mais do que detectar estresse — pode ajudar a coordenar a comunicação entre mitocôndrias e núcleo para que as defesas antioxidantes sejam ajustadas ao tipo e ao nível de dano. 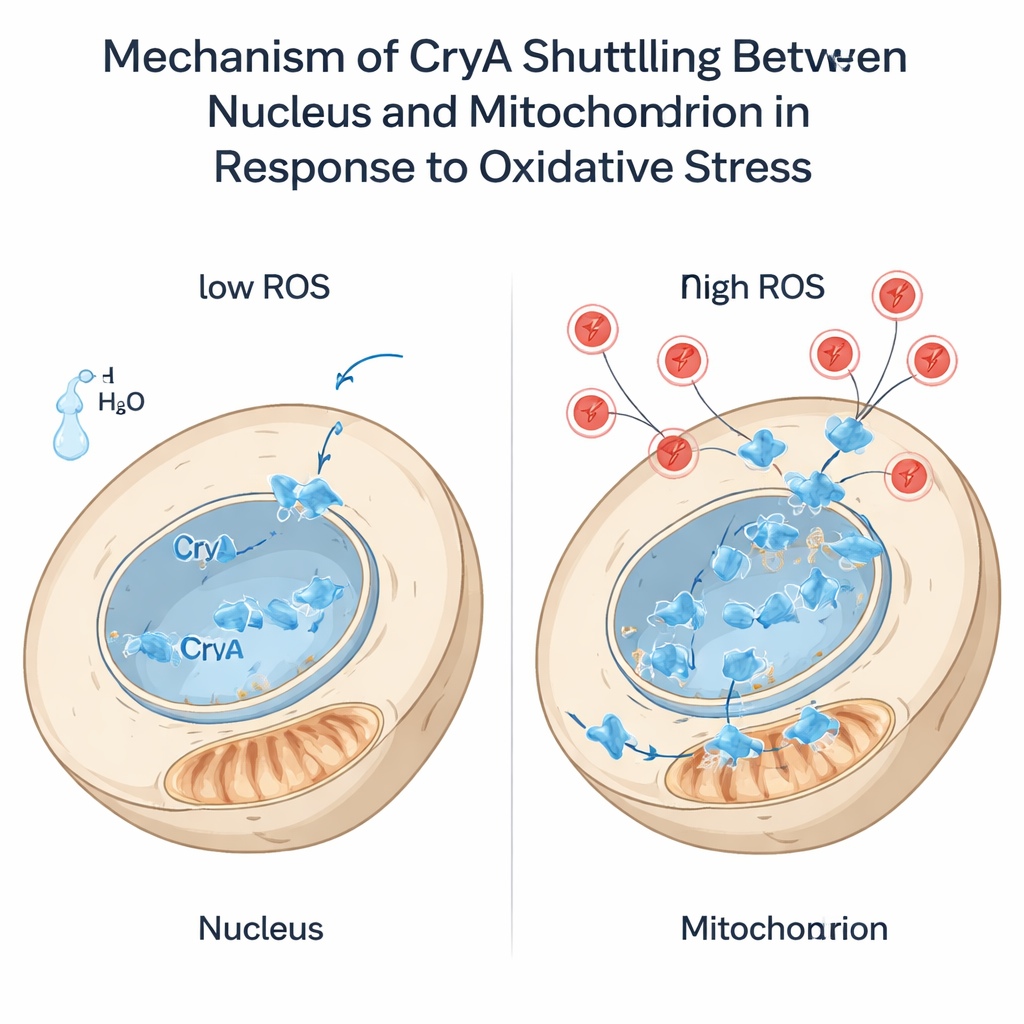
Por que isso importa
Para um não-especialista, CryA pode ser visto como um guarda de trânsito celular que observa tanto a luz externa quanto o estresse oxidativo interno e decide quando reduzir o crescimento, o desenvolvimento e a atividade gênica. Ao fazer transporte entre o núcleo e as mitocôndrias e ao conectar-se a vias de sinalização importantes, ela impede que o fungo reaja em excesso à luz ou ao estresse, ao mesmo tempo em que permite uma resposta protetora rápida. Proteínas e mecanismos similares existem em muitos organismos, portanto este trabalho oferece uma janela sobre como células vivas integram sinais ambientais com sinais de dano interno para sobreviver em um mundo em mudança.
Citação: Landmark, A., Rudolf, T., Hundshammer, K. et al. The photolyase/cryptochrome of Aspergillus nidulans senses oxidative stress and shuttles from nuclei to mitochondria. Nat Commun 17, 1483 (2026). https://doi.org/10.1038/s41467-026-69403-2
Palavras-chave: detecção de luz, estresse oxidativo, criptocromo, mitocôndrias, desenvolvimento fúngico