Clear Sky Science · pt
O lactato derivado de macrófagos direciona o remodelamento fenotípico de fibroblastos dérmicos via lactilação da lisina 23 da histona H3 primed por MCT1 em cicatriz hipertrófica
Por que algumas cicatrizes crescem espessas e elevadas
A maioria dos cortes e queimaduras eventualmente se atenua em cicatrizes finas e planas. Mas algumas feridas cicatrizam formando faixas espessas e elevadas de tecido chamadas cicatrizes hipertróficas, que podem coçar, doer e limitar o movimento. Este estudo revela um motor inesperado dessas cicatrizes persistentes: um subproduto metabólico comum chamado lactato, produzido por células imunes em pele rígida em processo de cicatrização, que reprograma células reparadoras vizinhas para comportar-se de maneira mais agressiva e pró-cicatrização.
Da reparação normal à cicatriz problemática
Na cicatrização saudável, as células da pele trabalham juntas para fechar a lesão e reconstruir o tecido. Os fibroblastos, as principais células de reparo da camada mais profunda da pele, fazem uma transição breve para uma forma mais ativa que sintetiza colágeno, a estrutura proteica da pele. Uma vez que a ferida é selada, essas células se acalmam novamente. Nas cicatrizes hipertróficas, entretanto, os fibroblastos permanecem presos nesse estado hiperativo, depositando colágeno em excesso em feixes espessos e desorganizados. Os autores começaram comparando pele normal com tecido de cicatriz hipertrófica e encontraram uma mudança metabólica clara: o microambiente da cicatriz favorecia uma química rápida de queima de açúcar que gera grandes quantidades de lactato, juntamente com altos níveis de uma proteína de transporte chamada MCT1, que conduz lactato para dentro das células. 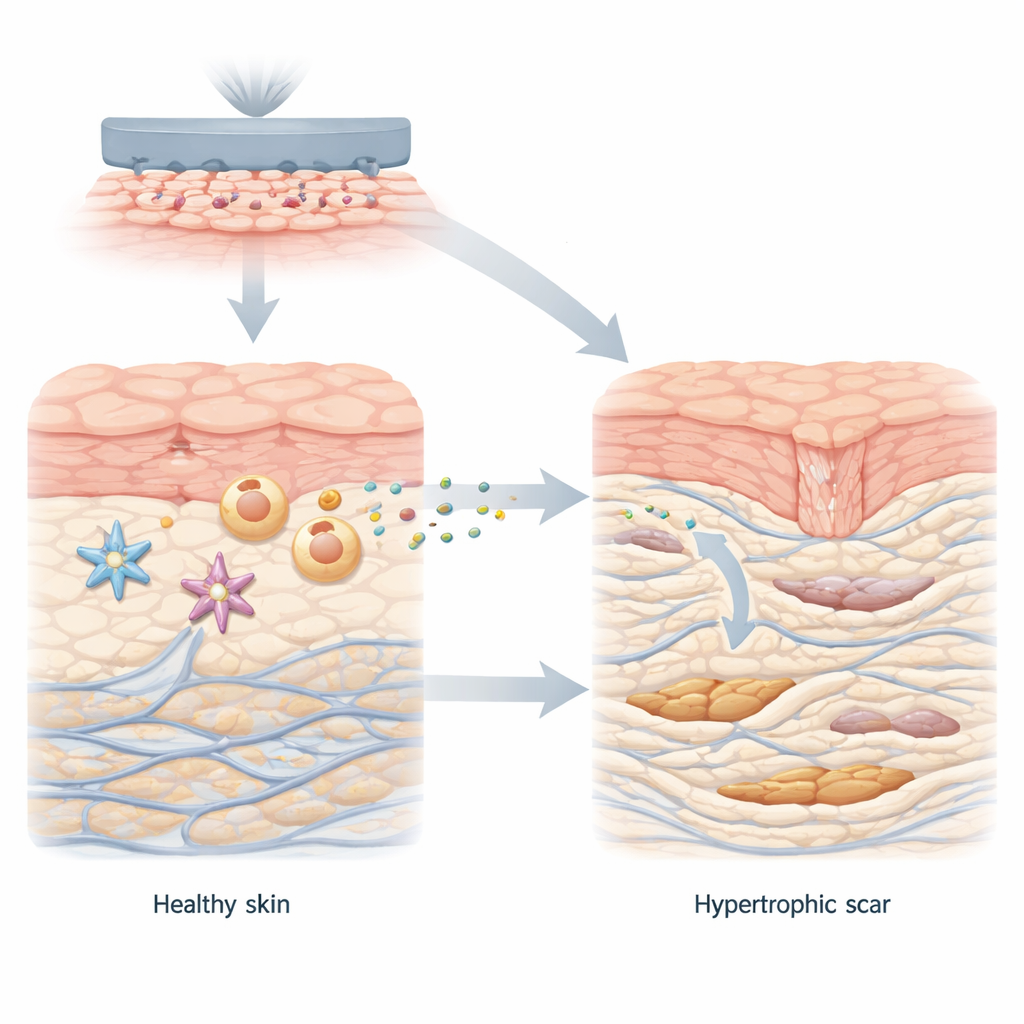
Células imunes como fábricas inesperadas de lactato
Para descobrir de onde vinha todo esse lactato, a equipe examinou diferentes tipos celulares da pele humana e de modelos em camundongos: macrófagos (células imunes que removem detritos e coordenam a cicatrização), células dos vasos sanguíneos e fibroblastos. Eles cultivaram essas células em materiais macios ou rígidos que imitam pele normal e cicatrizada. Em superfícies rígidas, apenas os macrófagos mudaram para um modo altamente glicolítico, faminto por açúcar, e liberaram grandes quantidades de lactato, tanto em placas de cultura quanto em tecido de cicatriz real. Quando os macrófagos foram removidos de feridas em cicatrização em camundongos, os níveis de lactato tecidual caíram e a formação de cicatriz diminuiu. Esses resultados apontam os macrófagos, especialmente os que percebem um ambiente rígido, como as principais fábricas de lactato que moldam o microambiente da cicatriz.
Lactato como sinal que reconfigura fibroblastos
Em seguida, os pesquisadores investigaram como esse excesso de lactato afeta os fibroblastos. Quando fibroblastos foram expostos a fluido rico em lactato proveniente de macrófagos cultivados em substratos rígidos, eles se multiplicaram mais rapidamente, movimentaram-se mais e produziram mais colágeno — todas características do estado agressivo de miofibroblasto. Bloquear o transportador MCT1 nos fibroblastos, ou reduzir a produção de lactato nos macrófagos, diminuiu fortemente essas alterações. Dentro dos fibroblastos, o lactato entrante fez mais do que alimentar a produção de energia: desencadeou uma marca química específica nas proteínas histonas, que embalam o DNA no núcleo celular. Essa marca, chamada lactilação de H3K23, estava muito mais presente em fibroblastos formadores de cicatriz do que em fibroblastos normais e atuava como um interruptor que ativava dois genes-chave, HEY2 e COL11A1, que juntos amplificam os sinais pró-cicatrização.
Um ciclo autorreforçador de cicatrização
As proteínas induzidas por essa marca de histona formam um loop de feedback poderoso. HEY2 aumenta a atividade de uma via envolvendo YAP1 e SMAD2, conhecida por empurrar os fibroblastos para um estado mais contrátil e produtor de colágeno. COL11A1, uma proteína estrutural relacionada ao colágeno, interage fisicamente com o transportador MCT1 nos fibroblastos, ajudando a estabilizá-lo e a tornar a captação de lactato mais eficiente. Em outras palavras, o lactato que entra na célula muda a regulação gênica de modo a aumentar ainda mais a entrada de lactato e a produção de colágeno, prendendo os fibroblastos em uma identidade pró-cicatriz. 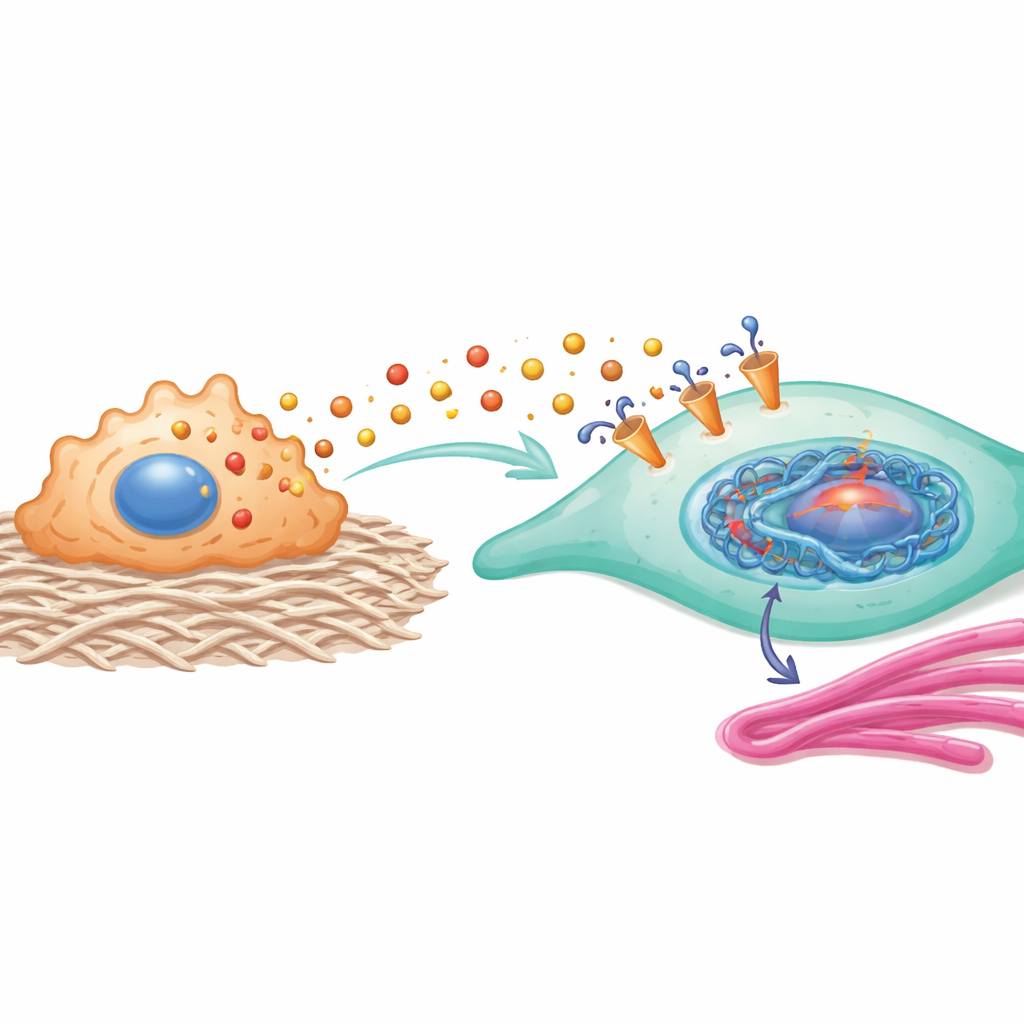
Atenuando o ciclo para melhorar a cicatrização
Para testar se interromper esse ciclo pode melhorar a cicatrização, a equipe usou camundongos nos quais o MCT1 podia ser removido seletivamente dos fibroblastos, além de um fármaco que bloqueia o MCT1. Em ambos os casos, as feridas fecharam mais rápido, a pele recém-formada parecia mais organizada e as fibras de colágeno foram mais finas e melhor alinhadas, com menos características de cicatriz hipertrófica. A marca específica da histona e seus genes a jusante também diminuíram. Depleção de macrófagos, a principal fonte de lactato, ou redução química do lactato teve efeitos anti-cicatriz semelhantes. Esses experimentos mostram que a cadeia ferida-rígida–macrófago–lactato–fibroblasto não é apenas uma correlação, mas um motor chave da cicatrização patológica.
O que isso significa para tratamentos futuros de cicatrizes
Este trabalho reposiciona o lactato de um simples resíduo metabólico para um mensageiro poderoso que conecta mecânica, metabolismo e controle gênico na cicatrização. Ao mostrar como o lactato derivado de macrófagos, transportado pelo MCT1, altera histonas e ativa um programa de cicatrização autorreforçador nos fibroblastos, o estudo destaca vários alvos terapêuticos promissores. Drogas que modulam a produção de lactato, bloqueiam o MCT1 ou interferem com a modificação histona específica podem um dia ajudar feridas a cicatrizarem mais rapidamente e com cicatrizes mais planas e menos perceptíveis.
Citação: Yuan, Y., Xiao, Y., Zou, J. et al. Lactate derived from macrophages drives skin dermal fibroblasts phenotypic remodeling via MCT1-primed histone H3 lysine 23 lactylation in hypertrophic scar. Nat Commun 17, 2694 (2026). https://doi.org/10.1038/s41467-026-69388-y
Palavras-chave: cicatriz hipertrófica, sinalização por lactato, crosstalk macrófago–fibroblasto, lactilação de histonas, terapia para cicatrização de feridas