Clear Sky Science · pt
A mioferlina é um componente de vesículas de transporte vRNP em estágio avançado para vírus de RNA envelopados
Por que isso importa para a saúde cotidiana
A gripe sazonal e outras infecções respiratórias podem parecer rotineiras, mas juntas matam milhões de pessoas no mundo a cada ano. Muitos desses vírus, incluindo o influenza A e o vírus sincicial respiratório (VSR), já driblam vacinas e antivirais ao mutar rapidamente. Este estudo foca em vez disso em algo que os vírus não conseguem mudar facilmente: a maquinaria celular humana que eles sequestram para sair das células infectadas. Ao descobrir um ponto fraco compartilhado nessa maquinaria, o trabalho aponta para medicamentos futuros que poderiam enfraquecer de uma só vez uma ampla gama de vírus respiratórios.
Uma rota celular de transporte que os vírus exploram
Nossas células das vias aéreas reutilizam constantemente porções da membrana externa por meio de um processo chamado reciclagem. Pequenas bolhas de membrana, ou vesículas, transportam cargas do interior da célula de volta à superfície, guiadas por uma família de proteínas conhecidas coletivamente como Rab11. O vírus influenza A, o VSR e um vírus relacionado chamado vírus de Sendai exploram essa rota em estágios avançados da infecção. Eles carregam seu material genético, empacotado como complexos ribonucleoproteicos, em vesículas que contêm Rab11, que o levam ao lado apical (voltado para a via aérea) da célula, onde novas partículas virais brotam e se espalham. Até agora, Rab11 era o único fator do hospedeiro claramente compartilhado por essas vesículas de transporte, deixando uma grande lacuna na compreensão de como elas se formam e funcionam.
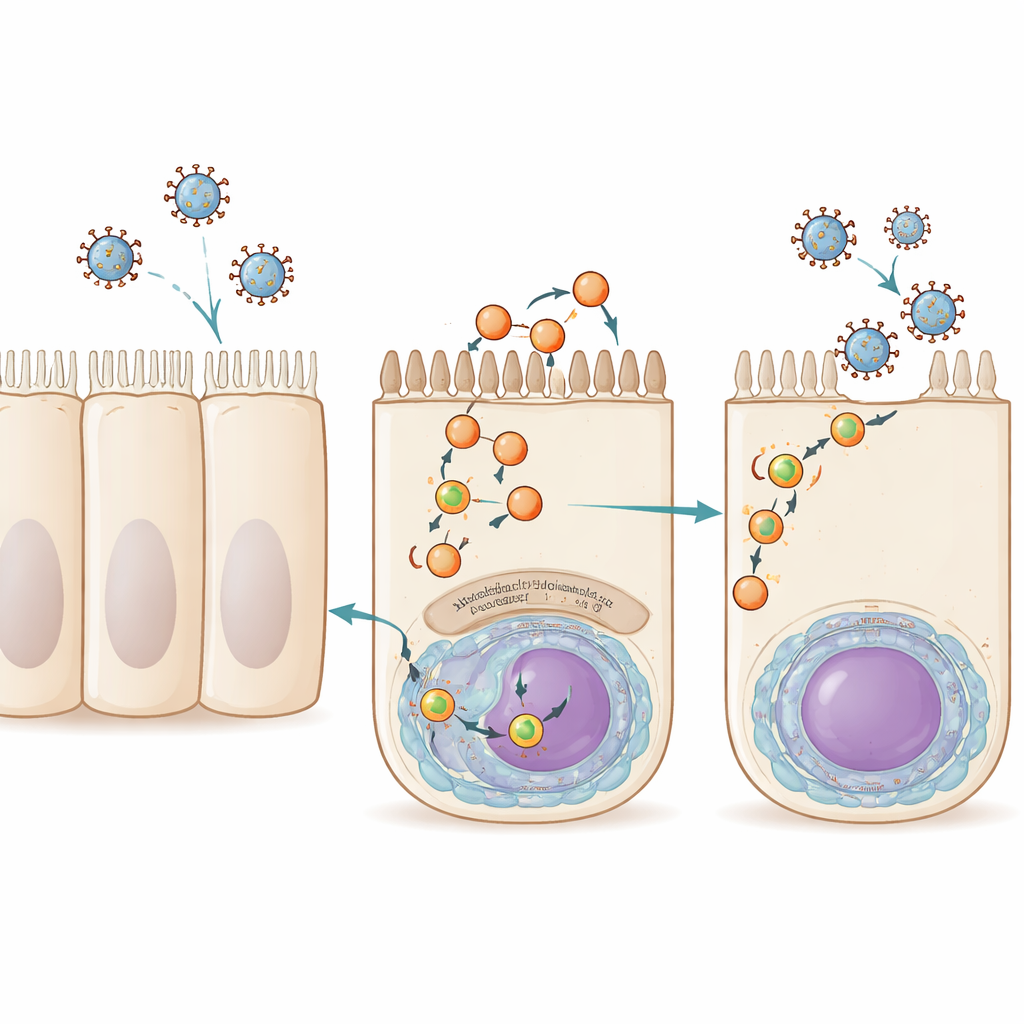
Encontrando um novo ator: a mioferlina
Os pesquisadores começaram perguntando quais proteínas humanas se associam fisicamente à maquinaria de empacotamento do genoma do influenza em diferentes momentos da infecção. Eles criaram um vírus influenza A cuja polimerase carregava uma etiqueta molecular e, em seguida, usaram espectrometria de massas para catalogar proteínas humanas ligadas a esse complexo no início e no fim da infecção. Entre centenas de candidatos, um se destacou nos pontos tardios: a mioferlina, uma grande proteína associada à membrana previamente ligada ao desenvolvimento muscular, endocitose e reparo de membrana. Quando a equipe reduziu os níveis de mioferlina em células derivadas do pulmão usando pequenos RNAs interferentes ou a bloqueou com um inibidor de pequena molécula, as células ainda produziram RNA viral e proteínas virais normalmente, mas liberaram muito menos partículas infectantes de influenza. Isso indicou que a mioferlina não é necessária para a cópia do genoma viral, mas é crucial para os estágios posteriores, quando novos vírus são montados e saem da célula.
A mioferlina viaja com a carga viral
Imagens de alta resolução revelaram onde a mioferlina se localiza durante a infecção. Em células não infectadas, a mioferlina se sobrepõe em grande parte às vesículas de reciclagem positivas para Rab11, tanto perto do núcleo quanto em direção à periferia celular, e a perda de qualquer uma das proteínas perturba a distribuição normal da outra. Durante a infecção por influenza, a rede Rab11 é dramaticamente remodelada em vesículas alargadas e irregulares que carregam ribonucleoproteínas virais. A mioferlina é mantida nessas vesículas remodeladas e mostra forte colocalização com o genoma viral e Rab11. Quando a equipe usou um fármaco que força os complexos de genoma viral e suas vesículas transportadoras a se aglomerarem, a mioferlina foi puxada para os mesmos agregados, confirmando que é um componente intrínseco dessas estruturas de transporte em estágio avançado e não apenas uma presença fortuita nas proximidades.
Um núcleo compartilhado por múltiplos vírus respiratórios
O estudo então investigou se essa dependência da mioferlina é única do influenza ou mais amplamente compartilhada. A redução da mioferlina em células pulmonares infectadas com VSR ou vírus de Sendai novamente causou uma forte queda na liberação de vírus infectantes, sem reduzir os níveis de RNA viral. Imagens de molécula única mostraram os genomas de ambos os vírus se agrupando junto com mioferlina e Rab11 em pontos citoplasmáticos que provavelmente representam centros de transporte, em vez de fábricas de replicação. Esse padrão apoia um quadro unificador: diferentes vírus respiratórios de RNA envelopados, apesar de estilos de vida diversos, convergem no mesmo sistema de vesículas Rab11–mioferlina quando chega a hora de mover seus genomas completos em direção à superfície celular para empacotamento e saída.
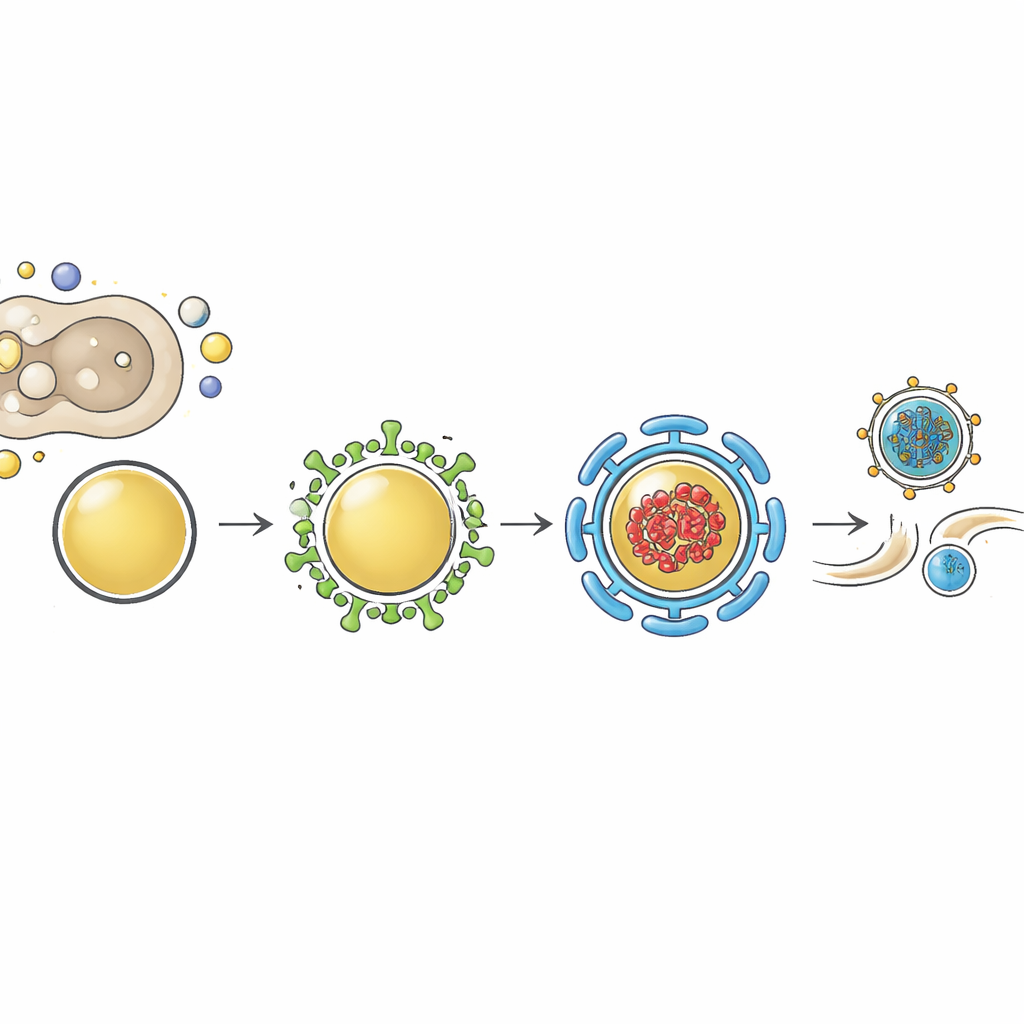
Como a mioferlina molda as vesículas que carregam vírus
A mioferlina é composta por múltiplos domínios "C2" que podem ligar-se a membranas e a proteínas parceiras. Trabalhos anteriores mostraram que um desses domínios interage com uma família de proteínas remodeladoras de membrana chamadas EHDs. Neste estudo, EHD1 e EHD2 marcados fluorescentemente foram encontrados dentro das mesmas vesículas remodeladas que carregam genomas de influenza e Rab11, especialmente quando essas vesículas foram experimentalmente agrupadas. A redução dos níveis de EHD2, assim como a redução da mioferlina, diminuiu os rendimentos de influenza sem afetar a replicação do genoma. Além disso, a remoção da mioferlina causou queda nos níveis de proteína EHD2, sugerindo que a mioferlina ajuda a estabilizar ou posicionar corretamente o EHD2 nas membranas. Os autores propõem que a mioferlina se situa em vesículas positivas para Rab11 e recruta proteínas EHD para esculpir suas membranas, completando a formação de "vesículas revestidas irregularmente" especializadas que são otimizadas para transportar carga viral até os locais de brotamento.
O que isso significa para estratégias antivirais futuras
Em conjunto, os achados posicionam a mioferlina como uma organizadora central de uma via de reciclagem do hospedeiro da qual muitos vírus respiratórios envelopados dependem em um passo crítico tardio. Como atingir apenas proteínas virais frequentemente leva à resistência rápida, fatores do hospedeiro reutilizados por múltiplos vírus são alvos de drogas atraentes. Interferir na função da mioferlina, ou em sua parceria com Rab11 e proteínas EHD, poderia em princípio retardar ou bloquear a disseminação de patógenos diversos, desde influenza e VSR até outros vírus dependentes de Rab11, como alguns coronavírus. Resta muito trabalho para traduzir esse conceito em terapias seguras, mas o estudo fornece um mapa detalhado de uma rota viral de escape compartilhada — e destaca a mioferlina como um ponto de estrangulamento promissor ao longo desse caminho.
Citação: Bonazza, S., Turkington, H.L., Sukumar, S. et al. Myoferlin is a component of late-stage vRNP trafficking vesicles for enveloped RNA viruses. Nat Commun 17, 2507 (2026). https://doi.org/10.1038/s41467-026-69386-0
Palavras-chave: gripe, vírus respiratórios, transporte vesicular, fatores hospedeiro, mioferlina