Clear Sky Science · pt
Defeitos estruturais nos fibrilos de amilóide-β impulsionam a nucleação secundária
Por que pequenas falhas em proteínas cerebrais importam
Na doença de Alzheimer e em doenças cerebrais relacionadas, certas proteínas se agregam em estruturas longas e filiformes chamadas fibrilos amilóides. Esses fibrilos não apenas marcam a doença; eles também ajudam a gerar novas partículas proteicas altamente tóxicas que podem prejudicar neurônios. Este estudo faz uma pergunta simples, porém poderosa: falhas estruturais raras dentro dos fibrilos amilóides atuam como os principais pontos quentes que desencadeiam novo crescimento nocivo? A resposta pode indicar maneiras de desacelerar ou interromper esses distúrbios ao mirar apenas alguns locais críticos, em vez de toda a superfície da proteína. 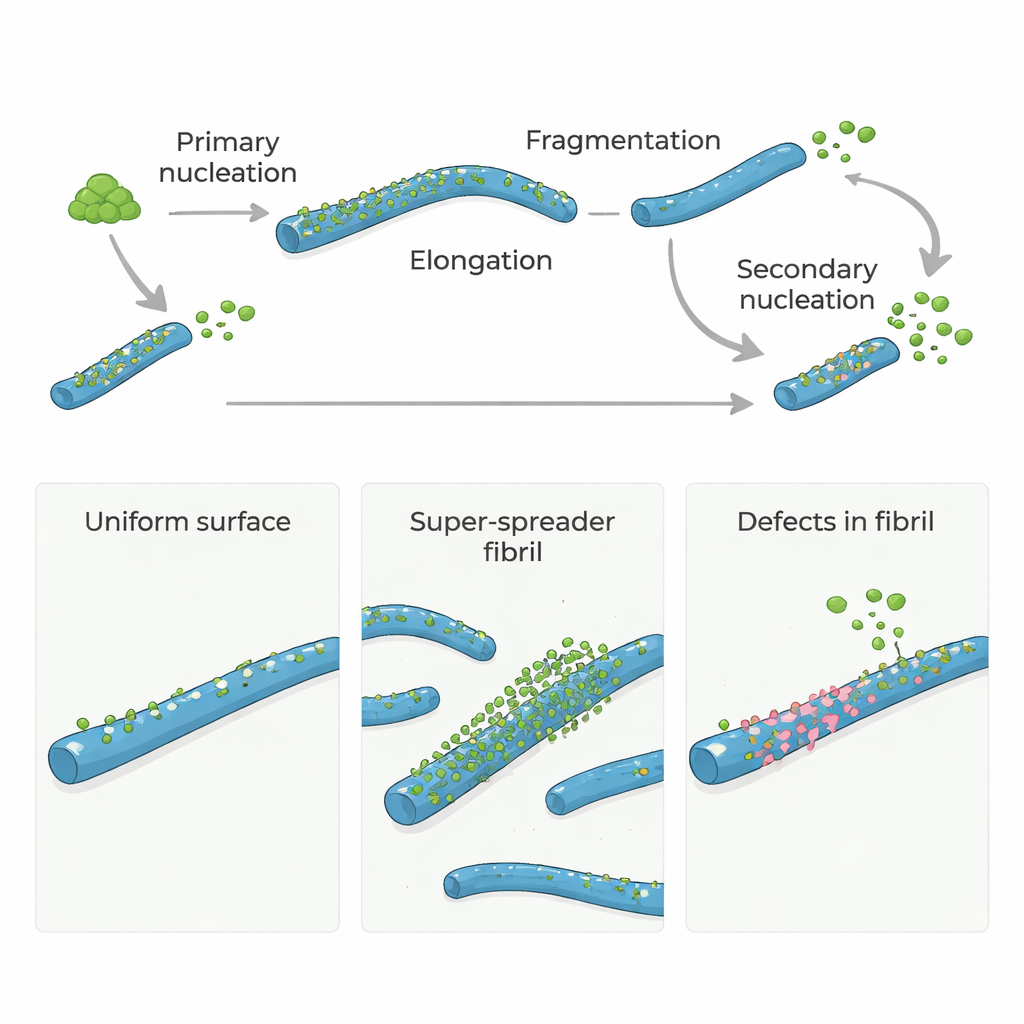
De proteína inerte a reação em cadeia descontrolada
As proteínas amilóide-β (Aβ), centrais na doença de Alzheimer, normalmente não formam agregados sozinhas muito rapidamente. Para começar, alguns monômeros precisam se montar lentamente nos primeiros fibrilos, um passo chamado nucleação primária. Uma vez que esses fibrilos iniciais existem, eles crescem rapidamente à medida que mais monômeros se adicionam às suas extremidades. Ainda mais importante, fibrilos existentes podem desencadear o surgimento de novos fibrilos em suas superfícies por um processo conhecido como nucleação secundária. Esse passo impulsionado pela superfície pode inundar o sistema com novos fibrilos e oligômeros pequenos e tóxicos, transformando um gotejamento lento em uma reação em cadeia descontrolada.
Todas as superfícies dos fibrilos são igualmente perigosas?
Muitos modelos pressupuseram que toda a superfície de um fibrilo amilóide é igualmente eficiente em catalisar a nucleação secundária. No entanto, experimentos recentes sugeriram que apenas uma pequena fração da superfície é realmente ativa. Para investigar isso, os autores utilizaram uma "chaperona" molecular natural chamada Brichos, conhecida por bloquear a nucleação secundária de Aβ40 e Aβ42 (duas formas-chave da amilóide-β). Medindo cuidadosamente quanto Brichos marcado com fluorescência se prende aos fibrilos, eles descobriram que a ligação é forte, mas em números muito baixos: aproximadamente uma molécula de Brichos para cada 100–150 moléculas de Aβ em um fibrilo. Ainda assim, essa cobertura esparsa foi suficiente para suprimir mais de 90% da nucleação secundária, o que significa que apenas sítios raros e localizados — em vez da superfície inteira — dominam a produção de novas assembléias tóxicas.
Investigando o papel de defeitos ocultos
Esses achados sugeriram que os sítios cruciais de nucleação podem ser defeitos estruturais — pequenas irregularidades formadas à medida que os fibrilos crescem, como camadas desalinhadas ou núcleos internos parcialmente expostos. Para testar essa ideia diretamente, os pesquisadores cultivaram fibrilos de Aβ40 em duas condições diferentes. Um conjunto, os fibrilos de "controle", foi formado sob condições tipicamente fortemente supersaturadas que favorecem crescimento rápido e aprisionamento cinético de defeitos. O outro conjunto foi criado usando um protocolo de recozimento lento e controlado por temperatura: os fibrilos foram crescidos com uma força motriz efetiva muito baixa, próxima ao seu limite de solubilidade, onde estruturas incorretas podem dissolver-se ou reparar-se antes de ficarem travadas. Microscopia crioeletrônica de alta resolução mostrou que ambos os conjuntos de fibrilos pareciam essencialmente idênticos em forma geral e torção, indicando que o processo de recozimento não alterou a morfologia básica. 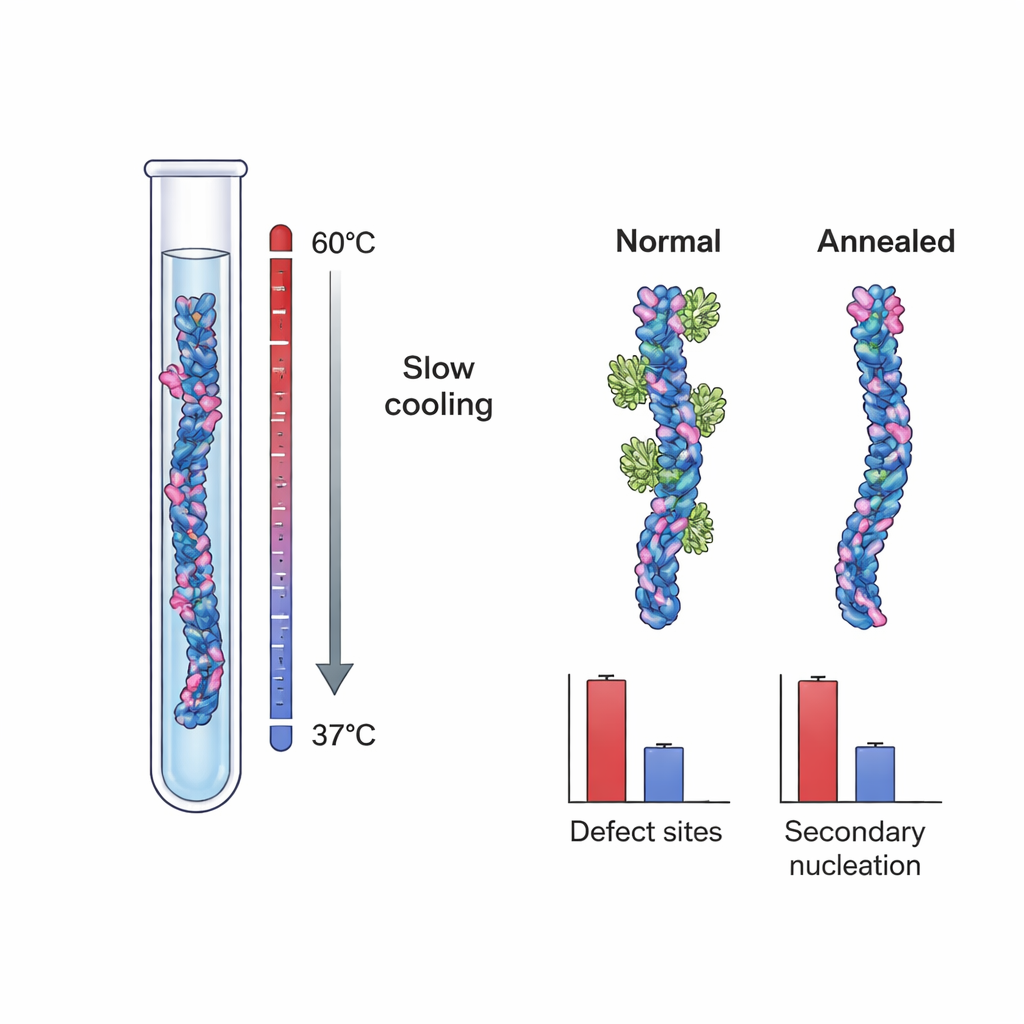
Menos falhas, menos sítios de crescimento perigosos
Quando a equipe mediu a ligação de Brichos a esses dois tipos de fibrilos, descobriram uma diferença marcante. Fibrilos de controle de Aβ40 tinham cerca de um sítio de ligação de Brichos por ~100 monômeros, novamente indicando sítios raros porém importantes. Já os fibrilos recozidos apresentaram apenas cerca de um sítio por ~800 monômeros — uma redução de quase 90% na frequência de sítios. Em testes separados nos quais esses fibrilos foram adicionados como "sementes" a soluções frescas de Aβ40, os fibrilos recozidos foram muito menos eficazes em desencadear nova agregação, mesmo quando sua massa total foi igualada à dos fibrilos de controle. Modelagem cinética detalhada mostrou que essa queda no poder de semeadura não podia ser explicada simplesmente por diferenças no comprimento dos fibrilos. Em vez disso, ela concordou quantitativamente com o número reduzido de sítios de ligação de Brichos, apoiando fortemente a ideia de que defeitos de crescimento atuam como os principais motores da nucleação secundária.
Um princípio geral com promessa terapêutica
Combinando argumentos termodinâmicos, reanálises de trabalhos anteriores e comparações entre várias proteínas formadoras de amilóide, os autores sustentam que defeitos de crescimento raros provavelmente são centrais para a nucleação secundária em muitos sistemas, não apenas na Aβ relacionada ao Alzheimer. Esses defeitos expõem parcialmente o núcleo interno compactamente empacotado do fibrilo, oferecendo um andaime pronto onde novos oligômeros e fibrilos podem se formar muito mais facilmente do que em uma superfície lisa. Reconhecer esses defeitos como os culpados principais abre novas vias para o projeto de fármacos. Em vez de tentar bloquear todas as possíveis interações na superfície de um fibrilo, terapias poderiam visar proteger ou reparar apenas esses escassos sítios defeituosos, ou reduzir as condições que os criam em primeiro lugar. Em termos práticos, isso poderia significar diminuir a concentração efetiva de proteínas formadoras de amilóide no cérebro ou projetar moléculas, inspiradas na Brichos, que reconheçam e neutralizem os pontos quentes de nucleação dirigidos por defeitos. Se bem-sucedidas, tais estratégias poderiam cortar a principal fonte de oligômeros tóxicos e retardar a progressão de doenças associadas ao amilóide.
Citação: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
Palavras-chave: fibrilos amilóides, doença de Alzheimer, nucleação secundária, agregação proteica, chaperona Brichos