Clear Sky Science · pt
Esgotamento de oxigênio em condensados biomoleculares é dominado pela densidade macromolecular
Bolsões Invisíveis Dentro das Células Vivas
Dentro de nossas células, muitas reações químicas dependem de um suprimento contínuo de oxigênio. Mas as células não são sacos simples de líquido: elas contêm compartimentos minúsculos em forma de gotícula, chamados condensados biomoleculares, que se formam sem membranas. Este estudo faz uma pergunta aparentemente simples, com grandes implicações: essas gotículas alteram a disponibilidade de oxigênio em diferentes partes da célula e, em caso afirmativo, por quê? A resposta desafia as ideias predominantes sobre como pequenas moléculas se comportam nesses microambientes congestionados.

Gotas Sem Paredes
Condensados biomoleculares são aglomerados macios, com comportamento semelhante a líquidos, formados por proteínas e ácidos nucleicos que se montam e se dissolvem conforme necessário. Eles ajudam a organizar a bioquímica concentrando algumas moléculas e excluindo outras, mesmo sem uma membrana envolvente. Trabalhos anteriores mostraram que muitos pequenas moléculas metabólicas e compostos semelhantes a fármacos são atraídos para essas gotículas, normalmente porque o interior se comporta um pouco como um solvente oleoso em comparação com o fluido aquoso da célula. O oxigênio, entretanto, é um caso especial: é uma molécula gasosa pequena que alimenta a respiração, mas também provoca reações colaterais danosas. Se os condensados enriquecem ou depletam oxigênio pode, portanto, influenciar quão eficientemente as enzimas funcionam e quanto dano oxidativo ocorre próximo ou dentro dessas gotículas.
Medindo Oxigênio em Compartimentos Minúsculos
Para sondar os níveis de oxigênio dentro dos condensados, os pesquisadores construíram um sistema modelo simples, porém ajustável, usando proteínas artificiais e flexíveis que formam gotículas facilmente em solução salina. Primeiro, eles criaram fases grandes e macroscópicas girando as amostras em uma centrífuga e então inseriram microeletrodos eletroquímicos finíssimos para ler diretamente as concentrações de oxigênio através da fronteira entre as camadas ricas e pobres em proteína. Essas medições revelaram que os níveis de oxigênio caem quando a sonda entra na fase densa em proteínas: as gotas parcialmente excluem o oxigênio em vez de absorvê-lo.
Iluminando o Oxigênio com Corantes Especiais
Como os eletrodos perturbam pequenas gotículas, a equipe recorreu à microscopia de imagem por tempo de vida de fosforescência, um método óptico que usa corantes especiais cuja emissão dura menos tempo quando há mais oxigênio presente. Ao acompanhar o tempo de vida da emissão dentro e fora de gotículas individuais, e corrigindo cuidadosamente como o ambiente da gotícula altera o comportamento de referência do corante, eles puderam inferir as concentrações de oxigênio sem perturbar fisicamente os condensados. Em uma gama de condições, os dados ópticos concordaram com as medições por eletrodos: o oxigênio é consistentemente mais baixo dentro dos condensados do que na solução circundante. Simulações computacionais usando um modelo molecular grosso também sustentaram essa imagem, mostrando que o oxigênio passa relativamente pouco tempo dentro das regiões densas de proteína.
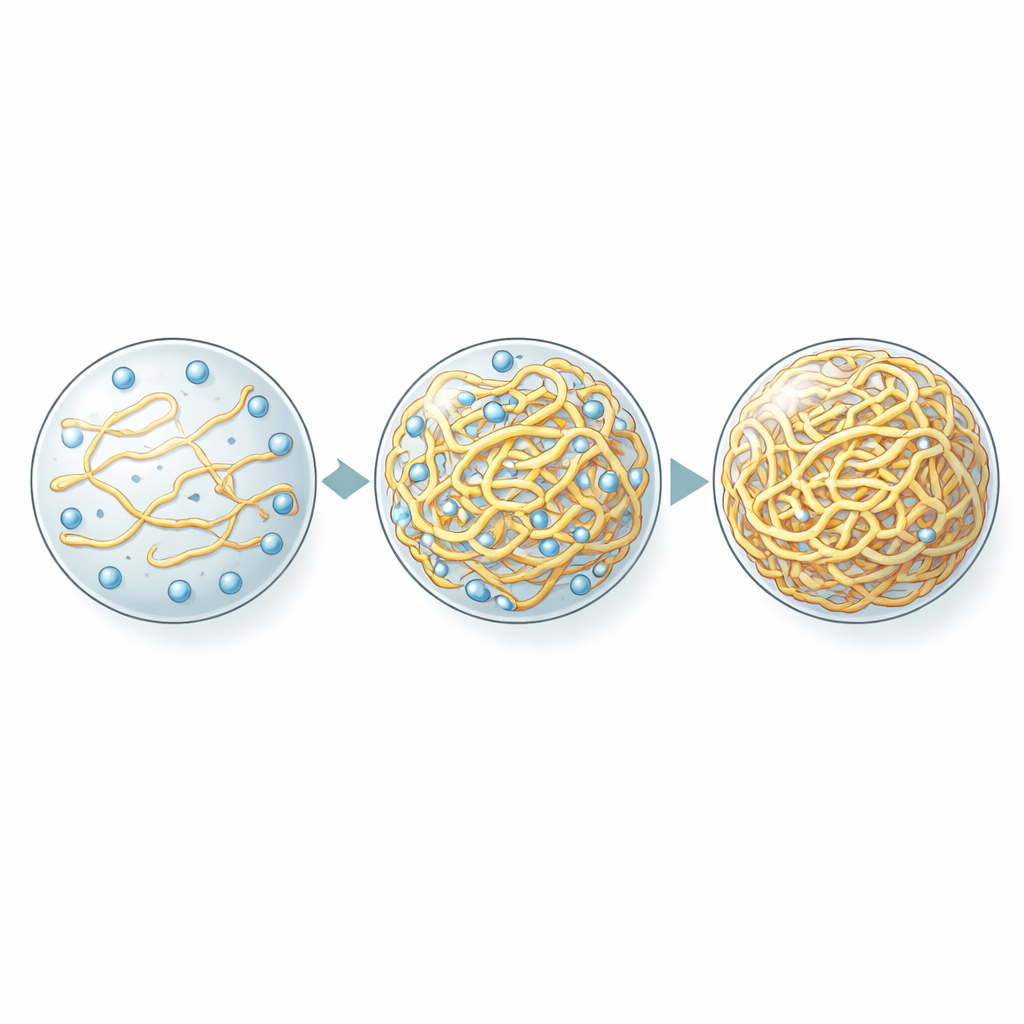
Densidade, Não Oleosidade, Define os Níveis de Oxigênio
O suspeito óbvio para controlar a captação de oxigênio é a hidrofobicidade — a “oleosidade” do interior da gotícula — que havia sido identificada anteriormente como o fator chave para como muitas outras pequenas moléculas se particionam nos condensados. Para testar isso, os autores alteraram sistematicamente as sequências proteicas para mudar tanto o número de unidades repetidas quanto seu caráter hidrofóbico, e então mediram o oxigênio dentro das gotículas resultantes. Surpreendentemente, os níveis de oxigênio não acompanharam o quão oleosas ou aquosas as gotículas eram. Em vez disso, eles se correlacionaram forte e inversamente com a quantidade de proteína empacotada na fase densa. Variantes que formaram condensados mais congestionados retiveram menos oxigênio, mesmo quando eram menos hidrofóbicas no geral. Outros corantes pequenos e oleosos comportaram-se de forma diferente: ainda preferiam gotículas mais hidrofóbicas, confirmando que o oxigênio quebrava as regras habituais.
Nova Visão de Gradientes de Oxigênio em Nanoscale
Esses achados conduzem a uma visão revisada de como os condensados moldam seu entorno químico. Para pequenas moléculas que não se ligam fortemente às proteínas estruturais, a pura densidade de macromoléculas torna-se o fator dominante: quanto mais volume as proteínas ocupam, menos espaço resta para o oxigênio dissolvido. Isso significa que as células podem gerar gradientes de oxigênio em distâncias de nanômetros a micrômetros simplesmente formando ou dissolvendo condensados, ou mudando o quão compactas essas gotículas estão. Em termos práticos, o trabalho sugere que organelas sem membrana podem sutilmente ajustar a disponibilidade de oxigênio para reações próximas — potencialmente acelerando algumas, desacelerando outras ou protegendo componentes sensíveis — por meio de um efeito físico de fechamento, em vez de por ligações químicas específicas.
Citação: Garg, A., Brasnett, C., Marrink, S.J. et al. Oxygen depletion in biomolecular condensates is dominated by macromolecular density. Nat Commun 17, 2603 (2026). https://doi.org/10.1038/s41467-026-69376-2
Palavras-chave: condensados biomoleculares, particionamento de oxigênio, aglomeramento macromolecular, separação de fases, microambientes celulares