Clear Sky Science · pt
Mecanismo de "roaming" ultrarrápido modulado pelo solvente em bromofórmio revelado por espalhamento de raios X em solução com femtossegundos
Por que moléculas minúsculas na água e no ar importam
O bromofórmio é uma molécula pequena, produzida naturalmente, que tem grande impacto ambiental. Quando a luz solar atinge essa molécula na atmosfera ou no spray oceânico, ela pode liberar átomos de bromo que ajudam a destruir o ozônio, o escudo que nos protege dos raios ultravioleta nocivos do Sol. Este estudo faz uma pergunta aparentemente simples, mas de consequências amplas: o ambiente líquido ao redor do bromofórmio altera o que acontece nos primeiros trilionésimos de segundo após a incidência da luz e, portanto, muda quanto bromo destruidor de ozônio aparece ao final?
Luz que parte uma molécula
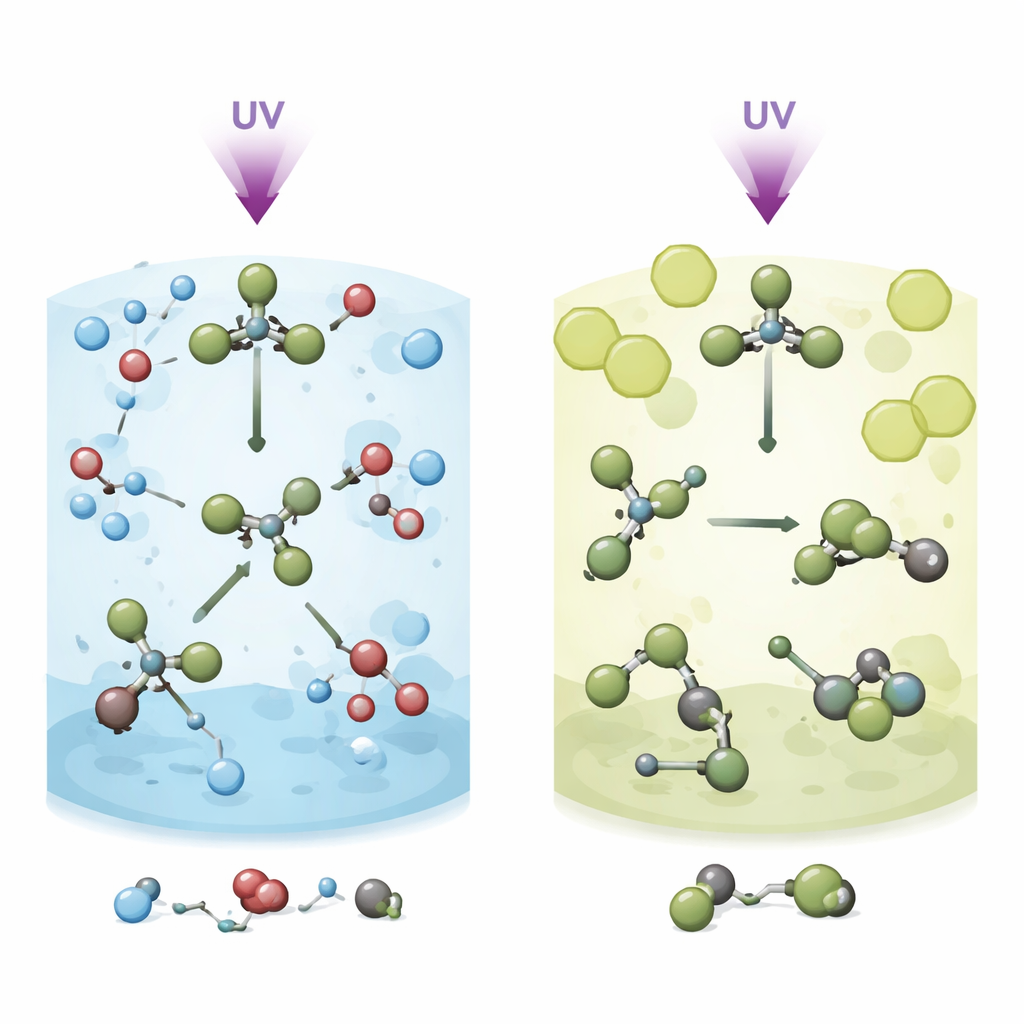
Os pesquisadores começam iluminando o bromofórmio dissolvido em dois líquidos diferentes com rajadas extremamente curtas de luz ultravioleta: metanol, que é polar e quimicamente reativo, e metilciclohexano, que é não polar e relativamente inerte. A luz enfraquece rapidamente uma das ligações carbono–bromo do bromofórmio, fazendo a molécula começar a se desfazer. Mas, em vez de simplesmente se separar, um átomo de bromo permanece por perto e "vagueia" ao redor do fragmento restante, CHBr₂. Esse movimento de roaming cria uma forma efêmera e reconfigurada chamada isômero. O enigma central é o que acontece com esse intermediário em roaming em diferentes líquidos e como essa escolha controla se o bromofórmio libera átomos de bromo livres ou é desviado para outros produtos.
Fazendo filmes moleculares com raios X
Para assistir a esses eventos, a equipe usa espalhamento de raios X em solução com resolução temporal de femtossegundos no European X-ray Free-electron Laser. Essencialmente, eles gravam um filme tipo estroboscópio de como as distâncias interatômicas mudam em tempo real, com resolução de pico- e sub-picosegundos. Ao comparar os padrões de espalhamento medidos com padrões gerados por computador para muitas estruturas possíveis, eles reconstróem como os comprimentos de ligação e ângulos dentro do bromofórmio evoluem após a excitação. Técnicas avançadas de análise e simulações aceleradas por aprendizado de máquina ajudam a separar vias reacionais sobrepostas e a atribuir vidas médias precisas a espécies de curta duração.
Dois líquidos, dois destinos bem diferentes
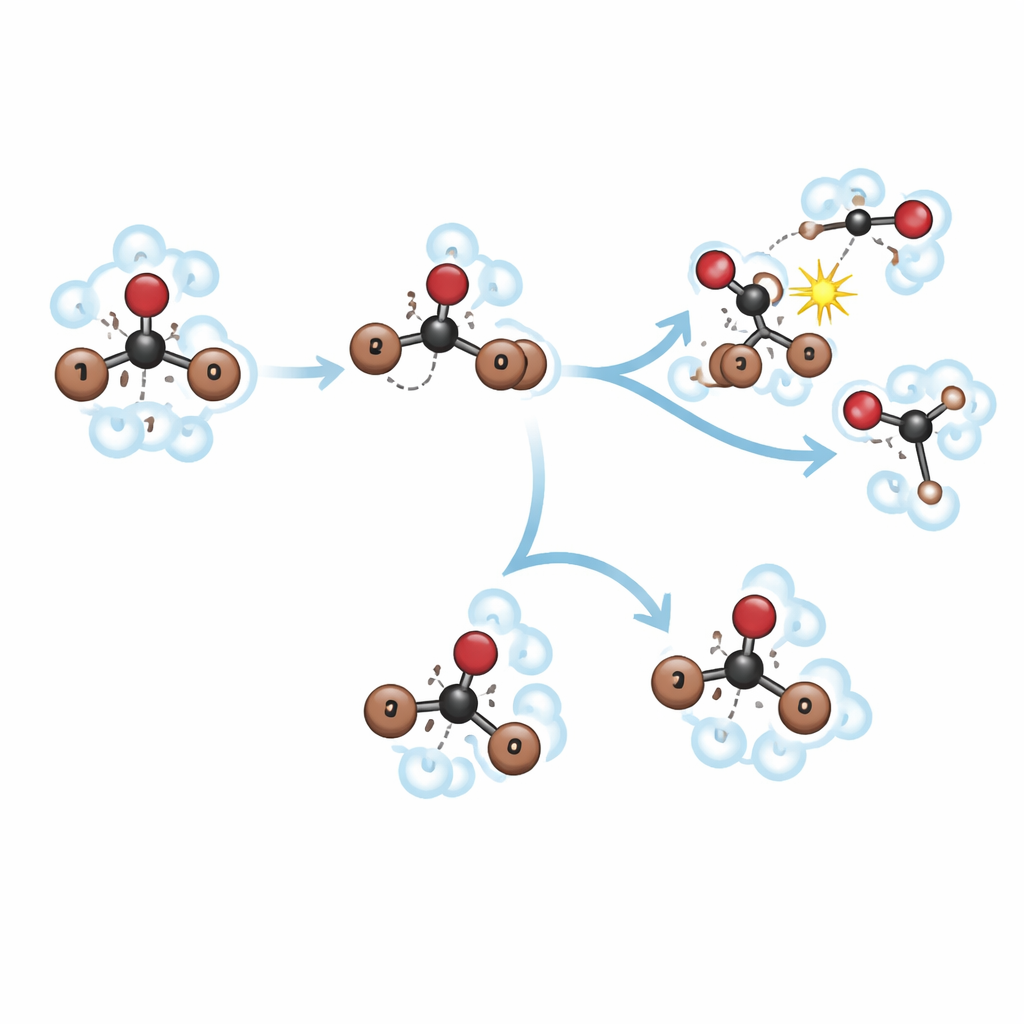
No metanol, o intermediário em roaming está presente, mas é de curta duração. Em cerca de 150 femtossegundos, a ligação carbono–bromo inicial se rompe, formando CHBr₂ e um bromo em roaming. Nos ~400 femtossegundos seguintes, esse isômero quente e vibrante se estica e se dobra repetidamente, o que aproxima os fragmentos das moléculas vizinhas de metanol com frequência. Em vez de relaxar para uma forma rearranjada estável, a estrutura em roaming é rapidamente interceptada pelo metanol em uma reação de "metanólise". Isso produz novas moléculas, CH₃OCHBr₂ e HBr, enquanto fragmentos livres CHBr₂ e Br de uma via de ruptura paralela e mais direta continuam a reagir mais lentamente ao longo de vários picosegundos. A "gaiola" molecular apertada do solvente e seus grupos hidroxila reativos atuam em conjunto para guiar o bromofórmio por essa rota de reação química, em vez de direcioná‑lo para um isômero de longa duração.
Quando o líquido dá espaço e deixa o roaming prosseguir
No metilciclohexano, a história muda dramaticamente. O mesmo impulso ultravioleta novamente gera movimento de roaming em cerca de 150 femtossegundos, mas o líquido não polar envolve o bromofórmio de forma mais frouxa e não reage prontamente com ele. Aqui, o bromo em roaming e o fragmento CHBr₂ têm espaço para reorientar-se e se acomodar em uma estrutura isomérica estável, em vez de se envolverem imediatamente com moléculas do solvente. A ruptura direta em fragmentos separados CHBr₂ e Br ainda ocorre e compete com a formação do isômero, mas agora o isômero rearranjado sobrevive por tempos muito maiores. Simulações mostram que a gaiola de solvente maior e mais macia no metilciclohexano incentiva esse comportamento de roaming similar ao do gás, enquanto a gaiola confinada e fortemente interagente no metanol canaliza o mesmo intermediário diretamente para reação química.
O que isso significa para o ozônio e além
Em conjunto, esses experimentos e cálculos mostram que o roaming é um passo inicial universal quando o bromofórmio absorve luz ultravioleta em ambientes líquidos, mas o solvente ao redor decide o que acontece a seguir. Em ambientes do tipo metanol, o roaming serve principalmente para impulsionar reações muito rápidas com o líquido, limitando a formação de isômeros de longa duração e moldando como e quando aparecem produtos portadores de bromo. Em ambientes do tipo metilciclohexano, o roaming alimenta em vez disso uma forma rearranjada de longa duração que pode liberar bromo em escalas de tempo diferentes. Ao filmar diretamente esses movimentos ultrarrápidos, o trabalho mostra que o caráter microscópico de gotas, aerossóis e outros ambientes em fase condensada pode controlar fortemente as vias químicas de moléculas relevantes para o ozônio, ajudando cientistas a construir modelos mais precisos da fotoquímica atmosférica e em solução.
Citação: Su, P., Zhang, J., Wang, H. et al. Ultrafast solvent-modulated roaming mechanism in bromoform revealed by femtosecond X-ray solution scattering. Nat Commun 17, 2514 (2026). https://doi.org/10.1038/s41467-026-69374-4
Palavras-chave: bromofórmio, mecanismo de roaming, fotquímica ultrarrápida, efeitos do solvente, depleção do ozônio