Clear Sky Science · pt
Ordem concorrente de ligações de hidrogênio impulsiona a tensão superficial anômala da água
Por que a superfície da água é mais estranha do que parece
A superfície da água permite que insetos caminhem sobre lagoas, molda gotas de chuva e controla como bolhas se formam e estouram. No entanto, quando cientistas medem o quão “tensa” é essa superfície — a tensão superficial — descobrem que a água se comporta de maneira surpreendentemente estranha à medida que esfria, especialmente quando é resfriada abaixo do seu ponto de congelamento normal. Este artigo usa simulações avançadas por computador para revelar como a organização oculta das moléculas de água na superfície explica esse mistério de longa data.
Dois tipos ocultos de água líquida
Embora experimentemos a água como um líquido simples e uniforme, suas moléculas podem se organizar localmente de duas maneiras contrastantes. Uma disposição é mais compacta e desordenada; os autores chamam isso de estado ρ. A outra é mais aberta e simétrica, com cada molécula cercada em um padrão aproximadamente tetraédrico de quatro vizinhos; isso é chamado de estado S. Trabalhos anteriores sugeriram que o equilíbrio entre esses dois padrões locais ajuda a explicar muitas das propriedades anômalas da água no volume. Aqui, os autores investigam como essa mesma imagem de dois estados se manifesta na interface ar–água, onde nasce a tensão superficial.
Como a superfície alinha as moléculas
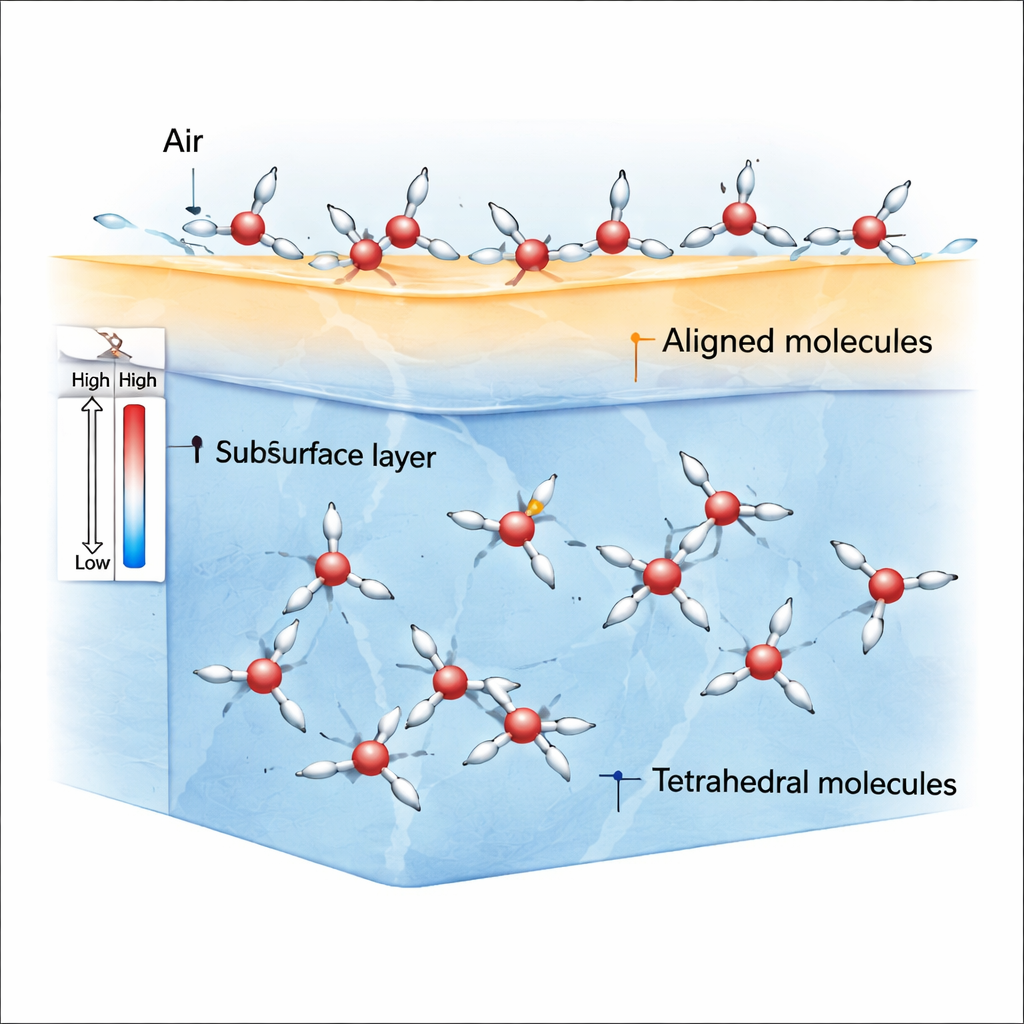
No limite entre o ar e a água, as moléculas deixam de sentir puxões iguais em todas as direções. Essa simetria quebrada favorece moléculas do estado ρ cujos átomos de hidrogênio e dipolos moleculares podem facilmente inclinar-se numa direção preferencial. Simulações mostram que próximo à temperatura ambiente e um pouco abaixo, a camada mais externa da água fica repleta dessas moléculas ρ alinhadas, enquanto moléculas do estado S são mais comuns um pouco abaixo da superfície e no volume. Como as moléculas do estado ρ se alinham fortemente, elas criam um desequilíbrio de forças — anisotropia de tensões — que gera uma tensão superficial relativamente alta em comparação com líquidos comuns como o benzeno.
Por que o resfriamento primeiro desacelera e depois acelera o apertamento da superfície
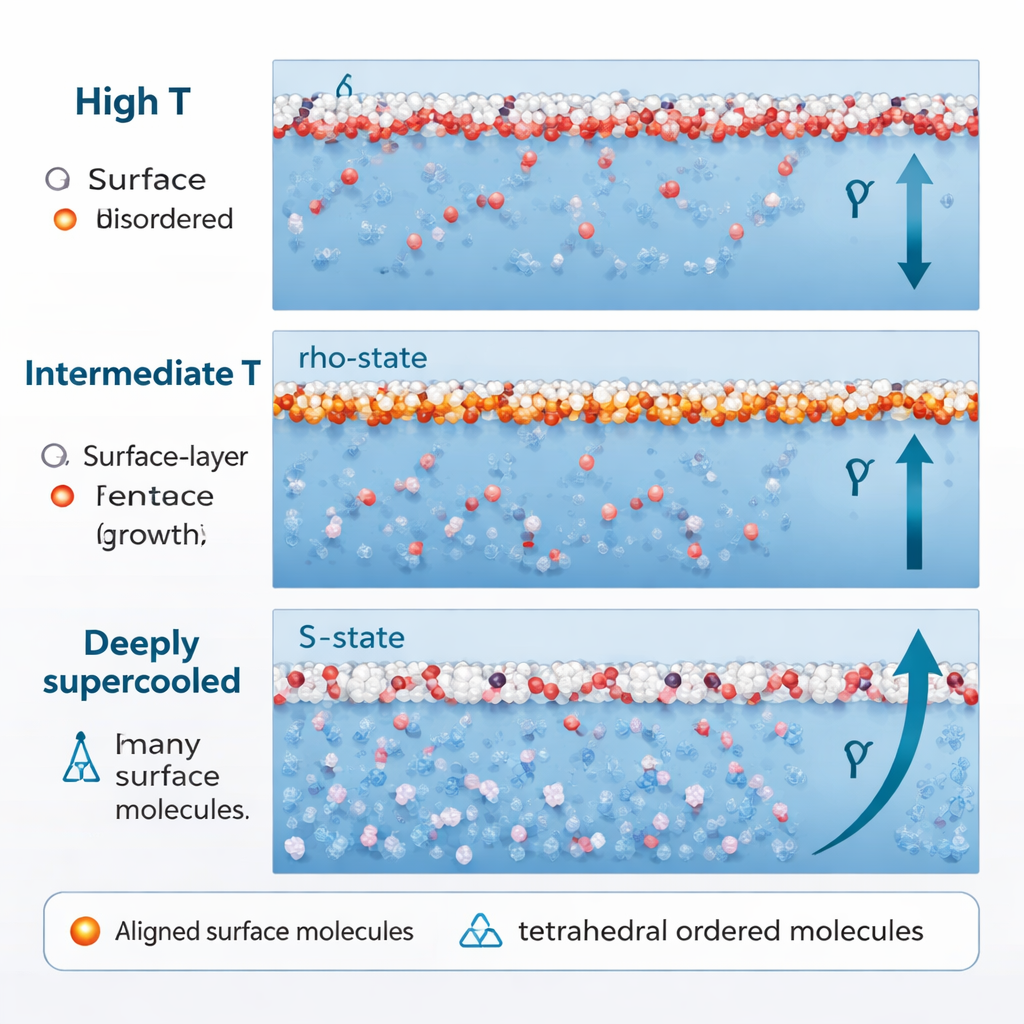
Na maioria dos líquidos simples, o resfriamento aperta a superfície de forma contínua, fazendo a tensão superficial aumentar quase linearmente. A água faz isso apenas em temperaturas mais altas. Ao esfriar em direção a cerca de –0,15 °C (275 K), o aumento da tensão superficial começa a desacelerar. As simulações mostram que essa desaceleração ocorre porque as moléculas do estado ρ na superfície já se alinharam tanto quanto possível; um resfriamento adicional mal altera sua contribuição. Ao mesmo tempo, as moléculas do estado S na subsuperfície permanecem majoritariamente orientadas ao acaso, portanto contribuem pouco para aumentar a tensão de superfície. O resultado líquido é uma espécie de platô: a temperatura continua caindo, mas a tensão superficial cresce apenas lentamente.
Superresfriamento profundo desencadeia um segundo apertamento
Quando a água é resfriada muito mais, bem abaixo do seu ponto de congelamento normal, para o regime profundamente superresfriado (em torno de 250 K e abaixo), seu comportamento muda novamente. A fração de estruturas tetraédricas do estado S aumenta bruscamente, mesmo perto da superfície. Crucialmente, essas moléculas do estado S deixam de apontar em direções aleatórias. Seus dipolos começam a se alinhar ao longo da direção perpendicular à superfície, impulsionados por interações entre dipolos moleculares vizinhos e por uma região de pressão negativa logo abaixo da superfície. Uma vez que isso acontece, a água no estado S, que antes amolecia a tensão superficial, passa a reforçá-la. Essa contribuição ordenada adicional produz um novo aumento mais rápido — o aumento “reentrante” — da tensão superficial em baixas temperaturas.
De enigmas de superfície ao gelo e além
Os mesmos aglomerados tetraédricos do estado S que enrijecem a superfície em baixas temperaturas também se assemelham a blocos de construção iniciais de certas formas de gelo, e as simulações os encontram enriquecidos perto da interface. Isso significa que a fronteira ar–água pode atuar como um berço para a formação do gelo, ajudando a explicar por que o congelamento frequentemente começa nas superfícies. Mais amplamente, o trabalho fornece um elo concreto, em nível molecular, entre como as moléculas de água se organizam e se orientam e a força com que a superfície puxa para dentro. Essa imagem estrutural-mecânica não apenas resolve a curva de temperatura estranha da tensão superficial da água, mas também oferece um roteiro para entender e controlar fenômenos interfaciais em outros líquidos formadores de rede, desde água superresfriada em nuvens até materiais usados em tecnologia e biologia.
Citação: Yuan, J., Qiu, K., Sun, G. et al. Competing hydrogen-bond orders drive water’s anomalous surface tension. Nat Commun 17, 1498 (2026). https://doi.org/10.1038/s41467-026-69356-6
Palavras-chave: tensão superficial da água, ligação de hidrogênio, água superresfriada, estrutura líquida, nucleação do gelo