Clear Sky Science · pt
STING sinergiza com TOX suprimindo a expressão de HO-1 para desencadear ferroptose em células T CD8+ infiltrantes de tumor e resistência à imunoterapia
Por que esta pesquisa importa para o tratamento do câncer
As imunoterapias modernas contra o câncer funcionam ao liberar as próprias células T assassinas do corpo, ainda que muitos tumores encontrem maneiras de desativá‑las. Este estudo descobre um interruptor de autodestruição oculto dentro das células T CD8+ que os tumores exploram, e mostra como desligar esse interruptor pode tornar a imunoterapia muito mais eficaz.
Uma via de morte oculta dentro das células T que lutam contra o tumor
Dentro de um tumor, as células T CD8+ deveriam caçar e destruir células cancerosas. Em vez disso, muitas vezes se tornam escassas, lentas e de vida curta. Os autores focaram em duas moléculas dentro das células T—STING, um sensor de dano ao DNA, e TOX, uma proteína associada ao desgaste das células T. Eles engenheiraram camundongos cujas células T CD8+ não tinham STING, TOX ou ambos, e então implantaram vários tipos de tumor. Surpreendentemente, camundongos cujas células T não possuíam STING ou TOX controlaram melhor os tumores. Seus tumores cresceram mais devagar, continham muito mais células T CD8+ e essas células produziram maiores quantidades de moléculas que matam o câncer, como interferon‑gama e granzima B. Isso apontou para um programa interno que sabota silenciosamente as células T dentro dos tumores.
Como a morte celular dirigida pelo ferro enfraquece a imunidade
Ao examinar a atividade gênica em células T infiltrantes de tumor, os pesquisadores encontraram que células T normais dentro dos tumores estavam preparadas para uma forma particular de morte celular chamada ferroptose. Ao contrário da apoptose, a ferroptose é desencadeada pelo excesso de ferro e pelo acúmulo de lipídios danificados nas membranas celulares. Em células T CD8+ comuns expostas a células tumorais, genes que promovem acúmulo de ferro e dano lipídico foram ativados, enquanto genes protetores foram reprimidos. Em contraste, células T deficientes em STING ou TOX exibiram o padrão oposto: expressaram mais das enzimas protetoras HO‑1 e GPX4, apresentaram níveis menores de ferro, menos peroxidação lipídica, mitocôndrias mais saudáveis e resistiram à morte por ferroptose. Testes em laboratório confirmaram que bloquear quimicamente a ferroptose mantinha as células T normais vivas, enquanto a remoção de STING ou TOX as tornava naturalmente resistentes.
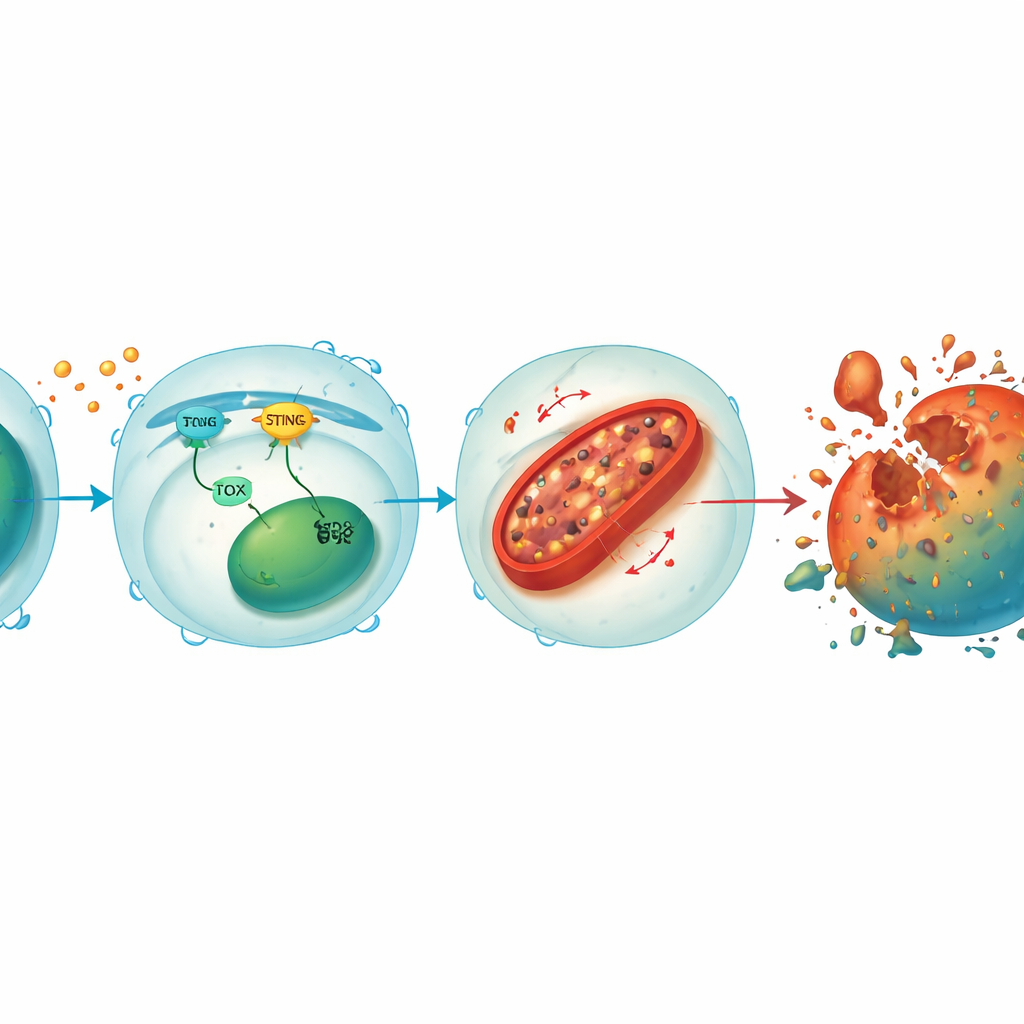
Um circuito que liga sinais de estresse ao dano mitocondrial
Ao aprofundar, a equipe descobriu que STING e TOX formam um circuito de reforço dentro das células T CD8+. Quando sinais tumorais ou virais ativam STING, isso aciona fatores a jusante que aumentam TOX, e TOX por sua vez ajuda a manter a atividade de STING. Juntos, eles suprimem HO‑1, uma enzima que normalmente ajuda a controlar o ferro celular. Com HO‑1 reprimida, o ferro se acumula nas mitocôndrias—as usinas de energia da célula—levando a altos níveis de moléculas reativas de oxigênio e oxidação dos lipídios de membrana. Esse dano mitocondrial esgota a produção de energia e, em última instância, empurra a célula T para a ferroptose. Restaurar STING ou TOX em células T knockout trouxe de volta o excesso de ferro e a morte celular, enquanto reduzir ainda mais HO‑1 tornou até mesmo as células protegidas vulneráveis novamente, ressaltando HO‑1 como um freio central nessa via destrutiva.
Como o lactato produzido pelo tumor puxa o gatilho
O microambiente tumoral é rico em lactato, um subproduto do metabolismo alterado do câncer. O estudo mostra que esse lactato não é apenas resíduo metabólico—ele ajuda ativamente a acionar o interruptor da ferroptose nas células T. Comparadas com outras células, as T CD8+ foram especialmente sensíveis ao lactato. À medida que o lactato entrava nas células por transportadores específicos, causava acúmulo de ferro, encolhimento mitocondrial, perda de DNA mitocondrial e mais dano oxidativo. Ao mesmo tempo, o lactato aumentava a atividade de STING e TOX e reprimia ainda mais HO‑1. Células T sem STING ou TOX foram muito mais resistentes ao dano induzido por lactato. Bloquear um transportador chave de lactato com um fármaco (AZD3965) protegeu as células T CD8+ da ferroptose em camundongos, aumentou sua presença dentro dos tumores e retardou o crescimento tumoral, imitando o benefício da deleção genética de STING nas células T.
Transformando uma vulnerabilidade em vantagem terapêutica
Esses insights mecanísticos têm implicações práticas. Quando os pesquisadores usaram terapia celular adotiva—infundindo camundongos com células T ativadas em laboratório—constataram que células T projetadas para não expressar STING ou TOX controlaram muito melhor os tumores do que células T normais. Além disso, combinar essas células T “resistentes à ferroptose” com tratamentos existentes, como bloqueadores de checkpoint PD‑1 ou TIM‑3, quimioterapia com cisplatina ou um fármaco ativador de STING, produziu redução tumoral marcadamente maior do que qualquer terapia isolada. Finalmente, em amostras tumorais de pacientes com câncer cervical, níveis mais altos de TOX e mais baixos de HO‑1 em linfócitos infiltrantes de tumor se associaram a pior sobrevida, sugerindo que essa via também molda desfechos clínicos em humanos.
O que isso significa para o futuro do cuidado do câncer
Em termos claros, o estudo revela que os tumores podem forçar nossas melhores células T anticâncer a enferrujarem de dentro para fora ao induzir uma forma de morte celular alimentada por ferro. Um circuito lactato–STING–TOX reduz a proteção oferecida por HO‑1, danifica as mitocôndrias e leva à ferroptose, reduzindo o número de células T CD8+ eficazes. Interromper esse circuito—engenheirando células T sem STING ou TOX, aumentando HO‑1 ou bloqueando a entrada de lactato—mantém as células T vivas, energizadas e prontas para atacar. Este trabalho aponta para imunoterapias de próxima geração que combinam ajuste metabólico e genético das células T com drogas existentes para superar a resistência e oferecer controle do câncer mais duradouro.
Citação: Zhu, Q., Zhang, Jb., Nie, Cp. et al. STING synergizes with TOX suppressing HO-1 expression to trigger ferroptosis in tumor-infiltrating CD8+ T cell and immunotherapy resistance. Nat Commun 17, 2543 (2026). https://doi.org/10.1038/s41467-026-69350-y
Palavras-chave: imunoterapia contra o câncer, células T CD8, ferroptose, microambiente tumoral, via STING TOX HO-1