Clear Sky Science · pt
Seq-Scope-eXpanded: ômicas espaciais além da resolução óptica
Vendo as Células com Mais Nitidez
Nossos corpos são formados por incontáveis células minúsculas, cada uma cheia de atividade que normalmente não conseguimos ver, mesmo com microscópios potentes. Este artigo apresenta o Seq-Scope-X, uma tecnologia que permite aos pesquisadores ampliar o nível de detalhe das estruturas teciduais, mapeando quais genes e proteínas estão ativos em pontos precisos dentro e entre as células. Esse nível de detalhe pode transformar o estudo do desenvolvimento, do sistema imune e de doenças como câncer ou lesão hepática.
Por que Mapear Moléculas no Local?
As células não funcionam isoladamente: vivem em vizinhanças, formam camadas e se especializam conforme sua posição. Métodos tradicionais de sequenciamento destroem o tecido, perdendo esse contexto espacial. Ferramentas mais recentes de “ômicas espaciais” mantêm as moléculas em posição, mas há um compromisso. Métodos baseados em imagem conseguem ver detalhes muito finos, mas geralmente rastreiam apenas um conjunto limitado de genes. Métodos baseados em sequenciamento podem ler quase todos os genes de uma vez, porém borram características finas, frequentemente espalhando sinais por vários micrômetros — maior que muitas estruturas subcelulares. Os autores buscaram fechar essa lacuna: preservar a leitura ampla e imparcial do sequenciamento, alcançando ou mesmo superando a nitidez dos microscópios modernos.
Esticando o Tecido para Vencer Limites Ópticos
A ideia central do Seq-Scope-X é aparentemente simples: aumentar suavemente o próprio tecido para que cada nanômetro original de estrutura fique mais fácil de resolver. A equipe primeiro ancora moléculas de RNA — ou etiquetas de DNA especiais ligadas a anticorpos — em um hidrogel macio construído ao redor do corte de tecido. Em seguida, digerem o tecido original e fazem o gel inchar em uma solução salina, esticando fisicamente tudo cerca de três vezes enquanto mantêm as posições relativas quase intactas. Esse gel expandido é então colocado sobre um chip de sequenciamento ultra-denso revestido com sondas de captura. Ao aquecer cuidadosamente o conjunto, as moléculas ancoradas são liberadas do gel e reassociadas ao chip, que pode ser sequenciado para revelar quais genes ou proteínas estavam presentes em cada pequena coordenada. 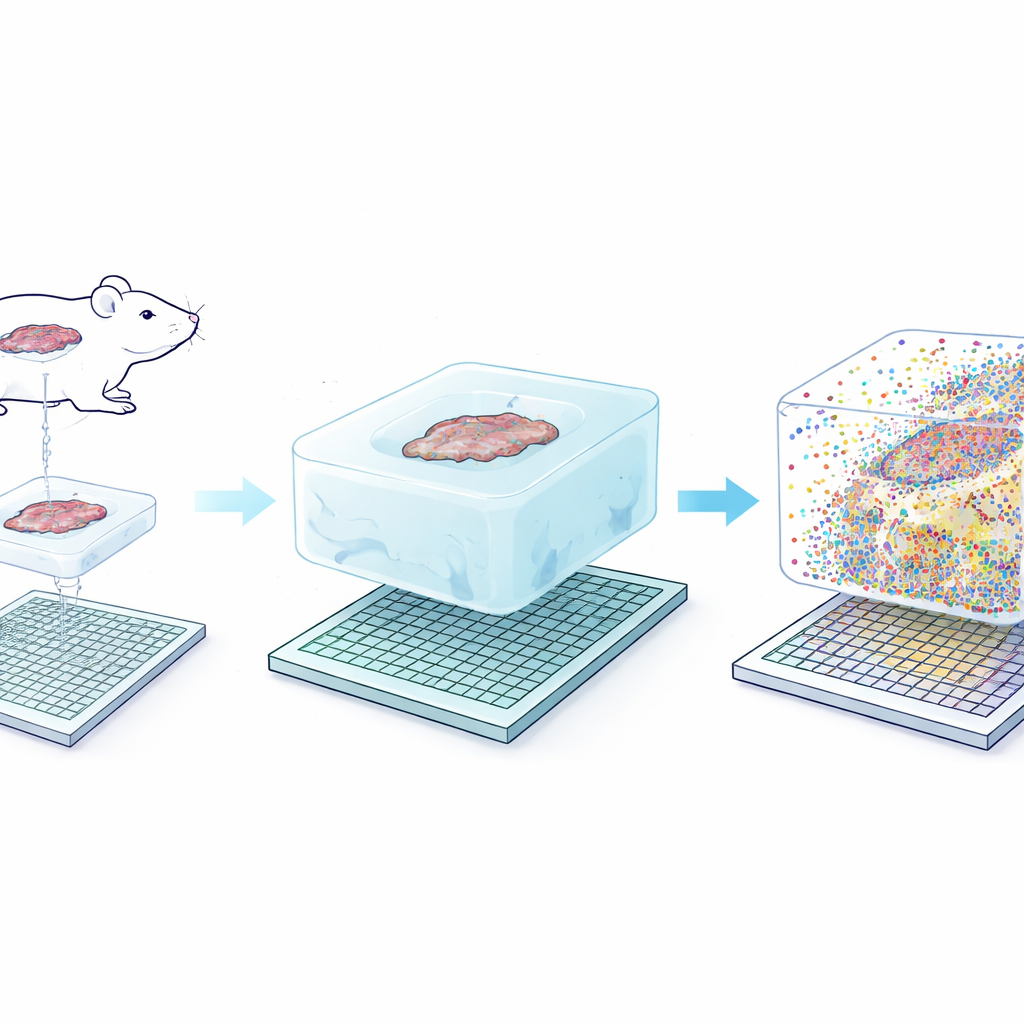
De Células Borradas a Mapas Subcelulares
Ao aplicar Seq-Scope-X em fígado de camundongo, os pesquisadores descobriram que o método melhorou a resolução espacial de aproximadamente 0,6 micrômetros para cerca de 0,2 micrômetros e aumentou o número de posições mensuráveis por milímetro quadrado em quase dez vezes. Em termos práticos, aquilo que antes parecia manchas borradas de sinal passou a revelar contornos nítidos de células individuais. Ainda mais notável, aglomerados de RNA que não haviam sido totalmente processados (não spliced) alinhavam-se fortemente com os centros dos núcleos, enquanto o RNA maduro (spliced) delineava o citoplasma ao redor. Isso permitiu aos autores traçar limites celulares usando apenas RNA e separar leituras gênicas nucleares e citoplasmáticas para quase todos os hepatócitos no tecido — algo que métodos anteriores baseados em sequenciamento só podiam sugerir.
Células com Personalidades Divididas
Com essa nova nitidez, a equipe descobriu uma forma inesperada de “vida dupla” molecular dentro das células hepáticas. Ao longo do conhecido gradiente dos vasos sanguíneos pelo lado portal até o lado central do lóbulos hepáticos, os hepatócitos se especializam em diferentes tarefas metabólicas. Seq-Scope-X mostrou que, em muitas células, o padrão gênico no núcleo não correspondia ao padrão no citoplasma circundante. Cerca de um terço dos hepatócitos aparentava ter um perfil nuclear alinhado com uma zona e um perfil citoplasmático alinhado com a zona vizinha. Métodos independentes baseados em imagem, incluindo MERFISH e ensaios de RNA fluorescente de molécula única, confirmaram que transcritos individuais podem se concentrar tanto no núcleo quanto no citoplasma. Em conjunto, essas descobertas sugerem que os hepatócitos podem deslocar dinamicamente seus papéis metabólicos ao longo do tempo, com o núcleo se preparando para um estado futuro enquanto o citoplasma reflete o estado atual. 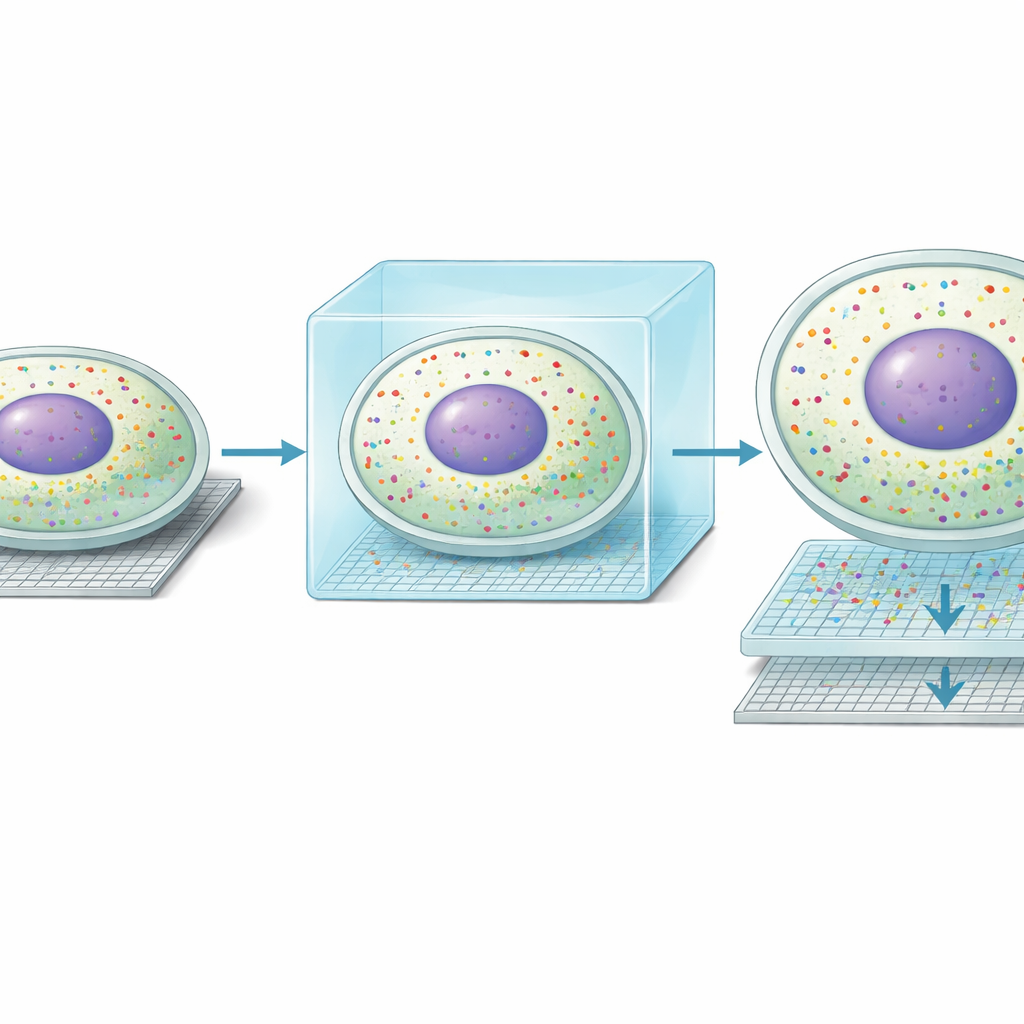
Além do Fígado: Cérebro, Intestino e Tecidos Imunes
Os autores então testaram se o Seq-Scope-X funciona em outros órgãos. No cérebro, separou claramente diferentes tipos de neurônios e células de suporte e revelou padrões subcelulares de RNA ao redor dos núcleos. No cólon, resolveu subtipos distintos de células caliciformes e camadas de colonócitos ao longo do eixo da cripta à superfície, novamente capturando assinaturas nucleares. Talvez mais dramaticamente, a equipe adaptou o método para proteínas usando anticorpos com código de barras de DNA no baço de camundongo e em tonsila humana. Seq-Scope-X pôde mapear simultaneamente mais de cem marcadores de superfície celular em resolução de célula única, distinguindo subconjuntos de células T e B muito próximos e células mieloides. Ao mudar para uma química de gel mais expansível, avançaram a resolução efetiva em direção ao verdadeiro nanossegundo (nanoscale), preservando a arquitetura tecidual o suficiente para mapeamento detalhado.
O Que Isso Significa Para o Futuro
Seq-Scope-X demonstra que ampliar fisicamente tecidos antes do sequenciamento pode superar limites de resolução de longa data, entregando detalhe quase ao nível de um microscópio enquanto ainda lê milhares de genes ou etiquetas de proteína de uma vez. Para um observador leigo, isso significa que os cientistas agora podem construir “atlas moleculares” que não só indicam onde as células estão, mas também revelam o que acontece dentro de diferentes partes de cada célula. Esses mapas podem ajudar a explicar como tecidos respondem a lesões, como células imunes se organizam em órgãos linfoides e tumores, ou como mudanças sutis dentro das células prenunciam doenças. Embora sejam necessários refinamentos adicionais para ampliar a cobertura e melhorar alguns painéis de marcação, Seq-Scope-X abre uma nova e poderosa janela sobre as paisagens microscópicas que sustentam a saúde e a doença.
Citação: Anacleto, A., Cheng, W., Feng, Q. et al. Seq-Scope-eXpanded: spatial omics beyond optical resolution. Nat Commun 17, 2564 (2026). https://doi.org/10.1038/s41467-026-69346-8
Palavras-chave: transcriptômica espacial, expansão de tecido, ômicas de célula única, proteômica espacial, zonação hepática