Clear Sky Science · pt
A IPA derivada da microbiota protege contra a colite ao regular a cetogênese mediada por HMGCS2 intestinal para facilitar a cicatrização da mucosa
Por que as bactérias intestinais importam para um intestino lesionado
Quando o revestimento do intestino é danificado, como na doença inflamatória intestinal (DII) ou após tratamentos médicos agressivos, o corpo precisa reparar rapidamente essa “pele” interna para evitar que conteúdos nocivos vazem para a corrente sanguínea. Este estudo revela como uma única molécula produzida por bactérias intestinais benéficas pode ajudar o intestino a se curar, apontando para novas formas de tratar distúrbios crônicos do intestino sem suprimir amplamente o sistema imunológico.
Um sinal útil de micróbios amigos
Os pesquisadores começaram comparando impressões químicas de amostras de fezes de pessoas com DII e voluntários saudáveis, bem como em vários modelos murinos de colite. Entre centenas de moléculas, uma se destacou: o ácido indol-3-propiónico (IPA), um produto da degradação do aminoácido alimentar triptofano produzido por certas bactérias intestinais. Os níveis de IPA foram consistentemente mais baixos em pessoas com doença de Crohn e em camundongos com colite do que em controles saudáveis. Isso sugeriu que a perda de IPA pode fazer parte do que dá errado quando o revestimento intestinal fica inflamado e não consegue se reparar.
Fortalecendo a parede protetora do intestino
Para testar se o IPA apenas acompanhava a doença ou realmente protegia contra ela, a equipe administrou IPA a camundongos antes de induzir vários tipos de lesão intestinal, incluindo colite química e dano por radiação. Camundongos que receberam doses adequadas de IPA tiveram cólons mais longos e saudáveis, menos alterações inflamatórias ao microscópio e uma camada de muco mais espessa com junções celulares mais apertadas. Eles apresentaram menor vazamento de marcadores inflamatórios e um número maior de células caliciformes, que produzem o muco protetor. Importante, esses benefícios foram observados mesmo em camundongos livres de germes, que não possuem microbioma residente, mostrando que, uma vez presente, o IPA pode agir diretamente sobre o revestimento intestinal sem precisar de outros micróbios.
Abastecendo células-tronco com um tipo especial de energia
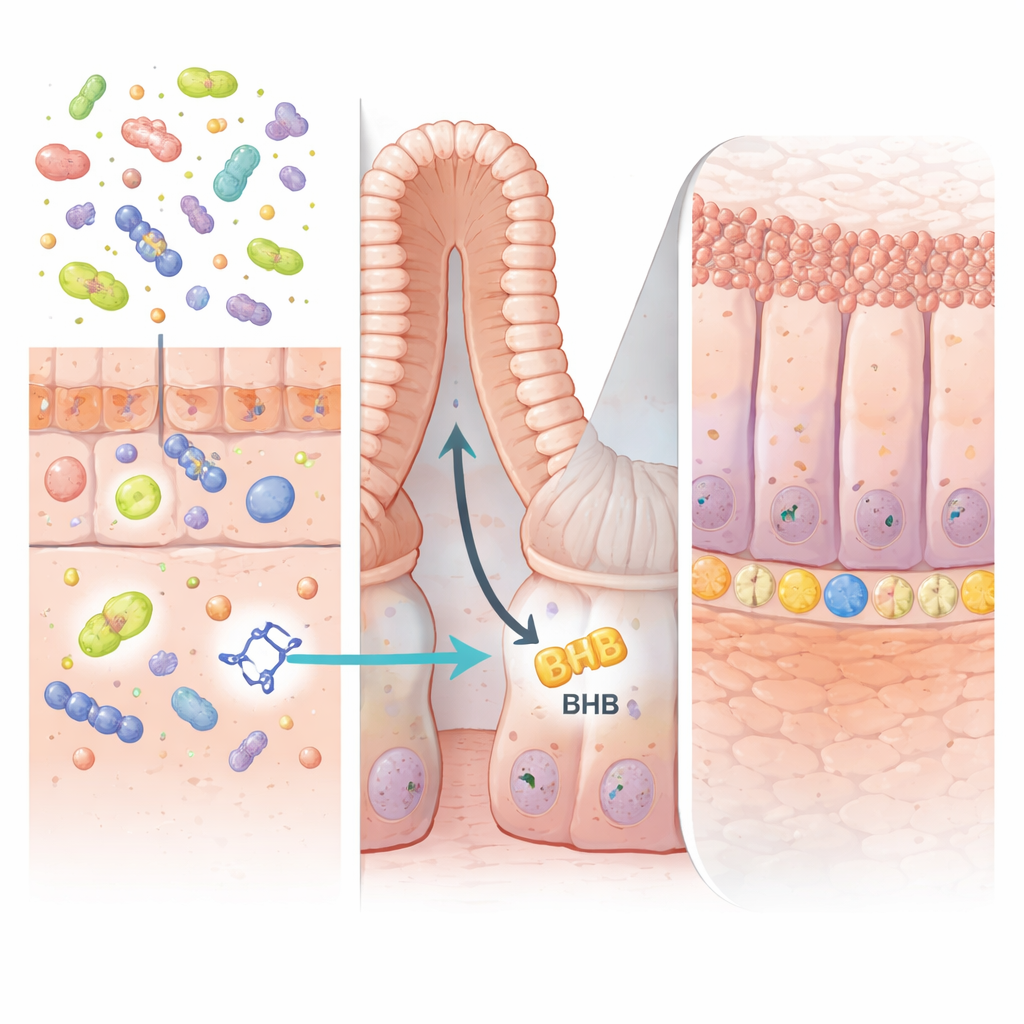
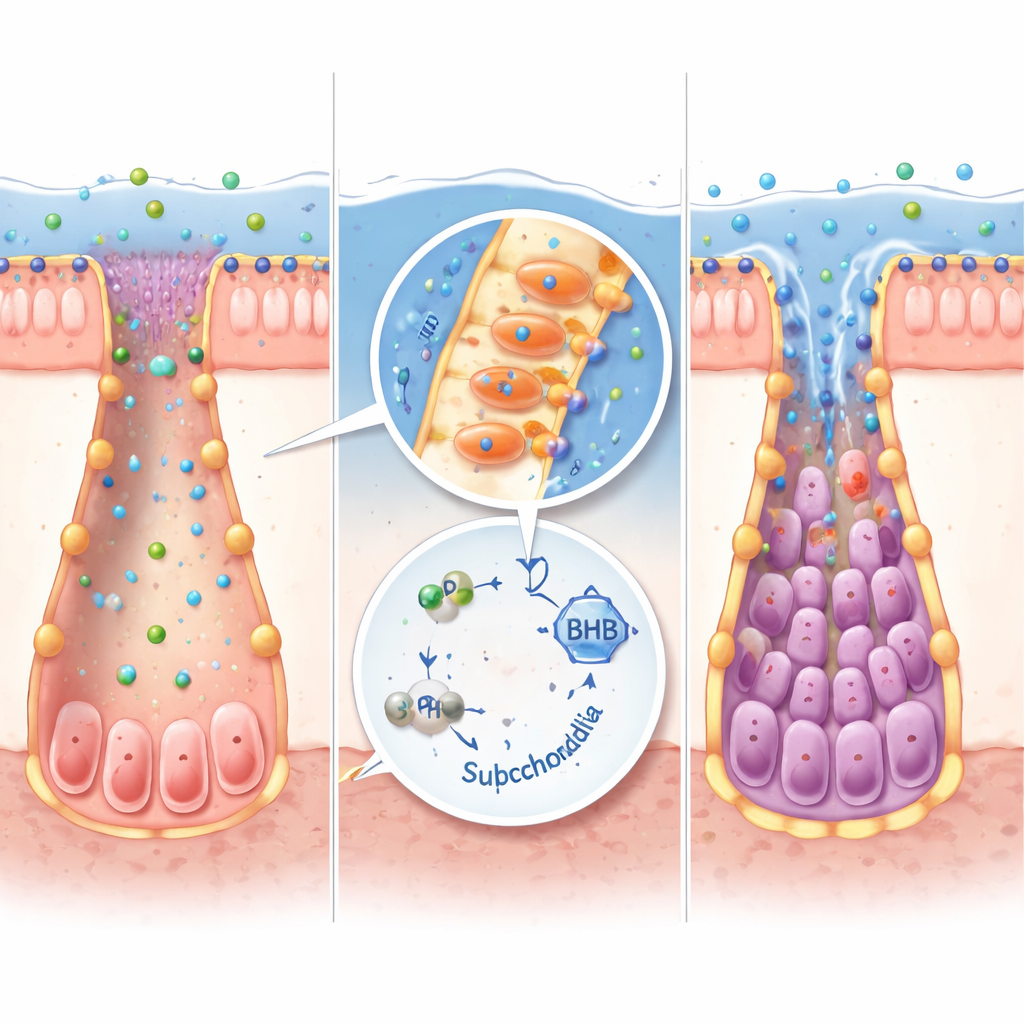
A chave da ação do IPA residia nas profundas “criptas” intestinais, as pequenas cavidades onde as células-tronco ficam e renovam constantemente o revestimento. Os autores mostraram que o IPA ativa uma proteína chamada PPARα nas células epiteliais intestinais. Isso, por sua vez, aumenta a produção de uma enzima chamada HMGCS2, que impulsiona a cetogênese — o processo de produção da molécula rica em energia β-hidroxibutirato (BHB). Níveis elevados de BHB na parede intestinal estimularam a expansão de células-tronco LGR5-positivas e a regeneração mais rápida do tecido danificado. Quando a enzima HMGCS2 ou o PPARα foram seletivamente deletados das células intestinais em camundongos, o IPA deixou de aumentar a atividade das células-tronco ou proteger contra a colite, confirmando que essa via produtora de corpos cetônicos é essencial.
De fábricas bacterianas a tecidos humanos
Nem todas as bactérias intestinais conseguem produzir IPA. Ao reanalisar grandes conjuntos de dados do microbioma, os pesquisadores identificaram Peptostreptococcus russellii como um importante produtor de IPA que está diminuído em várias coortes de DII. Em culturas laboratoriais, essa bactéria converteu triptofano em IPA de forma eficiente. Quando camundongos livres de germes foram colonizados com P. russellii, seus níveis de IPA aumentaram, genes produtores de cetonas foram ativados, marcadores de células-tronco aumentaram e a gravidade da colite diminuiu em comparação com camundongos que receberam um transplante microbiano genérico. A mesma via IPA–cetonas funcionou em organoides intestinais em miniatura cultivados a partir de tecidos de camundongo e humanos, onde a adição de IPA ou BHB ajudou as células-tronco a se recuperar após dano inflamatório enquanto reduzia sinais pró-inflamatórios.
O que isso pode significar para tratamentos futuros
Em conjunto, o trabalho delineia uma cadeia de eventos simples, porém poderosa: certas bactérias intestinais convertem o triptofano dietético em IPA; o IPA ativa um interruptor metabólico nas células intestinais; esse interruptor aumenta a produção de BHB; e o BHB, por sua vez, revive as células-tronco que reconstróem o revestimento intestinal. Para pessoas com DII ou outras condições que lesionam a barreira intestinal, terapias que restaurem o IPA ou imitem com segurança seus efeitos — por meio de dieta, probióticos direcionados ou fármacos designer — poderão promover uma verdadeira cicatrização da mucosa sem supressão imune ampla. Embora sejam necessários mais estudos em pacientes, esse eixo micróbio–metabólito–célula-tronco oferece um novo e promissor ângulo para reparar o intestino de dentro para fora.
Citação: Zhang, Y., Tu, S., Shao, X. et al. Microbiota-derived IPA protects against colitis by regulating intestinal HMGCS2-mediated ketogenesis to facilitate mucosal healing. Nat Commun 17, 2437 (2026). https://doi.org/10.1038/s41467-026-69341-z
Palavras-chave: microbioma intestinal, células-tronco intestinais, doença inflamatória intestinal, metabólitos microbianos, cicatrização da mucosa