Clear Sky Science · pt
CD38 degrada MAVS por mitofagia para inibir a secreção de interferon tipo I em células de carcinoma nasofaríngeo e prejudica a imunidade antitumoral mediada por células T CD8+
Por que isso importa para o tratamento do câncer
O carcinoma nasofaríngeo é um câncer que se origina atrás do nariz e é especialmente comum no Leste e Sudeste da Ásia. Medicamentos baseados no sistema imune que liberam as próprias células T do corpo mudaram o prognóstico de alguns pacientes, mas a maioria ainda não se beneficia. Este estudo revela um freio oculto dentro das próprias células tumorais: uma molécula chamada CD38 que silencia discretamente um sistema de alarme interno e enfraquece o ataque das células T CD8 citotóxicas. Entender e desativar esse freio pode fazer com que as imunoterapias existentes funcionem para muito mais pessoas.
Um interruptor oculto nas células tumorais
Os pesquisadores concentraram-se na CD38, uma proteína encontrada em muitas células imunes, mas também presente nas células do carcinoma nasofaríngeo. Trabalhos anteriores associaram a CD38 à resistência contra drogas de checkpoint populares que atingem PD-1 e PD-L1. Aqui, a equipe investigou se a CD38 dentro das células tumorais altera diretamente a capacidade das células T CD8 de reconhecer e destruir essas células. Ao cultivar células tumorais humanas com ou sem CD38 junto a células T CD8 humanas ativadas, descobriram que a remoção da CD38 das células cancerosas tornou as células T muito mais potentes: secretaram níveis mais altos de moléculas-chave de ataque, sobreviveram melhor e eliminaram mais células tumorais. Quando a CD38 foi restituída, a função das células T caiu, apontando a CD38 como um supressor intrínseco tumoral do ataque imune.
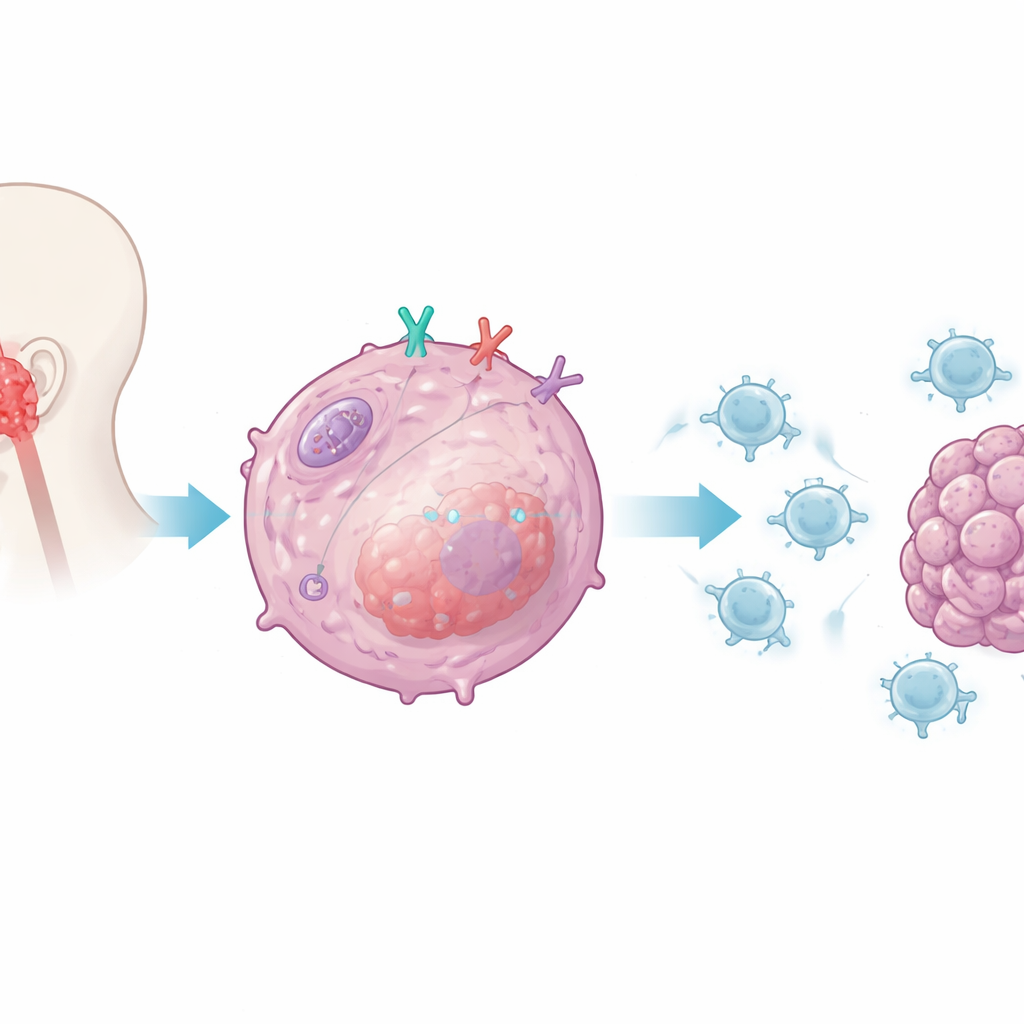
Diminuindo o alarme interno da célula
A equipe então investigou como a CD38 envia esse sinal supressor. Eles focaram no sistema de alarme inato da célula tumoral, que normalmente detecta material genético semelhante a vírus e desencadeia interferons tipo I — mensageiros potentes que estimulam o sistema imune. Em células tumorais sem CD38, os pesquisadores observaram um forte aumento de interferon-beta e de quimiocinas que atraem células T CD8 para os tumores. Demonstraram que a CD38 atenua seletivamente a via controlada por um sensor interno chamado RIG-I e seu adaptador MAVS, que se localiza nas mitocôndrias, as usinas de energia da célula. Quando a CD38 estava presente, a ativação dessa via e de suas moléculas sinalizadoras a jusante era reduzida; quando a CD38 foi removida, a sinalização e a produção de interferon dispararam, aumentando a visibilidade do tumor para o sistema imune.
Como a CD38 destrói um centro de sinalização chave
Aprofundando, os cientistas descobriram que a CD38 se associa fisicamente ao MAVS nas mitocôndrias e interfere na parceria do MAVS com o RIG-I, enfraquecendo a transmissão do sinal. Mais marcante, níveis mais altos de CD38 levaram a uma redução da proteína MAVS sem alterar seu material genético, sugerindo destruição ativa. Testes usando diferentes inibidores mostraram que essa perda dependia da maquinaria de reciclagem da célula conhecida como autofagia, e especificamente de uma forma que mira as mitocôndrias. A CD38 aumentou marcadores de “autofagia mitocondrial”, reduziu várias proteínas mitocondriais e promoveu o empacotamento do MAVS em estruturas autofagossômicas que são posteriormente degradadas. Bloquear a autofagia mitocondrial preservou o MAVS e restaurou a sinalização por interferon, indicando que a CD38 desativa o alarme ao direcionar o MAVS para o fluxo de resíduos da célula.
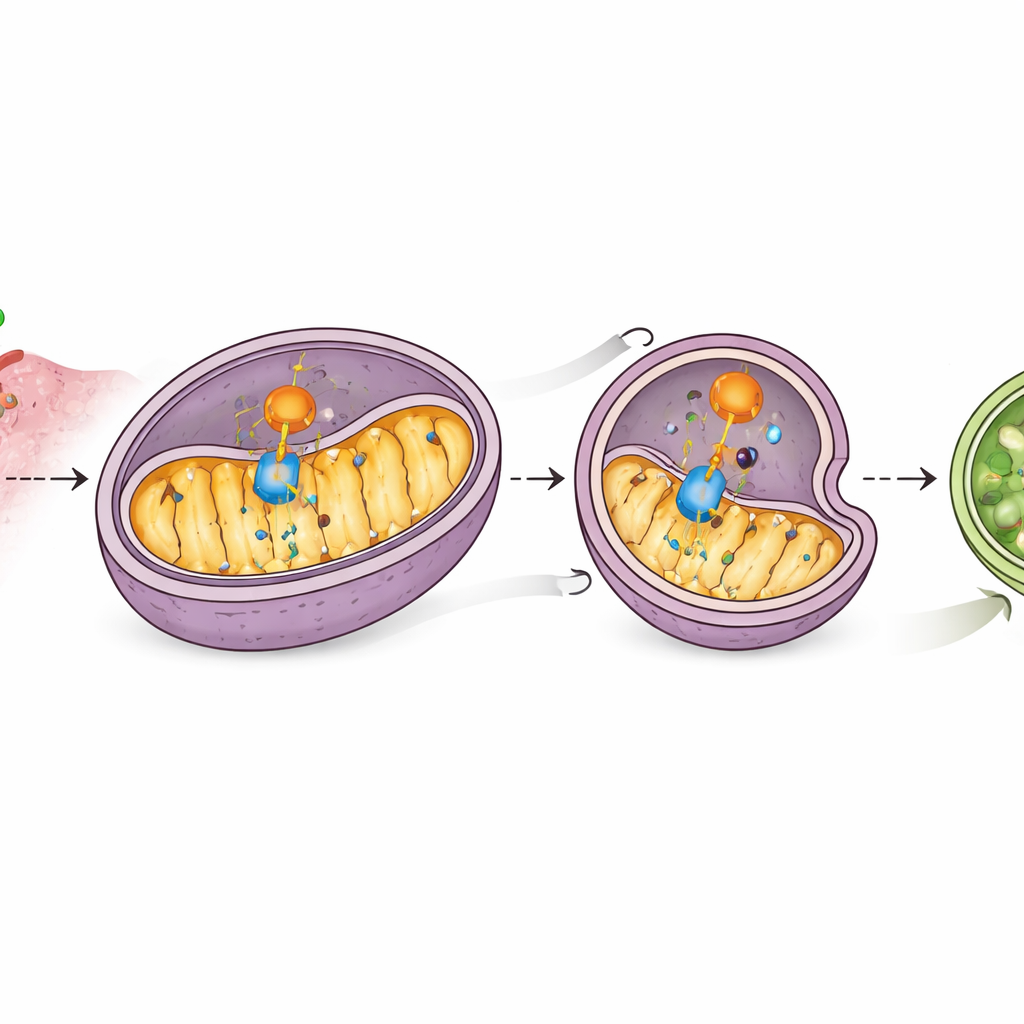
Um auxiliar que guia as mitocôndrias para a autodestruição
O estudo identificou outro ator, PHB2, uma proteína dentro das mitocôndrias que atua como receptor para a remoção seletiva mitocondrial. Espectrometria de massa e experimentos de ligação mostraram que a CD38 interage com a PHB2 e aumenta a presença da PHB2 nas mitocôndrias, onde a PHB2 por sua vez recruta a maquinaria central da autofagia. A PHB2 também se liga ao MAVS, e a CD38 fortalece esse contato. Quando a PHB2 foi reduzida, a CD38 não conseguiu mais desencadear eficazmente a autofagia mitocondrial, os níveis de MAVS se recuperaram e genes relacionados ao interferon foram reativados. Isso revela uma cadeia de eventos: a CD38 envolve a PHB2, a PHB2 envolve o MAVS, e juntos eles conduzem o MAVS para mitocôndrias destinadas à degradação, silenciando o alarme de interferon.
Evidências em modelos animais
Para testar o impacto em organismos vivos, os pesquisadores usaram tumores de camundongos projetados para não expressar CD38. Em camundongos com sistema imune intacto, esses tumores cresceram mais lentamente, continham mais células T CD8 e apresentaram uma fração maior de células produtoras de interferon-gama, um marco de respostas antitumorais ativas. Bloquear o receptor de interferons tipo I removeu essa vantagem, confirmando que a sinalização por interferon é essencial para a imunidade aumentada. Em camundongos humanizados portadores de tumores nasofaríngeos, reduzir a CD38 igualmente retardou o crescimento e aumentou a infiltração de células T CD8, mas esse benefício desapareceu quando o MAVS também foi reduzido nas células tumorais. Esses achados in vivo consolidam a ideia de que o eixo CD38–PHB2–MAVS dentro das células tumorais molda a intensidade da resposta das células T do organismo.
O que isso significa para terapias futuras
No geral, o trabalho mostra que a CD38 em células de carcinoma nasofaríngeo age como um sabotador interno da imunidade antitumoral. Ao promover uma forma seletiva de reciclagem mitocondrial, a CD38 esgota o MAVS, enfraquece a produção de interferon tipo I, reduz a apresentação de antígeno e, em última instância, mitiga o ataque das células T CD8. Compostos atuais que bloqueiam a CD38 atuam principalmente sobre sua atividade enzimática e não removem a proteína nem restauram o MAVS. Os autores argumentam que novas estratégias voltadas a reduzir os níveis de CD38 ou a interromper sua parceria com PHB2 ou MAVS poderiam reativar o alarme de interferon dentro dos tumores. Combinadas com inibidores de checkpoint existentes, tais abordagens podem converter mais carcinomas nasofaríngeos — e potencialmente outros cânceres — de imunologicamente frios a responsivos ao sistema imune.
Citação: Liang, L., Li, W., Liu, S. et al. CD38 degrades MAVS through mitophagy to inhibit type I interferon secretion in nasopharyngeal carcinoma cells and impairs CD8+T cell-mediated anti-tumor immunity. Nat Commun 17, 2544 (2026). https://doi.org/10.1038/s41467-026-69339-7
Palavras-chave: carcinoma nasofaríngeo, imunoterapia tumoral, interferon tipo I, células T CD8, mitofagia