Clear Sky Science · pt
Avaliação comparativa da inferência da via de sinalização EGF usando fosfoproteômica e interações quinase-substrato
Por que isso importa além do laboratório
Nossas células estão constantemente ouvindo e reagindo a sinais do ambiente. Um dos mais importantes é o fator de crescimento epidérmico (EGF), que ajuda a controlar como as células crescem, se dividem e sobrevivem. Quando esse sistema de comunicação falha, ele pode impulsar cânceres e outras doenças. Este estudo faz uma pergunta aparentemente simples, mas com grandes implicações: se usarmos as tecnologias de medição e os modelos computacionais avançados de hoje, o quanto realmente podemos melhorar nossa compreensão da via de sinalização do EGF em comparação com o que aparece nos diagramas dos livros didáticos?
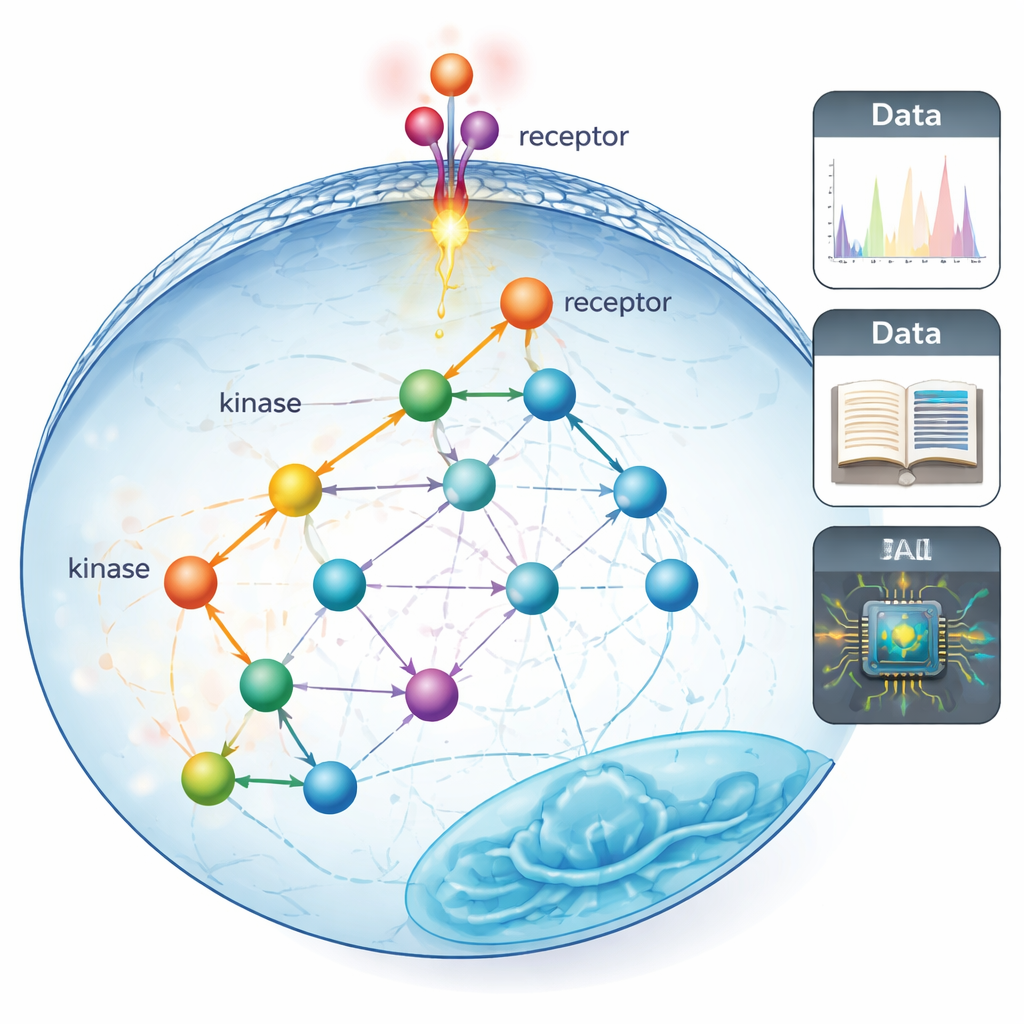
De linhas retas a diagramas de fiação da vida real
As “vias de sinalização” tradicionais são frequentemente desenhadas como cadeias arrumadas e quase lineares de proteínas que passam uma mensagem da superfície celular até o núcleo. Esses mapas foram construídos ao longo de décadas usando experimentos direcionados e lentos que podiam observar apenas algumas proteínas por vez. Os autores argumentam que isso nos deixou com uma visão estreita, como se víssemos apenas sob o poste de luz: sabemos muito sobre as poucas proteínas que eram fáceis de estudar e muito menos sobre a teia mais ampla de conexões que provavelmente existe em células reais.
Ouvindo milhares de interruptores moleculares ao mesmo tempo
Para ir além dessa visão limitada, a equipe usou fosfoproteômica, uma técnica de espectrometria de massa que pode rastrear dezenas de milhares de pequenos rótulos químicos chamados grupos fosfato em proteínas em um único experimento. Esses rótulos são colocados por enzimas chamadas quinases e atuam como interruptores rápidos liga/desliga para a sinalização. Os pesquisadores primeiro montaram os mapas mais abrangentes de “quem pode fosforilar quem” até hoje, mesclando três tipos de informação: achados curados da literatura, previsões de um modelo de inteligência artificial que lê sequências de proteínas e grandes triagens experimentais das preferências das quinases. Isso expandiu muito a cobertura de relações quinase–substrato conhecidas ou suspeitas, de cerca de 5% dos sítios mensuráveis para algo entre 70–80%.
Colocando à prova a sinalização EGF em muitos experimentos
Em seguida, eles focaram na resposta ao EGF, uma via clássica e um ator importante em cânceres de pulmão, mama, pele e cérebro. O grupo combinou três conjuntos de dados publicados de ponta com três novas medições temporais muito profundas em células derivadas do rim, além de dois estudos de controle com estímulos diferentes. Juntos, esses experimentos mediram mais de 40.000 sítios de fosforilação por conjunto de dados e acompanharam como eles aumentaram ou diminuíram nos minutos após a estimulação por EGF. Embora os padrões gerais variassem um pouco entre tipos celulares e tecnologias, sítios de fosforilação-chave na via EGF foram repetidamente ativados, confirmando que o sinal central é robusto mesmo em experimentos diversos.
Reconstruindo a conversa oculta entre as quinases
Tendo inferido quais quinases ficaram mais ou menos ativas, os autores então tentaram reconstruir a “conversa” subjacente entre elas: quais quinases provavelmente ativam ou influenciam outras. Eles converteram seus mapas quinase–substrato em redes quinase–quinase e aplicaram três estratégias computacionais, que vão de esquemas de ranqueamento simples a uma abordagem mais complexa que força o resultado a se parecer com uma árvore direcionada enraizada no receptor de EGF. Compararam as vias inferidas com vários tipos de “verdade de referência”: um mapa EGF cuidadosamente curado de um banco de dados, experimentos em larga escala onde quinases individuais foram superexpressas e pares de sítios de quinase cujo comportamento foi fortemente correlacionado ao longo do tempo.
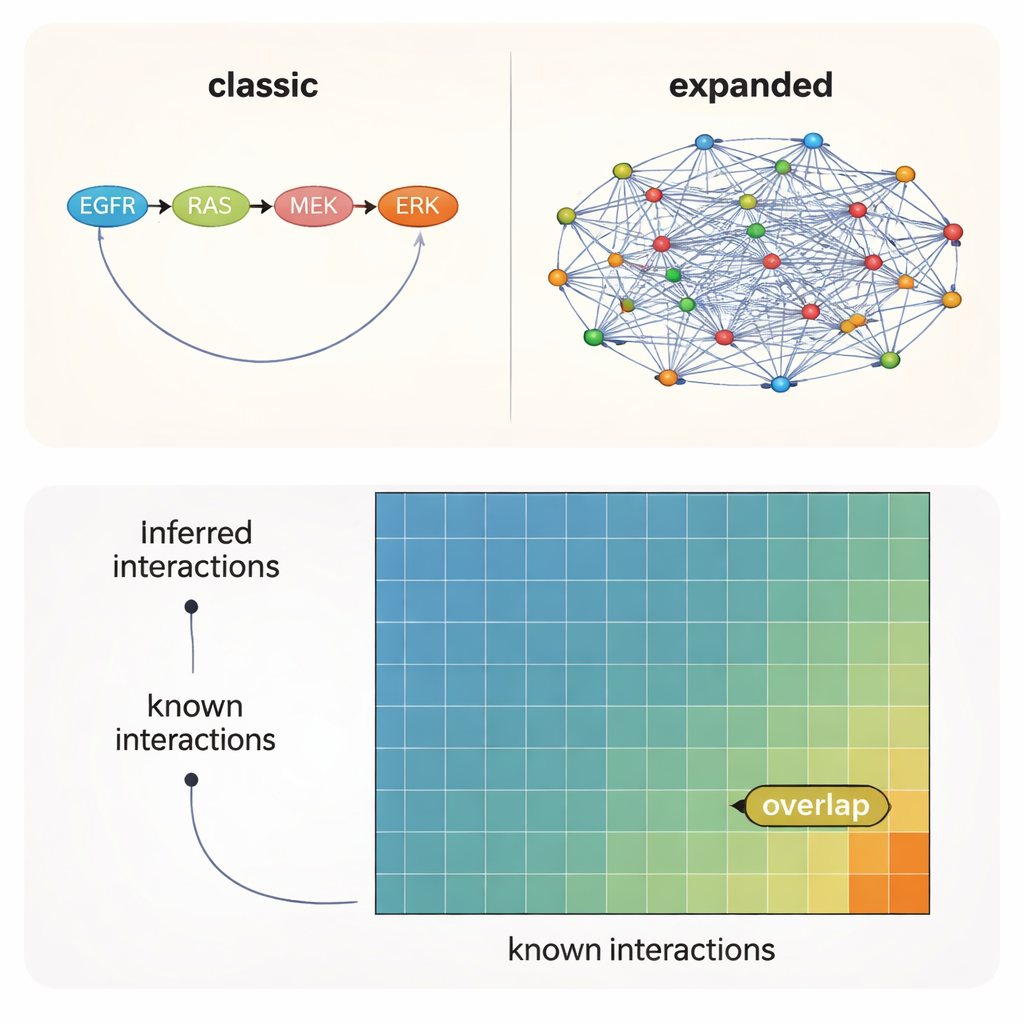
Os links mais plausíveis ainda estão fora do mapa oficial
Em todos os testes, uma mensagem ficou clara: a escolha do conhecimento prévio — qual rede inicial você fornece ao algoritmo — importou mais do que o método em si ou até o contexto experimental. Redes construídas a partir da literatura recuperaram o maior número de interações conhecidas, enquanto recursos preditivos mais amplos apontaram muitas conexões adicionais plausíveis que ainda não foram documentadas formalmente. Mesmo nas melhores condições, no entanto, apenas cerca de 10–12% das interações sugeridas pelos dados e modelos estavam presentes em qualquer um dos conjuntos de referência. Em outras palavras, aproximadamente 90% das ligações quinase–quinase suportadas ficam em território inexplorado.
O que isso significa para tratamentos futuros
Para não especialistas, a conclusão é que o conhecido diagrama da via EGF nos livros didáticos provavelmente é apenas a ponta do iceberg. A fosfoproteômica moderna combinada com métodos computacionais avançados revela uma rede de sinalização muito mais rica e entrelaçada. Muitas dessas conexões recém-sugeridas podem representar maneiras negligenciadas pelas quais células cancerosas redirecionam sinais para escapar de drogas, ou novas oportunidades para desenhar combinações de medicamentos mais inteligentes. O estudo não prova que todo novo link seja real, mas fornece um roteiro e ferramentas abertas para que pesquisadores testem essas ideias, com o objetivo final de terapias mais precisas e eficazes em doenças onde a sinalização EGF desempenha um papel central.
Citação: Garrido-Rodriguez, M., Potel, C., Burtscher, M.L. et al. Benchmarking EGF signaling pathway inference using phosphoproteomics and kinase-substrate interactions. Nat Commun 17, 2071 (2026). https://doi.org/10.1038/s41467-026-69332-0
Palavras-chave: Sinalização EGF, fosfoproteômica, quinases proteicas, redes de sinalização celular, biologia do câncer