Clear Sky Science · pt
Mycobacterium tuberculosis modula a fosforilação da ATP6V1E1 da célula hospedeira para promover sobrevivência intracelular
Por que isso importa para combater a tuberculose
A tuberculose continua sendo uma das doenças infecciosas mais letais do mundo, matando mais de um milhão de pessoas por ano. Nossas células imunes dispõem de poderosos “recipientes ácidos de reciclagem” que normalmente digerem micróbios invasores. Este artigo revela como a bactéria da tuberculose, Mycobacterium tuberculosis (Mtb), sabota esse sistema de acidificação dentro de nossas células e mostra que uma droga direcionada a esse estratagema pode ajudar animais infectados a eliminar a infecção mais eficazmente.
O banho ácido celular para germes
Quando as bactérias da tuberculose são inaladas para os pulmões, são rapidamente englobadas por células imunes chamadas macrófagos. As bactérias acabam em vesículas de membrana que deveriam se fundir com lisossomos — pequenos sacos cheios de enzimas digestivas que funcionam melhor em um ambiente fortemente ácido. Essa acidez é gerada por uma bomba molecular, a ATPase vacuolar (V-ATPase), que usa combustível celular para empurrar prótons para dentro dos lisossomos e reduzir o pH interno. A acidificação adequada é crucial para degradar Mtb, contudo décadas de trabalho mostram que esse patógeno de algum modo mantém seus compartimentos menos ácidos e sobrevive.
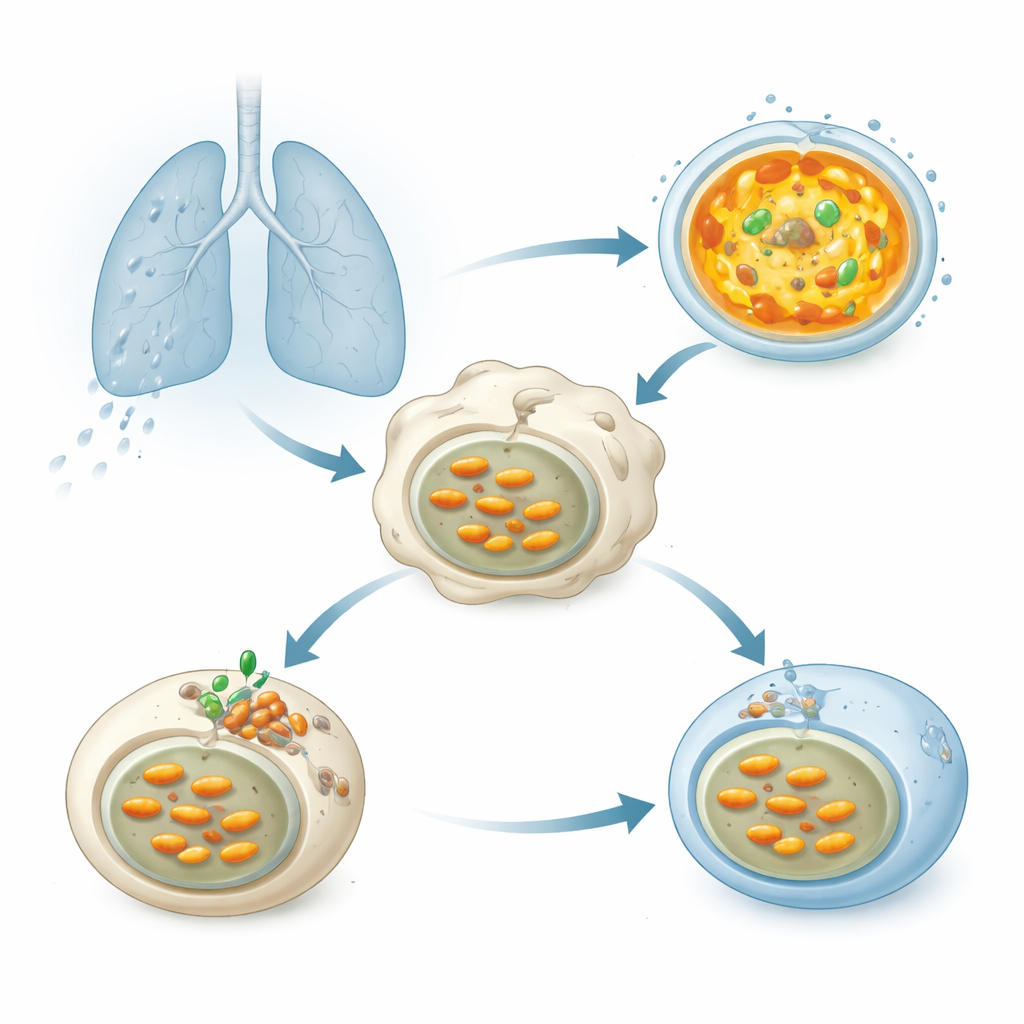
Um ajudante bacteriano secreto que bloqueia a acidificação
Os pesquisadores triaram mais de 200 proteínas que a Mtb pode liberar para ver quais enfraquecem a acidificação lisossomal em células humanas. Uma delas se destacou: uma enzima chamada Chp2 (também conhecida como Rv1184). Quando as células produziam Chp2, seus lisossomos mostraram menor intensidade com corantes sensíveis ao ácido, indicando um pH mais alto, menos hostil. Cepas de Mtb engenheiradas para não produzir Chp2 não suprimiam mais a acidificação; em macrófagos infectados e em camundongos, essas bactérias mutantes foram eliminadas com mais eficiência e causaram danos pulmonares mais leves. Restaurar Chp2 na cepa mutante devolveu tanto o bloqueio da acidificação quanto a maior carga bacteriana, identificando Chp2 como um fator de virulência que ajuda a Mtb a persistir dentro das células hospedeiras.
A subunidade da bomba do hospedeiro que age como um interruptor de controle
Para entender como Chp2 interfere na acidificação, a equipe procurou componentes do hospedeiro aos quais ele pudesse se ligar. Descobriram que Chp2 se anexa diretamente a uma parte específica da V-ATPase, uma subunidade chamada ATP6V1E1 (E1, para abreviar), que ajuda a estabilizar a estrutura da bomba. Aumentar a quantidade de E1 nas células elevou a acidificação lisossomal e tornou mais difícil a sobrevivência da Mtb, enquanto reduzir E1 teve o efeito oposto. Camundongos que carregavam apenas uma cópia funcional do gene E1 apresentaram lisossomos menos ácidos, maiores cargas bacterianas nos pulmões e danos teciduais mais severos após a infecção, mostrando que E1 é um defensor importante do hospedeiro contra a tuberculose.
Uma marca de quinase na bomba que diminui a acidez
Os autores então perguntaram se “marcas” químicas na E1 poderiam ajustar a atividade da bomba. Eles descobriram que adicionar grupos fosfato a duas tirosinas específicas (Tyr56 e Tyr57) em E1 atua como um freio: mimetizar a fosforilação reduziu a acidificação e impediu a montagem completa da V-ATPase, enquanto impedir a fosforilação teve o efeito contrário. Ao examinar um painel de enzimas, identificaram uma quinase chamada BMX como a proteína do hospedeiro que coloca essa marca. Quando o BMX foi bloqueado geneticamente ou com um inibidor de pequenas moléculas, a fosforilação de E1 diminuiu, a bomba montou-se de forma mais eficiente nas membranas lisossomais, os lisossomos tornaram-se mais ácidos e a sobrevivência da Mtb dentro dos macrófagos caiu.
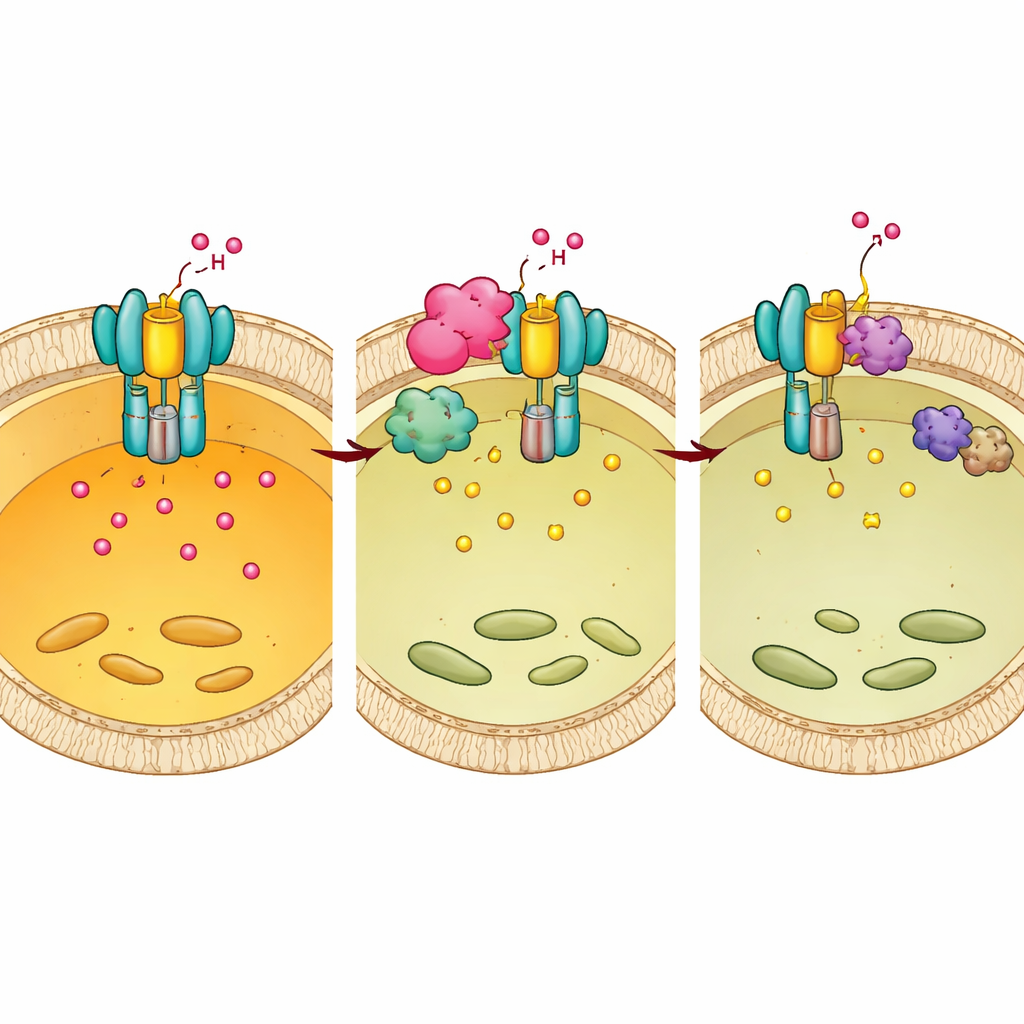
Como a Mtb reconfigura o interruptor do hospedeiro a seu favor
Chp2 e BMX mostram-se operando em conjunto. Experimentos estruturais e bioquímicos demonstraram que Chp2 atua como um andaime que aproxima E1 e BMX na superfície lisossomal, potencializando a fosforilação de E1 em Tyr56/57. Essa marcação extra atrapalha a montagem completa da bomba, eleva o pH lisossomal e cria um ambiente mais brando no qual a Mtb pode persistir. Quando o BMX foi inibido, a vantagem de sobrevivência conferida por Chp2 desapareceu, tanto em células cultivadas quanto em camundongos infectados. Importante, tratar camundongos com o inibidor de BMX após a infecção reduziu cargas bacterianas e a patologia pulmonar em animais normais, mas não em camundongos com E1 enfraquecida, indicando que a droga age restaurando a acidificação efetiva mediada por E1.
Transformando o truque do patógeno em uma ideia de tratamento
Em termos cotidianos, este estudo mostra que as bactérias da tuberculose introduzem uma proteína auxiliar em nossas células que interfere na “bomba ácida” do descarte, reduzindo-a o suficiente para que os micróbios escapem da destruição. Ao identificar a subunidade da bomba que serve como o botão de controle (E1) e a enzima do hospedeiro que a aciona (BMX), os autores revelam um ponto preciso onde um medicamento pode intervir. Inibir o BMX em camundongos reativa de forma eficaz o banho ácido interno da célula e melhora a eliminação bacteriana. Essas descobertas abrem caminho para terapias direcionadas ao hospedeiro que tornam nossas próprias células mais hostis à Mtb, potencialmente complementando antibióticos e ajudando a combater a tuberculose resistente a medicamentos.
Citação: Chen, J., Tang, F., Qin, L. et al. Mycobacterium tuberculosis modulates phosphorylation of host ATP6V1E1 to promote intracellular survival. Nat Commun 17, 2434 (2026). https://doi.org/10.1038/s41467-026-69331-1
Palavras-chave: tuberculose, lisossomos, terapia direcionada ao hospedeiro, Mycobacterium tuberculosis, V-ATPase