Clear Sky Science · pt
Rede neuronal pré-óptica kisspeptina-nNOS-GnRH (KiNG) regula a ritmicidade de LH por ativação-inibição em camundongos
Por que esta história cerebral importa para a fertilidade
A ovulação e a fertilidade dependem de um grupo minúsculo de células cerebrais que liberam um hormônio mestre em pulsos e em surtos ocasionais. Quando esse temporizador falha, a reprodução pode ser comprometida. Este estudo revela como dois tipos de moléculas sinalizadoras no cérebro de camundongos — uma que liga a atividade e outra que silenciosamente a desliga novamente — trabalham em conjunto para moldar esses ritmos hormonais. Entender esse circuito temporal oculto pode, em última instância, ajudar a explicar certas formas de infertilidade e sugerir novas maneiras de tratar distúrbios reprodutivos.
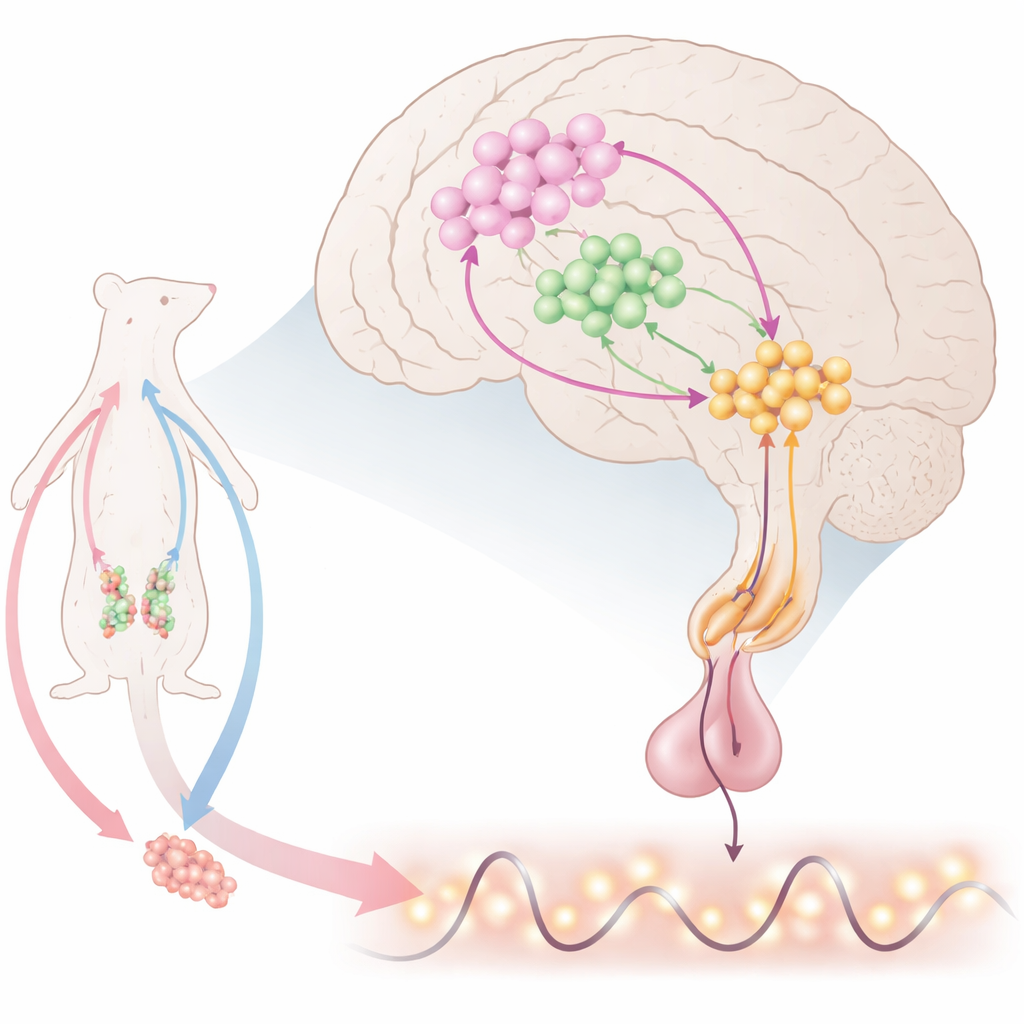
O cronômetro cerebral para a reprodução
Nas profundezas do cérebro, células nervosas especiais liberam o hormônio liberador de gonadotrofina (GnRH), que diz à hipófise para liberar hormônio luteinizante (LH) e hormônio folículo-estimulante. Estes, por sua vez, controlam os ovários e os testículos. O GnRH não é liberado de forma contínua; em vez disso, aparece como pulsos regulares e, nas fêmeas, um grande surto pré-ovulatório. Os cientistas sabem que muitos sinais convergem sobre as células de GnRH, mas a combinação exata que produz tanto pulsos quanto surtos permaneceu pouco clara. Este trabalho foca em uma pequena região na frente do hipotálamo, onde as células de GnRH se misturam com dois outros atores importantes: neurônios produtores de kisspeptina, que excitam o GnRH, e neurônios que fabricam óxido nítrico (NO), um sinal gasoso capaz de difundir por curtas distâncias.
Uma parceria liga–desliga entre dois sinais
Os pesquisadores propõem uma rede tripartite “KiNG”, composta por kisspeptina, neurônios produtores de NO (nNOS) e células de GnRH. A kisspeptina é um potente ativador que pode impulsionar a liberação de GnRH e LH, mas a estimulação constante na verdade desliga o sistema, sugerindo que um freio interno é necessário. Usando sondas moleculares altamente sensíveis, ferramentas genéticas e registros em cortes cerebrais em camundongos, a equipe demonstra que a kisspeptina faz mais do que excitar diretamente os neurônios de GnRH. Ela também ativa neurônios nNOS próximos na área pré-óptica, especialmente em uma região chamada OV/MePO. Quando os níveis de kisspeptina aumentam, essas células nNOS produzem rajadas de NO, que desencadeiam a produção de um segundo mensageiro, o cGMP, em células circundantes, incluindo as próprias neurônios de GnRH. Esse sinal NO–cGMP reduz o disparo de GnRH, fornecendo um interruptor de desligamento embutido ao impulso da kisspeptina.
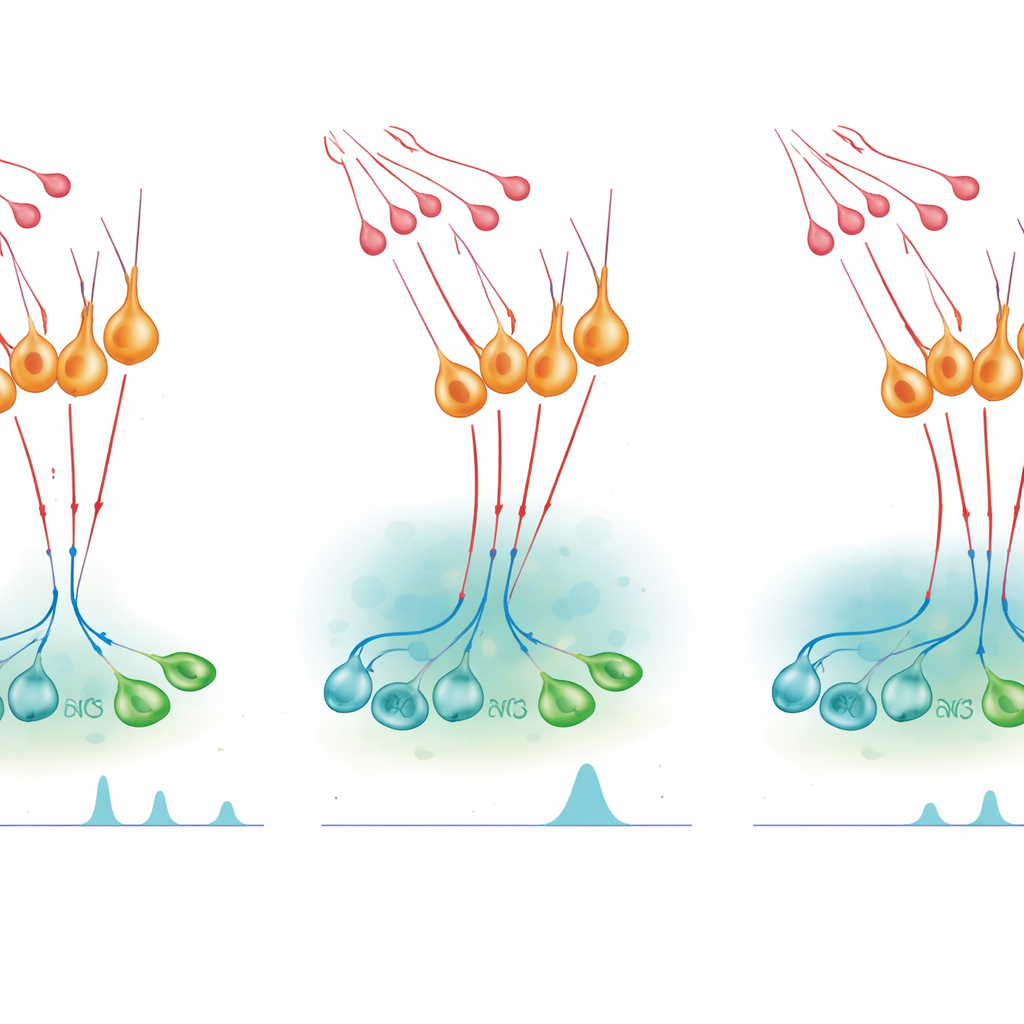
Ligando surtos hormonais e contê-los
Para testar como esse microcircuito afeta a liberação hormonal, a equipe usou chaves quimio-genéticas — receptores projetados ativados por uma droga inerte — para ativar ou desativar neurônios nNOS em camundongos vivos. Ativar artificialmente as células nNOS durante uma fase normalmente silenciosa do ciclo feminino foi suficiente para produzir um aumento no LH semelhante a um surto, e o mesmo ocorreu em machos. Bloquear a produção de NO aboliu esse efeito, mostrando que o NO desses neurônios é necessário para o surto. Ainda assim, quando os cientistas inibiram os neurônios nNOS ou reduziram sua sensibilidade à kisspeptina, uma injeção de kisspeptina produziu uma elevação exagerada e prolongada de LH. Fármacos que bloqueiam a síntese de NO tiveram efeito amplificador semelhante, enquanto um medicamento que prolonga o sinal do cGMP encurtou a resposta à kisspeptina e reduziu a liberação subsequente de LH. Em conjunto, esses experimentos indicam que o NO tanto ajuda a sincronizar os neurônios de GnRH para criar surtos quanto limita quanto tempo a kisspeptina pode mantê‑los ativados.
Um ritmo flexível ao longo do ciclo ovariano
O estudo também revela que esse equilíbrio liga–desliga muda ao longo do ciclo feminino. Usando um método sensível de detecção de RNA, os autores observaram que mais neurônios nNOS expressam o receptor de kisspeptina no dia anterior à ovulação, quando os níveis de estrogênio estão altos e ocorre o surto de LH. Durante as fases mais silenciosas, menos neurônios nNOS respondem à kisspeptina, produzindo apenas pequenas quantidades locais de NO que contêm suavemente os pulsos de GnRH sem interrompê‑los. No dia do surto, uma entrada de kisspeptina mais intensa e a expressão aumentada do receptor aumentam massivamente a produção de NO, permitindo que o NO se espalhe mais e silencie temporariamente muitos neurônios de GnRH ao mesmo tempo. À medida que o sinal de NO desaparece, essas células se recuperam em conjunto, gerando o grande e coordenado surto de LH necessário para a ovulação.
O que isso significa para a saúde humana
Em termos simples, este trabalho mostra que o mesmo sinal que inicia os neurônios de GnRH — a kisspeptina — também recruta um sistema de freio retardado por meio do NO, garantindo que os surtos hormonais sejam fortes, mas não descontrolados. A rede KiNG age, portanto, tanto como acelerador quanto como freio do tempo reprodutivo, ajustando os pulsos de GnRH durante a maior parte do ciclo e moldando o surto que desencadeia a ovulação. Como alterações genéticas nas vias da kisspeptina e do NO foram encontradas em pessoas com problemas reprodutivos, entender esse circuito de equilíbrio fino pode orientar novas abordagens para diagnosticar e tratar infertilidade e condições relacionadas.
Citação: Delli, V., Moulinier, M., Lazaridou, AM. et al. Preoptic kisspeptin-nNOS-GnRH (KiNG) neuronal network regulates LH rhythmicity through activation-inhibition in mice. Nat Commun 17, 2558 (2026). https://doi.org/10.1038/s41467-026-69316-0
Palavras-chave: hormônios reprodutivos, hipotálamo, kisspeptina, óxido nítrico, tempo da ovulação